- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Человек и эволюция: старение или молодость?
Содержание
- 2. Эволюцию не остановить. Но может ли человек повлиять на эволюцию?
- 3. Мир меняется все быстрее, реальным стало многое
- 4. По прогнозам ряда известных ученых, скоро люди
- 5. Задача отменить старение организма, уже перешла в
- 6. Если обратить внимание на ускоряющиеся темпы совершенствования
- 7. У Вас есть шанс прожить, сколько пожелаете,
- 8. Трудно представить задачу, более достойную приложения сил,
- 9. Причины старения.Существует около сотни гипотез объясняющих природу
- 10. Скорее всего, нет единой причины, по которой
- 11. Есть серьёзные основания ожидать
- 12. Свободные радикалы.Кислород заставляет железо ржаветь,
- 13. Агрессивные формы кислорода или оксиданты необходимы организму,
- 14. Свободные радикалы - это молекулы
- 15. Пострадавшие молекулы стремятся отнять электрон у других
- 16. Подробнее об этих маленьких убийцах:Оксиданты образуются в
- 17. Борьба со свободными радикалами идет несколькими путями:
- 18. Лимит Хейфлика.Как известно из начального курса биологии,
- 19. Не смотря на то, что "лимит Хейфлика"
- 20. Клетки человека обладают способностью делиться 50–60 раз.
- 21. Таким образом, теломераза и стала причиной спасения ЕДИНИЧНЫХ
- 22. К тому же, поддержание длины теломерной ДНК
- 23. Апоптоз и старение.Апоптоз - это биологический ассенизатор.
- 24. Мировая наука освятила апоптоз отдельной клетки. За
- 25. Польза и вред апоптоза.Если апоптоз выходит из-под
- 26. Апоптоз и клеточное старение.Группа канадских биологов нейтрализовала
- 27. Некоторые старые клетки, утратившие способность к делению,
- 28. Гипотеза о самоубийстве организма.Академиком Скулачевым В.П. выдвинуто
- 29. Гены старения.Если бы существовали гены целиком ответственные
- 30. Старение человека обусловлено не одним,
- 31. Гены, определяющие МЕЖВИДОВЫЕ различия продолжительности жизни действительно
- 32. Скачать презентацию
- 33. Похожие презентации
Эволюцию не остановить. Но может ли человек повлиять на эволюцию?




























Слайд 4 По прогнозам ряда известных ученых, скоро люди перестанут
умирать по причинам связанным со старением организма, даже некоторые
из живущих сегодня уже смогут избежать этого и получат возможность оставаться в состоянии физического и умственного здоровья столько, сколько пожелают.Слайд 5 Задача отменить старение организма, уже перешла в ранг
инженерных проектов, сегодня вопрос стоит скорее, не как именно
это сделать, а какое из направлений окажется первым, доведенным до практического использования. Средством для победы над старением становится комплекс высоких технологий: наномедицина, генная инженерия, биотехнологии и др.Слайд 6 Если обратить внимание на ускоряющиеся темпы совершенствования технологий,
становится ясно, что даже терапии замедления старения первого поколения
– той, что даст вам всего лишь несколько дополнительных десятилетий, наверняка будет достаточно, чтобы вы не умирали от старения в любом возрасте. Т.к. за те дополнительные 30-ть лет сами технологии разовьются на столько что позволят вам прожить еще 50-т лет и т.д. При этом с календарным возрастом вероятность смерти по причине связанной со старением будет только падать.Слайд 7 У Вас есть шанс прожить, сколько пожелаете,
а не те жалкие восемьдесят лет, отпущенные нашим эволюционным прошлым.
Слайд 8 Трудно представить задачу, более достойную приложения сил, чем
борьба с собственным старением и смертью. Не пытаться бороться
с ними - противоестественно, во всяком случае, сейчас, когда для этого появляются серьёзные научные средства.Общественное сознание очень инертно, глубоко укоренилась установка что старость и смерть от нее неизбежны, большинство просто приняло это как должное. Такой стереотип мышления основан на том, что так было всегда, однако уже стало реальностью многое из того, что несколько поколений назад люди, не могли себе даже представить.
Слайд 9
Причины старения.
Существует около сотни гипотез объясняющих природу старения,
однако, научным сообществом из всего этого многообразия признано не
более десятка концепций.Большинство специалистов сходится во мнении, что старение является феноменом, включающим целый комплекс взаимозависимых процессов.
Слайд 10 Скорее всего, нет единой причины, по которой мы
стареем, (допустим, износ или самоубийство клеток), а есть целый
ряд причин, суммарное действие которых и вызывает разрушительные последствия, которым придуман обобщенный термин - старение.Причем, такие разрушительные изменения происходят на клеточном, организменном, и молекулярном уровнях. Вероятно, многие конкурирующие теории старения правы по-своему, а каждая из них даёт лишь часть общей картины.
Слайд 11 Есть серьёзные основания ожидать
в ближайшие десятилетия перехода в стадию практического применения накопленных знаний. Можно ожидать достижения уровня науки и техники, необходимого для многократного увеличения продолжительности жизни, ближе к середине 21-го века.
Слайд 12
Свободные радикалы.
Кислород заставляет железо ржаветь,
а масло -
становиться прогорклым.В процессе жизнедеятельности в нашем организме образуются агрессивные формы кислорода (свободные радикалы , они же оксиданты) и провоцируют процессы, сходные с ржавлением или гниением, это разложение буквально съедает нас изнутри.
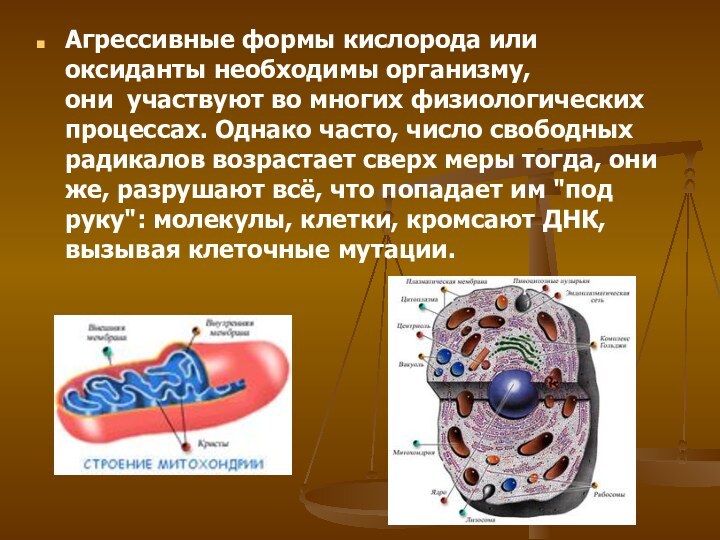
Слайд 13 Агрессивные формы кислорода или оксиданты необходимы организму, они
участвуют во многих физиологических процессах. Однако часто, число свободных
радикалов возрастает сверх меры тогда, они же, разрушают всё, что попадает им "под руку": молекулы, клетки, кромсают ДНК, вызывая клеточные мутации.Слайд 14 Свободные радикалы - это молекулы
с неспаренным электроном.
Они весьма нестабильны и очень легко вступают в химические реакции. Такая нестабильная частица, сталкиваясь с другими молекулами, "крадет" у них электрон, что существенно изменяет структуру этих молекул.
Слайд 15 Пострадавшие молекулы стремятся отнять электрон у других "полноценных"
молекул, вследствие чего развивается разрушительная цепная реакция, губительно действующая
на живую клетку. Цепные реакции с участием свободных радикалов могут являться причиной многих опасных заболеваний.Установлено, что свободные радикалы отнимают у нас не один десяток лет жизни! Научно доказано что Свободные радикалы, повинны в развитии таких болезней, как: рак, атеросклероз, инфаркт, инсульт, ишемия, атеросклероз, заболевания нервной и иммунной систем и заболевания кожи.
Слайд 16
Подробнее об этих маленьких убийцах:
Оксиданты образуются в нашем
теле четырьмя способами “Фабриками” свободных радикалов служат маленькие продолговатые
тельца внутри клетки — митохондрии, ее энергетические станции.Возникнув в клетке, радикалы повреждают ее внутренние структуры, а также оболочки самих митохондрий, что усиливает утечку.
В результате становится все больше и больше активных форм кислорода, и они разрушают клетку.
Слайд 17 Борьба со свободными радикалами идет несколькими путями: с
помощью препаратов - "ловушек", нейтрализующих уже имеющиеся свободные радикалы,
и средств, препятствующих образованию свободных радикалов.Например, биофлавоноиды, открытые Альбертом Сент-Георги обладают способностью связывать свободные радикалы.
Слайд 18
Лимит Хейфлика.
Как известно из начального курса биологии, клетки
обладают способностью делиться. И
какое-то время они это охотно делают.Однако, со временем, клетки утрачивают способность к самовоспроизведению. Это явление получило название "лимит Хейфлика" . Человеческая клетка в состоянии делиться всего 50—70 раз.
Слайд 19
Не смотря на то, что "лимит Хейфлика" это
ограничитель не позволяющий жить бесконечно долго, есть мнение, что
сей ресурс не вырабатывается за время жизни современного человека. Так Алексей Оловников (первый кто предположил о существовании теломер) говорит: действие теломер доказано, однако к старению сегодня, это не имеет прямого отношения. Каждый курильщик со временем умрет от рака - только не все доживают до момента, когда это произойдет, вероятно, так и с теломерами.Слайд 20 Клетки человека обладают способностью делиться 50–60 раз. В
опытах группы "Герон" после введения теломеразы клетка дает свыше
100 делений. Ракового перерождения клеток не происходит.В январе 1998 года средства массовой информации во всем мире буквально взорвались сообщениями о том, что группе американских ученых удалось заставить нормальные клетки человека преодолеть "лимит Хейфлика".
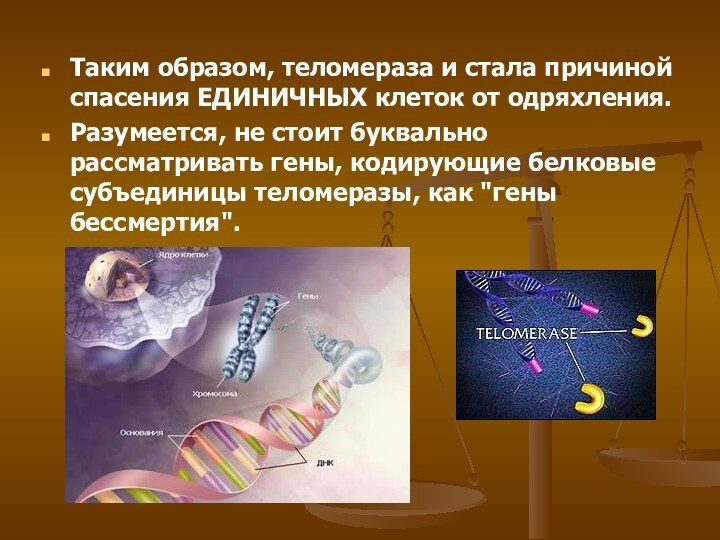
Слайд 21 Таким образом, теломераза и стала причиной спасения ЕДИНИЧНЫХ клеток
от одряхления.
Разумеется, не стоит буквально рассматривать гены, кодирующие белковые
субъединицы теломеразы, как "гены бессмертия". Слайд 22 К тому же, поддержание длины теломерной ДНК на
определённом уровне зависит не только от взаимодействия с ней
теломеразы и теломерсвязывающих белков, но и от других, пока неизвестных факторов, регулирующих образование самих компонентов теломер-образующего комплекса.Но тот факт, что введение в раковые клетки HeLa препаратов, блокирующих РНК-компонент теломеразы, приводит к укорочению теломер и последующей гибели клеток, вселяет надежду на появление новых средств борьбы с раком.
Слайд 23
Апоптоз и старение.
Апоптоз - это биологический ассенизатор.
Он включает гибель (саморазрушение) неправильно развивающейся,
потенциально опасной или просто ненужной для окружающих тканей клетки, апоптоз предохраняет организм.К примеру, на апоптозе основана и защита от раковых заболеваний - соседи раковой клетки убивают себя, образуя “мертвую зону”, и только сбой в программе массового суицида приводит к заболеванию раком.
Слайд 24 Мировая наука освятила апоптоз отдельной клетки. За открытие
генов, задача которых - кодировать белки, провоцирующие самоубийство клеток
в 2002 году была присуждена Нобелевская премия по физиологии. Когда возникает подозрение, что что-то не так, поступает приказ “уйти из жизни”, он передается через цепочку белков, последний сообщает клетке приказ исполнить, и она начинает распадаться.
Слайд 25
Польза и вред апоптоза.
Если апоптоз выходит из-под контроля,
то гибель клеток становится патологической. Усиленный, неконтролируемый апоптоз вызывает
массированную гибель клеток.Одна клетка, решая покончить с собой, может посылать смертоносный сигнал своим соседям, в результате погибает не она одна, а целый клеточной пласт.
Слайд 26
Апоптоз и клеточное старение.
Группа канадских биологов нейтрализовала два
гена отвечающих за апоптоз у червей, в организме которых
всего тысяча клеток. Эти черви стали жить в шесть раз дольше. Строение человека гораздо сложнее, апоптоз выполняет необходимую организму функцию, удаляет поврежденные клетки и клетки с нарушенной функцией, поэтому если просто отключить апоптоз, это сократит жизнь человека.Хотя апоптоз, безусловно, полезен для молодого организма, он может приводить к неблагоприятным для здоровья явлениям в более позднем возрасте, способствуя старению организма.
Слайд 27 Некоторые старые клетки, утратившие способность к делению, становятся
резистентными (не чувствительными) к апоптозу, такие старые клетки накапливаются,
достигается некий пороговый уровень, когда утрачивается прежнее здоровье тканей.Очевидно что, многие аспекты рассмотренной проблемы требуют своего уточнения, что, безусловно, необходимо для выработки рациональной стратегии вмешательства в процесс.
Слайд 28
Гипотеза о самоубийстве организма.
Академиком Скулачевым В.П. выдвинуто любопытное
предположение, о существовании некой генетической программы самоуничтожения, которая постепенно
и разрушает организм.Уже доказано, что по крайней мере для некоторых живых существ, смерть есть результат включения программы самоубийства, очень схожей с апоптозом по принципу реализации.