- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по физике 10 кл Законы термодинамики
Содержание
- 2. Вопросы для повторения:Что такое внутренняя энергия?Назовите способы
- 3. Зависимость внутренней энергии от параметров газа
- 4. Способы изменения внутренней энергии
- 5. Первый закон термодинамики
- 6. Первый закон термодинамикиИзменение внутренней энергии системы при
- 7. Первый закон термодинамики
- 8. Первый закон термодинамикиКоличество теплоты, переданное системе идет на совершение системой работы и изменение её внутренней энергии
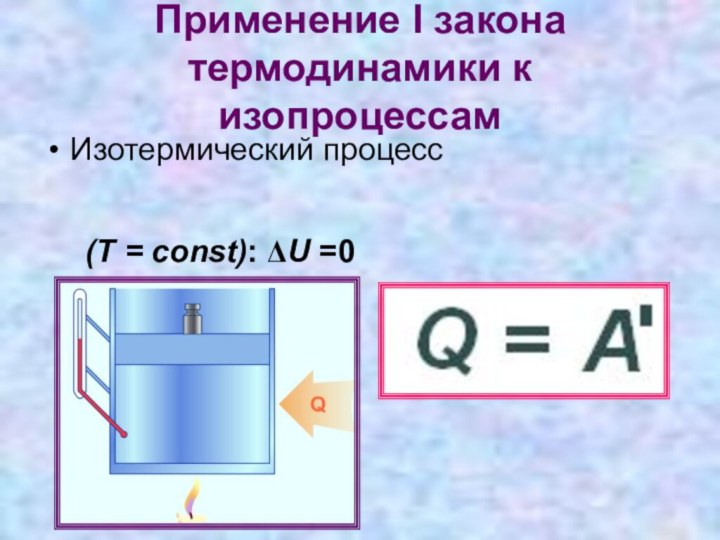
- 9. Применение I закона термодинамики к изопроцессамИзотермический процесс(T = const): ΔU =0
- 10. Применение I закона термодинамики к изопроцессамИзобарный процесс:A = pΔV = vRΔT (p = const):
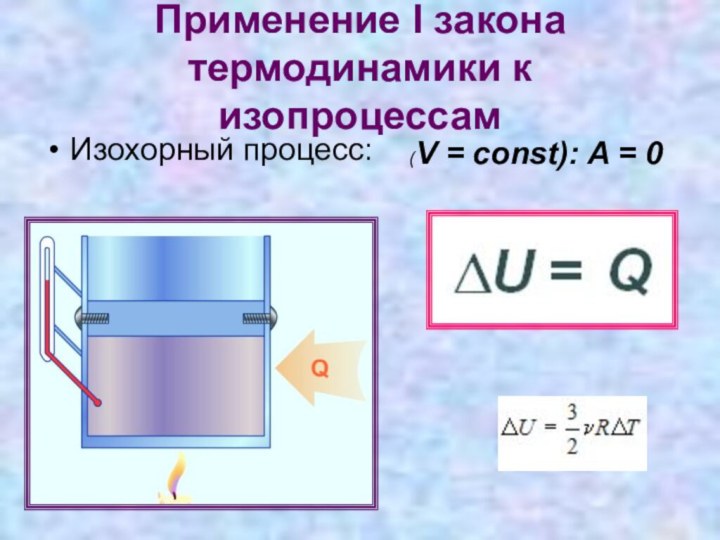
- 11. Применение I закона термодинамики к изопроцессамИзохорный процесс:(V = const): A = 0
- 12. Применение I закона термодинамики к изопроцессамАдиабатный процесс:
- 13. Адиабатный процессАдиабатными можно считать все быстропротекающие процессы
- 14. Термодинамика циклического процесса. Для произвольного циклического
- 15. Необратимость процессов в природе.Необратимые – процессы, которые
- 16. Необратимость процессов в природе.Что произойдет с колебаниями маятников с течением времени?
- 17. Необратимость процессов в природе.
- 18. Необратимость процессов в природе.
- 19. Необратимость процессов в природе.Все процессы в природе НЕОБРАТИМЫ!
- 20. II закон термодинамики.Формулировка Клаузиуса (1850): невозможен процесс,
- 21. Скачать презентацию
- 22. Похожие презентации
Вопросы для повторения:Что такое внутренняя энергия?Назовите способы изменения внутренней энергии.Как определить работу газа?Как определить количество теплоты?Объясните физический смысл удельных величин.













Слайд 2
Вопросы для повторения:
Что такое внутренняя энергия?
Назовите способы изменения
внутренней энергии.
смысл удельных величин.
Слайд 6
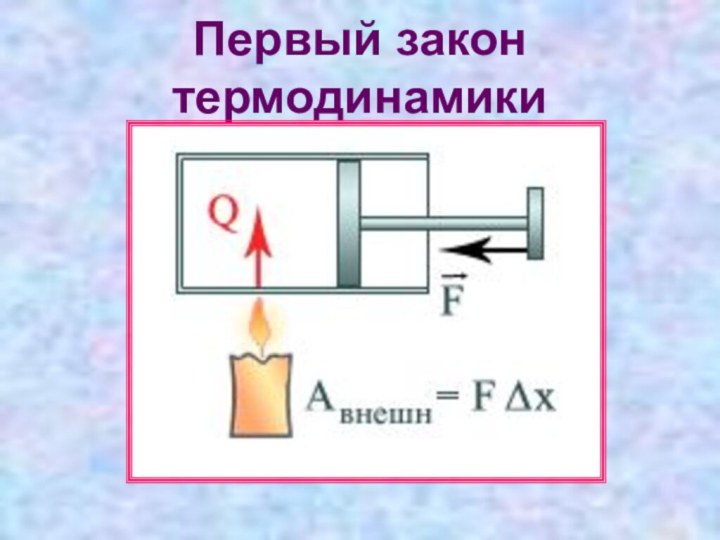
Первый закон термодинамики
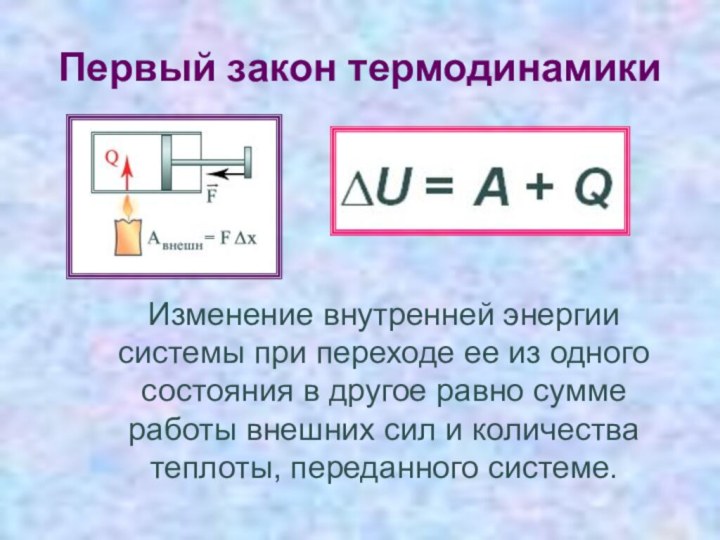
Изменение внутренней энергии системы при переходе
ее из одного состояния в другое равно сумме работы
внешних сил и количества теплоты, переданного системе.
Слайд 8
Первый закон термодинамики
Количество теплоты, переданное системе идет на
совершение системой работы и изменение её внутренней энергии
Слайд 10
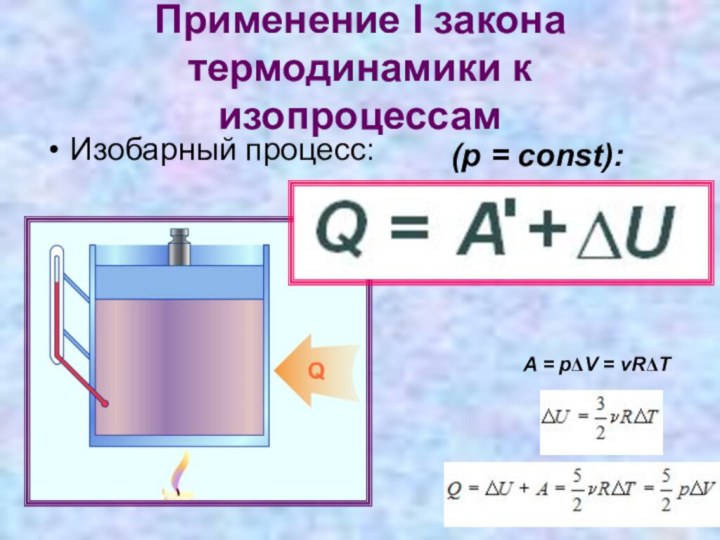
Применение I закона термодинамики к изопроцессам
Изобарный процесс:
A =
pΔV = vRΔT
(p = const):
Слайд 12
Применение I закона термодинамики к изопроцессам
Адиабатный процесс: процесс,
происходящий без теплообмена с окружающей средой.
Q=0
Температура меняется только
за счет совершения работы
Слайд 13
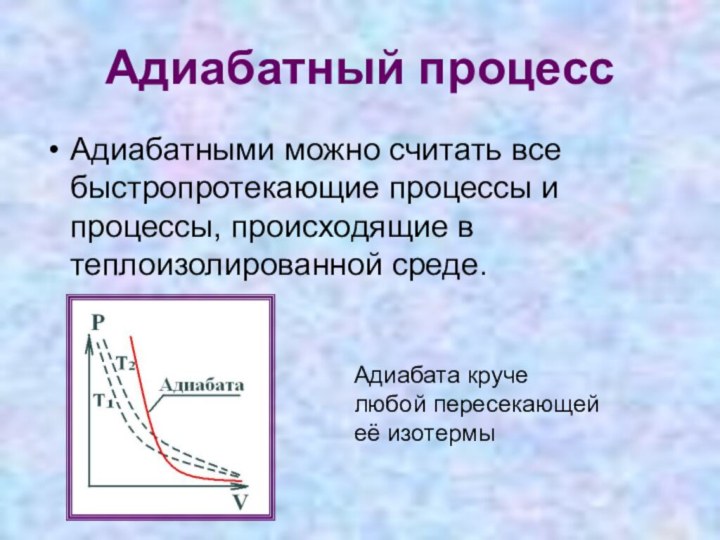
Адиабатный процесс
Адиабатными можно считать все быстропротекающие процессы и
процессы, происходящие в теплоизолированной среде.
Адиабата круче любой пересекающей её
изотермы
Слайд 14
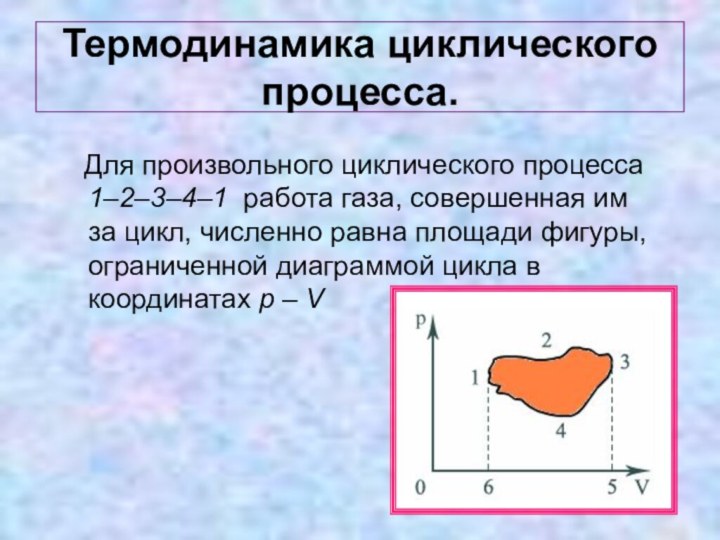
Термодинамика циклического процесса.
Для произвольного циклического процесса
1–2–3–4–1 работа газа, совершенная им за цикл, численно равна
площади фигуры, ограниченной диаграммой цикла в координатах p – V
Слайд 15
Необратимость процессов в природе.
Необратимые – процессы, которые могут
самопроизвольно протекать только в одном направлении. В обратном направлении
они могут протекать только как одно из звеньев более сложного процесса.
Слайд 16
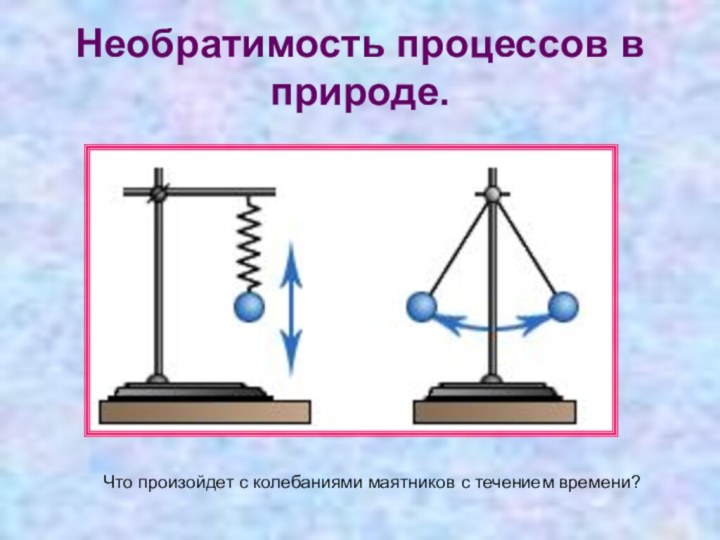
Необратимость процессов в природе.
Что произойдет с колебаниями маятников
с течением времени?
Слайд 20
II закон термодинамики.
Формулировка Клаузиуса (1850): невозможен процесс, при
котором тепло самопроизвольно переходило бы от тел менее нагретых
к телам более нагретым.Формулировка Томсона (1851): невозможен круговой процесс, единственным результатом которого было бы производство работы за счет уменьшения внутренней энергии.
Формулировка Клаузиуса (1865): все самопроизвольные процессы в замкнутой неравновесной системе происходят в таком направлении, при котором энтропия системы возрастает; в состоянии теплового равновесия она максимальна и постоянна.
Формулировка Больцмана (1877): замкнутая система многих частиц самопроизвольно переходит из более упорядоченного состояния в менее упорядоченное. Невозможен самопроизвольный выход системы из положения равновесия. Больцман ввел количественную меру беспорядка в системе, состоящей из многих тел – энтропию.