- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Физика атома, атомного ядра и элементарных частиц
Содержание
- 2. Строение атома
- 3. Модели атомовДемокрит полагал, что свойства того или иного
- 4. Ранняя планетарная модель атома Нагаоки.В 1904
- 5. Ранняя планетарная модель атома Нагаоки
- 6. Модель атома Томсона (модель «Пудинг с изюмом»). Дж.
- 7. Модель атома Томсона (модель «Пудинг с изюмом»).
- 8. Недостатки модели:не объясняла дискретный характер излучения атома
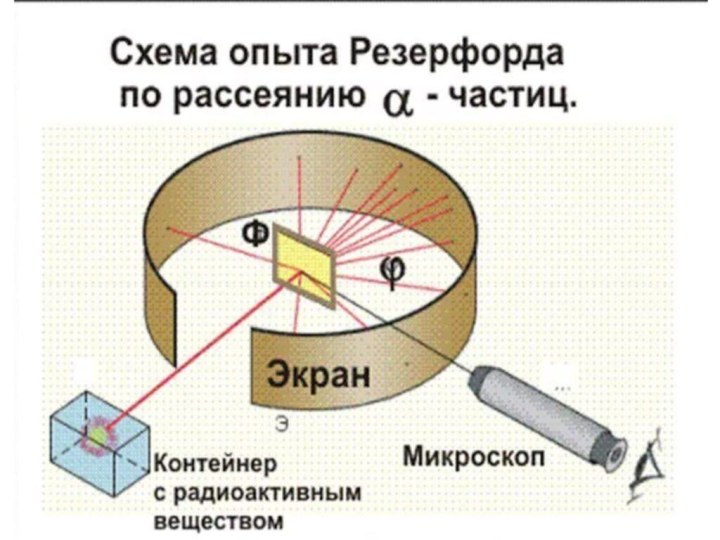
- 9. Опыты Резерфорда
- 12. Модель атома РезерфордаВесь положительный заряд атомов сосредоточен
- 13. Модель атома РезерфордаВ ядре сосредоточена практически вся
- 14. Трудности модели атома Резерфорда. Постулаты Бора
- 15. Трудности модели атома РезерфордаЭлектрон вращается вокруг ядра
- 16. Кризис в теории атома был преодолен в 1913 г. Нильсом Бором
- 17. Постулаты БораI постулат - постулат стационарных состояний:В атоме существуют
- 18. Постулаты БораII постулат - правило частот:При переходе атома из
- 21. Энергетическая схема атомных уровней.
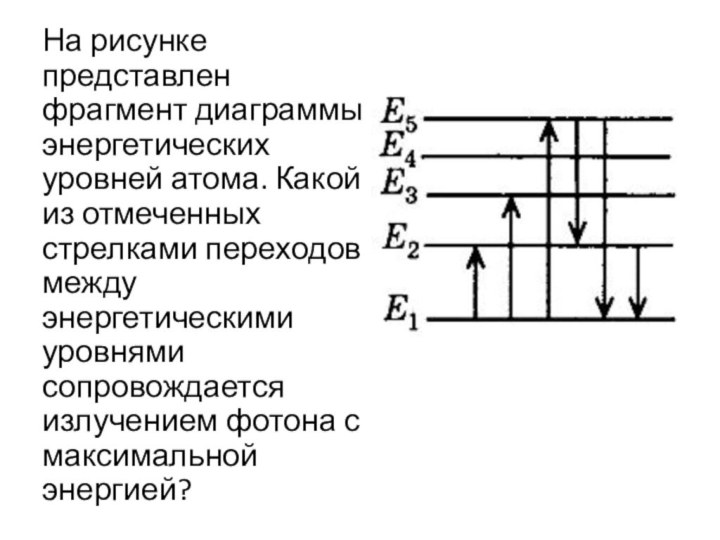
- 22. На рисунке представлен фрагмент диаграммы энергетических уровней
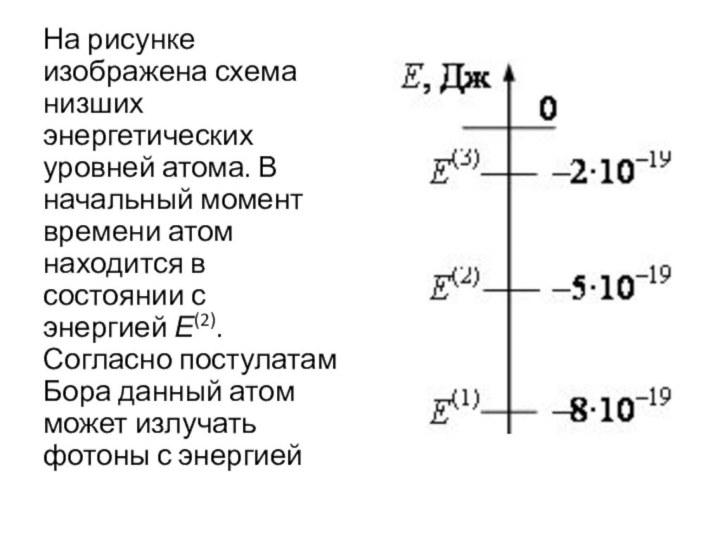
- 23. На рисунке изображена схема низших энергетических уровней
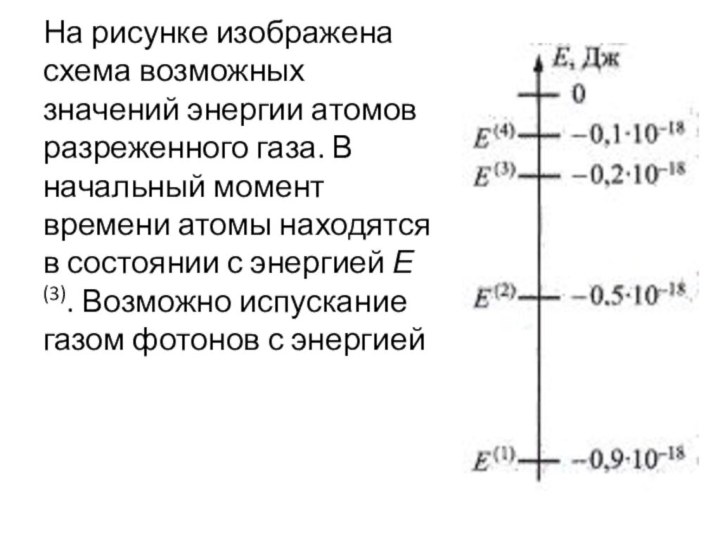
- 24. На рисунке изображена схема возможных значений энергии
- 25. Радиоактивность
- 26. Радиоактивность – явление самопроизвольного (спонтанного) превращения одних ядер в другие с испусканием различных частиц.
- 27. Явление радиоактивности обнаружил Антуан Анри Беккерель в
- 28. 1898 г французские ученые Мария Склодовская-Кюри и Пьер Кюри РадийПолонийТорий
- 29. Опыты М. Кюри привели к следующим результатам.Радиоактивность обнаруживают
- 30. Мария Склодовская-Кюри в 1903 г. вместе с
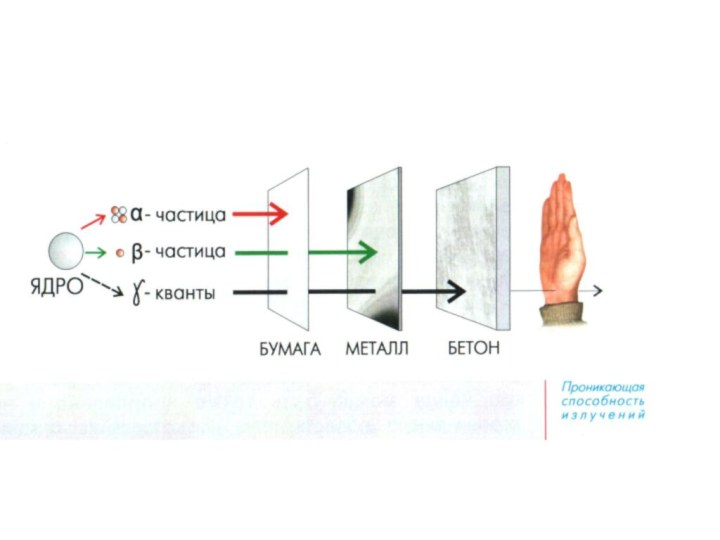
- 33. α – частица - положительно заряженная частица,
- 35. Особенности радиоактивного излученияПостоянство (на протяжении суток, месяцев,
- 36. Радиоактивные превращения атомных ядер.Правила смещения.
- 38. Альфа - распад Альфа – распад – превращение атомных ядер, сопровождаемое испусканием альфа частицы.
- 39. Альфа - распад При альфа – распаде ядро
- 40. Альфа - распад В результате альфа – распада элемент смещается на две клетки к началу периодической системы.
- 41. Альфа - распад
- 42. Бета - распад Бета – распад - превращение атомных ядер, сопровождаемое испусканием электрона.
- 43. Бета - распад При бета – распаде из
- 44. Бета - распад В результате бета – распада
- 45. Бета - распад
- 46. Гамма - излучение Гамма – излучение – не
- 47. Скачать презентацию
- 48. Похожие презентации
Строение атома




































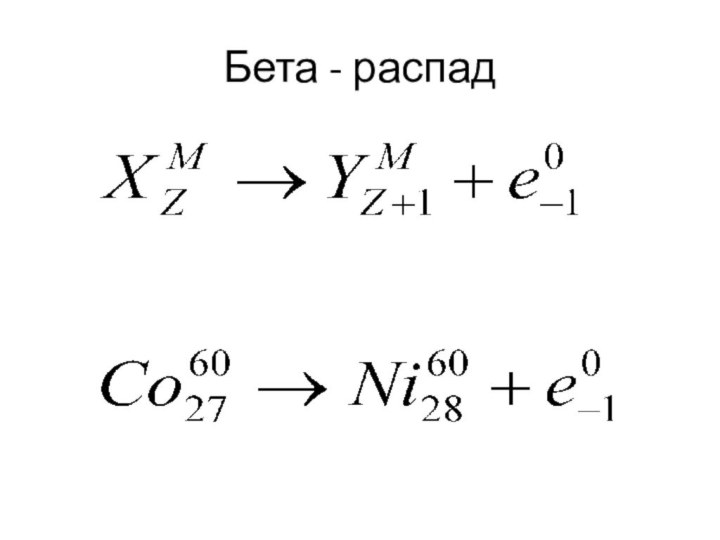


Слайд 4
Ранняя планетарная
модель атома Нагаоки.
В 1904 году японский
физик Хантаро Нагаока предложил модель атома, построенную по аналогии с планетой Сатурн.
В этой модели вокруг маленького положительного ядра по орбитам вращались электроны, объединённые в кольца. Модель оказалась ошибочной.
Слайд 6
Модель атома Томсона
(модель «Пудинг с изюмом»).
Дж. Дж. Томсон предложил
рассматривать атом как некоторое положительно заряженное тело с заключёнными
внутри него электронами. Была окончательно опровергнута Резерфордом после проведённого им знаменитого опыта по рассеиванию альфа-частиц.
Слайд 8
Недостатки модели:
не объясняла дискретный характер излучения атома и
его устойчивость;
не дает возможности понять, что определяет размеры
атомов; оказалась в полном противоречии с опытами по исследованию распределения положительного заряда в атоме
Слайд 12
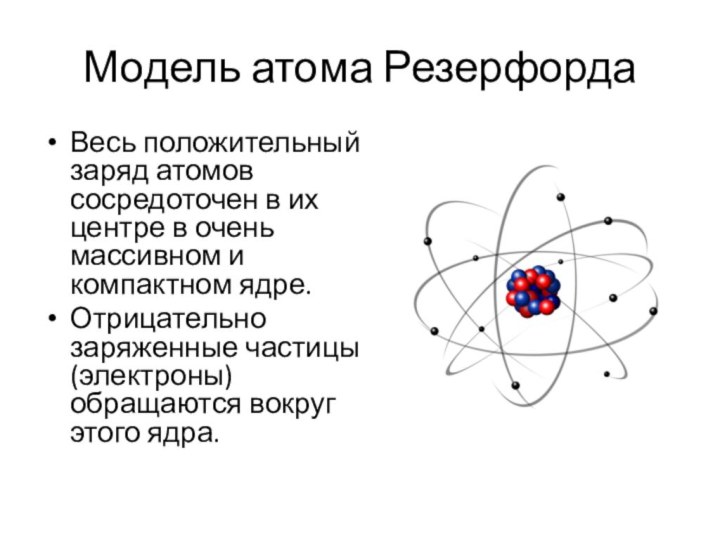
Модель атома Резерфорда
Весь положительный заряд атомов сосредоточен в
их центре в очень массивном и компактном ядре.
Отрицательно
заряженные частицы (электроны) обращаются вокруг этого ядра.
Слайд 13
Модель атома Резерфорда
В ядре сосредоточена практически вся масса
атома.
В целом атом нейтрален.
Положительный заряд ядра равен
сумме отрицательных зарядов всех электронов атома.
Слайд 15
Трудности модели атома Резерфорда
Электрон вращается вокруг ядра с
очень большим ускорением.
Ускоренно движущаяся заряженная частица излучает электромагнитные
волны с частотой, равной частоте его обращения вокруг ядра. Излучение сопровождается потерей энергии.
Теряя энергию электрон должен приближаться к ядру.
Атом прекратит свое существование.
Слайд 17
Постулаты Бора
I постулат - постулат стационарных состояний:
В атоме существуют стационарные
квантовые состояния, не изменяющиеся с течением времени без внешнего
воздействия на атом. В этих состояниях атом не излучает электромагнитных волн, хотя и движется с ускорением. Каждому стационарному состоянию атома соответствует определенная энергия атома. Стационарным состояниям соответствуют стационарные орбиты, по которым движутся электроны.
Слайд 18
Постулаты Бора
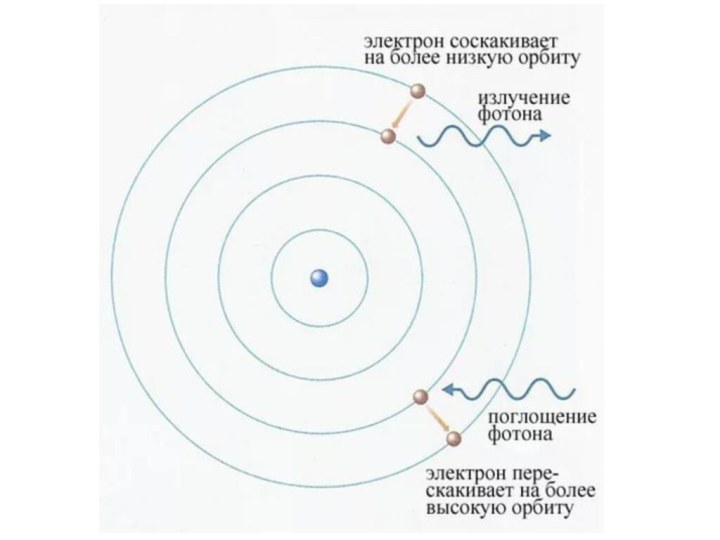
II постулат - правило частот:
При переходе атома из одного
стационарного состояния в другое излучается или поглощается 1 фотон.
а)
Атом излучает 1 фотон (который несет 1 квант энергии), когда электрон переходит из состояния с большей энергией (Е k) в состояние с меньшей энергией (Е n). б) Атом поглощает 1 фотон, когда переходит из стационарного состояния с меньшей энергией
Слайд 22 На рисунке представлен фрагмент диаграммы энергетических уровней атома.
Какой из отмеченных стрелками переходов между энергетическими уровнями сопровождается
излучением фотона с максимальной энергией?Слайд 23 На рисунке изображена схема низших энергетических уровней атома.
В начальный момент времени атом находится в состоянии с
энергией Е(2). Согласно постулатам Бора данный атом может излучать фотоны с энергиейСлайд 24 На рисунке изображена схема возможных значений энергии атомов
разреженного газа. В начальный момент времени атомы находятся в
состоянии с энергией Е(3). Возможно испускание газом фотонов с энергиейСлайд 26 Радиоактивность – явление самопроизвольного (спонтанного) превращения одних ядер
в другие с испусканием различных частиц.
Слайд 27 Явление радиоактивности обнаружил Антуан Анри Беккерель в 1896
г.
Получил за эту работу Нобелевскую премию по физике в
1903 г.
Слайд 29
Опыты М. Кюри привели к следующим результатам.
Радиоактивность обнаруживают не
только уран, но и все его химические соединения.
Радиоактивность препарата с любым
химическим составом равна радиоактивности чистых урана или тория, взятых в количестве, в котором они содержатся в этом препарате.Слайд 30 Мария Склодовская-Кюри в 1903 г. вместе с мужем
Пьером Кюри получила Нобелевскую премию по физике за исследование
радиоактивного излучения.В 1911 г. получила Нобелевскую премию по химии за выделение радия.
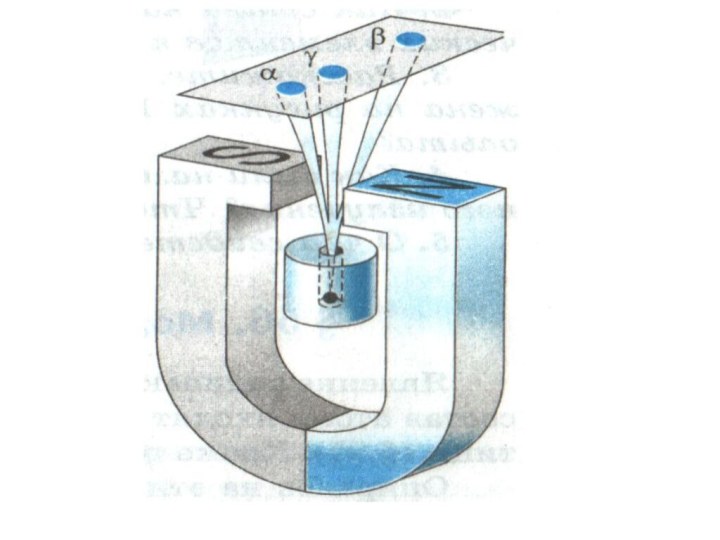
Слайд 33 α – частица - положительно заряженная частица, ядро
атома гелия;
β – частица - отрицательно заряженная частица, электрон;
γ
– излучение– электромагнитное излучение, распространяющееся со скоростью света.
Слайд 35
Особенности радиоактивного излучения
Постоянство (на протяжении суток, месяцев, лет
интенсивность излучения не меняется);
Радиоактивность сопровождается выделением энергии, которая выделяется
непрерывно на протяжении длительного периода времени На радиоактивность не оказывает влияние перепады температуры, давления, различные химические реакции в которые вступает радиоактивный элемент