- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Физико-химические методы анализа
Содержание
- 2. ПланКлассификация физических и физико-химических методов анализаКлассификация оптических методов анализаЗаконы светооглощенияРефрактометрияЭлектрохимияПотенциометрияХроматография
- 3. Классификация физических и физико-химических методов анализа:Оптические методы.Хроматографические методы.Электрохимические методы.Радиометрические методы.Термические методы.Масс-спектрометрические.
- 4. Классификация оптических методов анализа:По изучаемым объектам: атомный
- 5. По области электромагнитного спектра. Спектроскопия (спектрофотометрия) в
- 6. Общие положенияДлина волны λ - расстояние, проходимое
- 7. Закон Бугера-Ламберта (в 1729 г. - Бугер,
- 8. Закон Бера (1852 г.): оптическая плотность
- 9. Объединенный закон Бугера-Ламберта-Бера: оптическая плотность прямопропорциональна концентрации
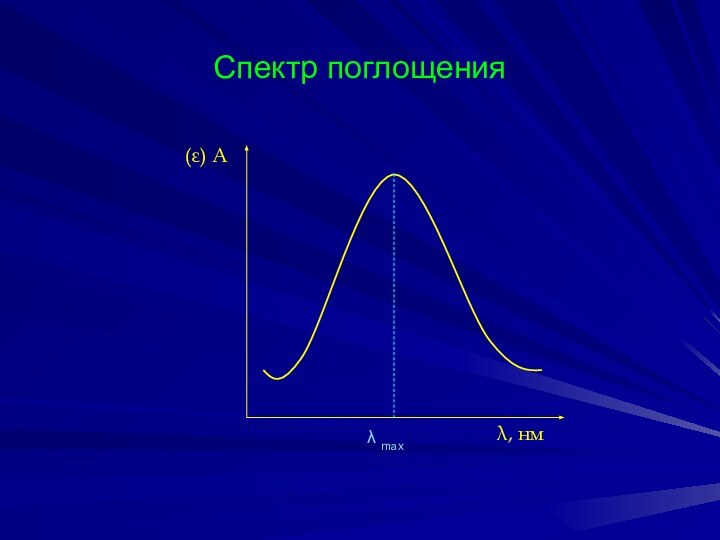
- 10. Спектр поглощения(ε) Аλ, нмλ max
- 11. РЕФРАКТОМЕТРИЯ
- 12. При переходе света из оптически менее плотной
- 13. Закон преломления Снеллиуса:отношение синусов углов падения sin
- 14. Электрохимические методы анализа. Классификация методов. Потенциометрический анализ. Хроматографические методы анализа. Ионообменная хроматография.
- 15. Электрохимические методы анализа основаны на измерении электрохимичеких параметров электрохимических явлений, возникающих в исследуемом растворе.
- 16. Классификация электрохимических методов анализа Классификация, основанная
- 17. Потенциометрия Потенциометрический анализ (потенциометрия) – основан
- 18. Хроматография динамический сорбционный способ разделения смесей,
- 19. Отличительной особенностью хроматографических методов является их
- 20. Хроматография позволяет одновременно производить идентификацию и количественное определение разделяемых компонентов смеси.
- 21. Ионообменная хроматография Основана на обратимом обмене содержащихся
- 22. Применение ионообменной хроматографииразделения электролитовочистки от примесей извлечения
- 23. ЛитератураЮ.А. Харитонов Аналитическая химия. Книга 2 Количественный
- 24. Скачать презентацию
- 25. Похожие презентации
ПланКлассификация физических и физико-химических методов анализаКлассификация оптических методов анализаЗаконы светооглощенияРефрактометрияЭлектрохимияПотенциометрияХроматография






















Слайд 2
План
Классификация физических и физико-химических методов анализа
Классификация оптических методов
анализа
Слайд 3
Классификация физических и физико-химических методов анализа:
Оптические методы.
Хроматографические методы.
Электрохимические
методы.
Радиометрические методы.
Термические методы.
Масс-спектрометрические.
Слайд 4
Классификация оптических методов анализа:
По изучаемым объектам: атомный и
молекулярный спектральный анализ.
По характеру взаимодействия электромагнитного излучения с веществом.
Различают:Атомно-абсорбционный анализ.
Эмиссионный спектральный анализ.
Пламенная фотометрия.
Молекулярный абсорбционный анализ.
Люминесцентный анализ.
Спектральный анализ с использованием эффекта комбинационного рассеяния света (раман-эффекта).
Нефелометрический анализ.
Турбидиметрический анализ.
Рефрактометрический анализ.
Интерферометрический анализ.
Поляриметрический анализ.
Слайд 5
По области электромагнитного спектра.
Спектроскопия (спектрофотометрия) в УВИ
области спектра, т.е. в ближней ультрафиолетовой (УФ) области –
в интервале длин волн 200-400 нм (185-390 нм) и в видимой области – в интервале длин волн 400-760 нм (390-760 нм).Инфракрасная спектроскопия, изучающая участок спектра в интервале 0,76-1000 мкм (1 мкм = 10-6 м).
Реже используются: рентгеновская спектроскопия, микроволновая спектроскопия и др.
По природе энергетических переходов.
Электронные спектры.
Колебательные спектры.
Вращательные спектры.
Слайд 6
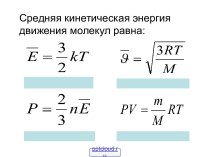
Общие положения
Длина волны λ - расстояние, проходимое волной
за время одного полного колебания. Чаще измеряют в нм
(1 нм = 10-9 м).Частота ν - число раз в секунду, когда электрическое поле достигает своего максимального положительного значения. Единица измерения - герц (1 Гц = 1 с-1).
Волновое число - число длин волн, укладывающихся в единицу длины, = 1/λ. Измеряют волновое число в обратных сантиметрах (см-1).
Уравнение Планка:
где - изменение энергии элементарной системы в результате поглощения или испускания фотона с энергией
(h – постоянная Планка: h=6,6262·10-34 Дж·с).
Слайд 7 Закон Бугера-Ламберта (в 1729 г. - Бугер, в
1760 г. - Ламберт): однородные слои одного и того
же вещества одинаковой толщины поглощают одну и ту же долю падающей на них световой энергии при постоянной концентрации растворенного вещества.е - основание натуральных логарифмов;
k1 - коэффициент поглощения среды;
l - толщина поглощающего слоя, см.
Слайд 8
Закон Бера (1852 г.): оптическая плотность раствора
прямопропорциональна концентрации растворенного вещества при постоянной толщине слоя
,
где k2 - коэффициент пропорциональности;
С - концентрация растворенного вещества.
Слайд 9
Объединенный закон Бугера-Ламберта-Бера:
оптическая плотность прямопропорциональна концентрации растворенного
вещества и толщине поглощающего слоя раствора.
k - коэффициент светопоглощения,
зависящий от природы растворенного вещества, температуры, растворителя и длины волны света
Слайд 12 При переходе света из оптически менее плотной среды
(I) в среду с оптически большей плотностью (2) угол
падения света α всегда больше угла преломления β.α
β
1
2
Слайд 13
Закон преломления Снеллиуса:
отношение синусов углов падения sin α
и преломления sin β – есть величина постоянная для
каждого вещества, ее называют показателем преломления n:
Слайд 14 Электрохимические методы анализа. Классификация методов. Потенциометрический анализ. Хроматографические
методы анализа. Ионообменная хроматография.
Слайд 15 Электрохимические методы анализа основаны на измерении электрохимичеких параметров
электрохимических явлений, возникающих в исследуемом растворе.
Слайд 16
Классификация электрохимических методов анализа
Классификация, основанная на учете природы
источника электрической энергии в системе.
Методы без наложения внешнего
(постороннего) потенциала. Методы с наложением внешнего (постороннего) потенциала.
Слайд 17
Потенциометрия
Потенциометрический анализ (потенциометрия)
– основан на использовании зависимости
разности электродных потенциалов от концентрации (активности) определяемого вещества в
растворе.Такая зависимость описывается уравнением Нернста:
Ер = Е0 + 0,059/n·lgа
Слайд 18
Хроматография
динамический сорбционный способ разделения смесей, основанный на распределении
вещества между двумя фазами, одна из которых подвижная, а
другая — неподвижная, и связанный с многократным повторением сорбционных и десорбционных актов.Слайд 19 Отличительной особенностью хроматографических методов является их универсальность, то
есть возможность использования:
— для очистки веществ;
— концентрирования веществ из
сильно разбавленных растворов;— разделения сложных смесей органических и неорганических веществ;
— идентификации веществ;
— определения количественного состава.
Слайд 20
Хроматография позволяет одновременно производить идентификацию и количественное определение
разделяемых компонентов смеси.
Слайд 21
Ионообменная хроматография
Основана на обратимом обмене содержащихся в растворе
ионов на ионы, входящие в состав сорбента (ионообменника).
Слайд 22
Применение ионообменной хроматографии
разделения электролитов
очистки от примесей
извлечения и
концентрирования
получения кислот, оснований, солей
выделения редкоземельных металлов
определения
воды количественного определения веществ