- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Рак поджелудочной железы (значение проблемы, возможности лечения)
Содержание
- 2. 1.ВведениеКраткие сведение о поджелудочной железе2.Основная частьСпособствующие факторыОписание болезниКлиническая картинаДиагностикаСимптомыЛечениеПрофилактика3.Ввод
- 3. Общие сведения об анатомии поджелудочной железы и
- 4. Общие сведения об анатомии поджелудочной железы и
- 5. Общие сведения об анатомии поджелудочной железы и
- 6. Поджелудочная железа и двенадцатиперстная кишка 1
- 8. Поджелудочная железа, pancreas — крупная железа, расположенная
- 9. Описание болезни Рак поджелудочной
- 10. Рак поджелудочной железы (РПЖ) является грозным онкологическим
- 11. Статистика РПЖ Среди опухолей желудочно-кишечного тракта
- 12. Рак поджелудочной железы чаще встречается в развитых странах,
- 13. Эпидемиология РПЖ Точные причины
- 14. Эпидемиология РПЖ Считается, что
- 15. Эпидемиология РПЖ Значение алкоголя в
- 16. Этиология Заболеваемость раком поджелудочной железы ежегодно увеличивается.
- 17. К предраковым заболеваниям относятся:Аденома поджелудочной железыХронический панкреатитКиста
- 18. Предрасполагающие болезни и состояния Диабет: была показана
- 19. Патология рака поджелудочной железы Протоковая аденокарцинома, самая
- 20. Стадирование рака поджелудочной железы
- 21. Стадирование рака поджелудочной железы Т2 -
- 22. Симптомы рака поджелудочной железы
- 23. Симптомы рака поджелудочной железы
- 24. Симптомы рака поджелудочной железы
- 25. Симптомы рака поджелудочной железы
- 26. Маркеры рака поджелудочной железы
- 27. Маркеры рака поджелудочной железы У
- 28. Гистологическая классификация Гистологическая классификация приводится согласно
- 29. Клиника рака головки поджелудочной железы Желтушный период
- 34. Диагностические мероприятия (алгоритм):Общий анализ крови, мочи; Биохимический
- 35. Диагностические мероприятия (алгоритм):КТ органов брюшной полости, забрюшинного
- 36. Прежде чем начинать лечение рака поджелудочной железы, необходимо
- 37. КТ-диагностика рака поджелудочной железы: современное состояние проблемыПроблема
- 39. 3-ий Международный семинар по многосрезовой компьютерной томографии (МСКТ), 3D визуализации, виртуальной эндоскопии6-8 июня 2002, Рим
- 40. 2D или 3D?От MIP к объемному рендеренгу
- 41. 3D - объемный рендеринг (VR)Введение в объемный
- 42. Стратегии контрастного усиления при МСКТОбъемная МСКТ: общие
- 43. Стратегии контрастного усиления при МСКТОбъемная МСКТ: принципы
- 44. Стратегии контрастного усиления при МСКТЭффективное использование КВ
- 45. МСКТ с криволинейными мультипланарными реконструкциями при опухолях
- 46. Одно из наиболее ценных преимуществМДКТ
- 47. Трехмерное моделирование на
- 48. Наиболее часто используемые методыпостпроцессорной обработки данных: проекция
- 49. При ракепанкреатобилиарной области парапанкреатические лим-фатические сосуды поражаются
- 50. Проведение МДКТ-ангиографии ПЖ стало неотъем-лемой частью подготовки
- 51. Общие принципы лечения
- 52. Хирургическое лечение рака поджелудочной железы
- 54. Хирургическое лечение рака поджелудочной железы
- 55. Хирургическое лечение рака поджелудочной железы
- 56. Хирургическое лечение рака поджелудочной железы
- 57. Хирургическое лечение рака поджелудочной железы
- 58. Хирургическое лечение рака поджелудочной железы
- 59. Хирургическое лечение нерезектабельного рака поджелудочной железы
- 61. Паллиативные операции при раке ПЖ
- 62. 1. Билиарная декомпрессия при механической желтухе.1.1. Показания:как
- 63. 2. Интраоперационные методы декомпрессии желчных протоков.2.1. Применяемые
- 64. 2.3. Анастомозы с общим желчным протоком –
- 65. Выполнение холецистогастро- и холецистодуоденоанастамоза допустимы лишь в
- 66. Этот тип оперативного вмешательства крайне неблагоприятен у
- 67. Химиотерапия 1. Кальция фолинат 20 мг/м2 в
- 68. 4. FOLFIRINOX:оксалиплатин 85 мг/м2 в вену
- 69. Химиолучевая терапия1. Химиотерапия:флуороурацил 500 мг/м2 внутривенно струйно
- 70. Ложе опухоли и края резекции определяются по
- 71. 2/3 одной почки),
- 72. Главная цель современной лучевой терапии - направленное
- 74. модуляция интенсивности полей излучения (технология RapidArc)модифицированная по
- 75. Индивидуальная программа лучевого лечения рака поджелудочной железы
- 76. Для воздействия на экзокринные опухоли поджелудочной железы
- 77. Лучевая терапия рака поджелудочной железы чаще всего
- 78. К сожалению, только 15-20% больных раком поджелудочной
- 79. Комбинированное применение лучевой терапии одновременно или поочередно
- 80. В некоторых случаях, у пациентов с метастазирующей
- 81. Как действует лучевая терапия (радиотерапия) Высокоэнергетическое рентгеновское
- 82. Во время предварительного планирования лучевого лечения, специалисты-радиологи
- 83. Самым распространенным видом лучевого воздействия на злокачественные
- 84. При раке поджелудочной железы используются также новейшие
- 85. Технология RapidArc основана на использовании высокоточных линейных
- 86. Побочные эффекты лучевой терапии Перед началом лучевой
- 87. Побочные эффекты радиотерапии можно разделить на две
- 88. Острые последствия лучевого лечения возникают уже через
- 89. Варианты лучевого лечения рака поджелудочной железы Для
- 90. Методы лечения рака: лучевая терапия (радиотерапия) Новейшие
- 91. Лучевая терапия при Cr поджелудочной железы по
- 92. Абсолютные противопоказания к ЛТвыраженная диарея язвенная болезнь
- 93. Предоперационное облучение применяется в настоящее время редко.
- 94. Интраоперационное облучение как самостоятельный метод также не
- 95. Эффективность внутритканевой лучевой терапии опухолей панкреас невелика,
- 96. При этом в зону лучевого воздействия на
- 97. Одним из направлений улучшения результатов при неоперабельном
- 98. При нерезектабельных опухолях оценивалось введение химиопрепаратов одновременно с облучением
- 99. При монотерапии используют:5Fu в различных режимах 500
- 100. Возможно проведение комбинированной химиотерапии:
- 101. При проведении комбинированной химиотерапии по сравнению с
- 102. Лечение по стадиям1. Стадия IА–В: хирургическое лечение;адъювантная
- 103. 3. Стадия IV:химиотерапия;паллиативные хирургические вмешательства;симптоматическая терапия.4. Рецидив рака ПЖ:химиотерапия;паллиативные хирургические вмешательства;химиолучевая терапия.
- 104. Наблюдение, сроки и объем обследования1. Режим наблюдения:первый
- 105. Метастазирование.Метастазирование при раке поджелудочной железы происходит лимфогенным, гематогенным
- 106. Метастазирует рак поджелудочной железы рано,
- 107. Лимфогенное метастазирование происходит в несколько этапов, на каждом
- 108. Профилактика рака поджелудочной железы: необходимо отказаться от
- 109. Прогноз. При опухолях панкреато-дуоденальной зоны прогноз серьезный, ибо
- 110. ЗаключениеРак поджелудочной железы - трагичная глава клинической
- 111. Заключение Возможно улучшение отдалённых результатов радикальных
- 112. Скачать презентацию
- 113. Похожие презентации
1.ВведениеКраткие сведение о поджелудочной железе2.Основная частьСпособствующие факторыОписание болезниКлиническая картинаДиагностикаСимптомыЛечениеПрофилактика3.Ввод
































































































Слайд 2
1.Введение
Краткие сведение о поджелудочной железе
2.Основная часть
Способствующие факторы
Описание болезни
Клиническая
картина
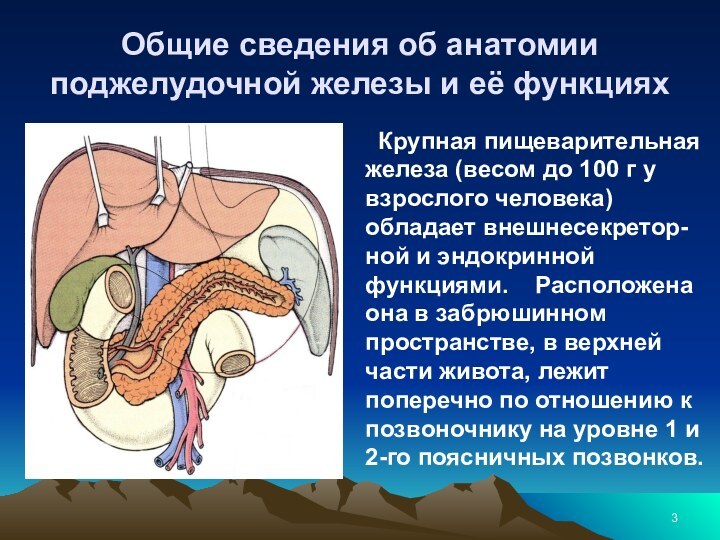
Слайд 3 Общие сведения об анатомии поджелудочной железы и её
функциях
Крупная пищеварительная железа (весом до 100
г у взрослого человека) обладает внешнесекретор-ной и эндокринной функциями. Расположена она в забрюшинном пространстве, в верхней части живота, лежит поперечно по отношению к позвоночнику на уровне 1 и 2-го поясничных позвонков. Слайд 4 Общие сведения об анатомии поджелудочной железы и её
функциях
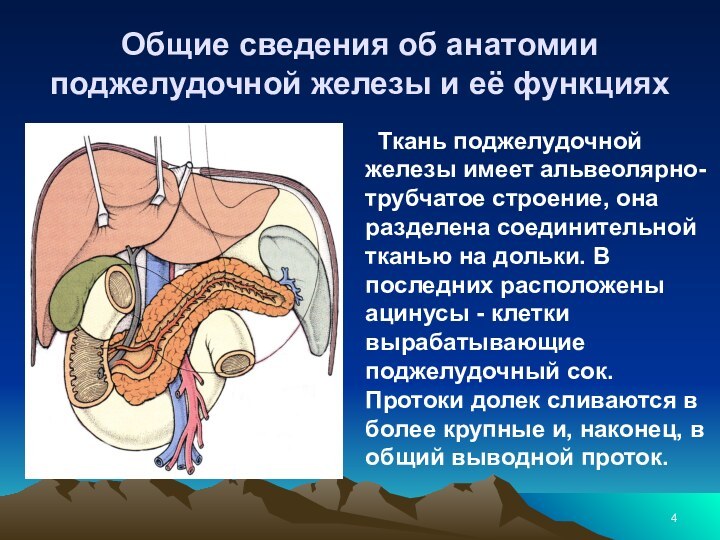
Ткань поджелудочной железы имеет альвеолярно-трубчатое строение,
она разделена соединительной тканью на дольки. В последних расположены ацинусы - клетки вырабатывающие поджелудочный сок. Протоки долек сливаются в более крупные и, наконец, в общий выводной проток. Слайд 5 Общие сведения об анатомии поджелудочной железы и её
функциях
Эндокринная часть расположена в виде
небольших скоплений инсулоцитов, не имеющих протоков в толще долек. (Островки Лангерганса). Клетки островков Лангерганса вырабатывают инсулин, глюкагон и другие гормоны, непосредственно поступающие в кровь. В поджелудочном соке (его выделяется до 2 литров в сутки) содержится 3 группы ферментов - амилазы - переваривающие углеводы, протеазы - расщепляющие белки и липазы - разрушающие жиры.
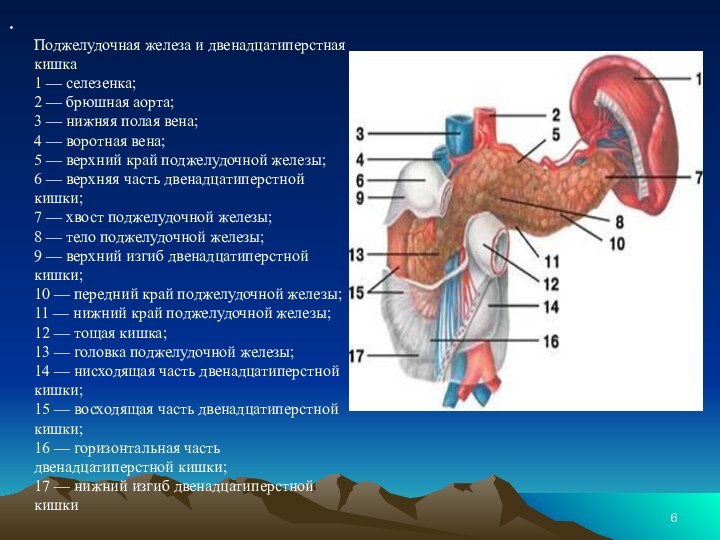
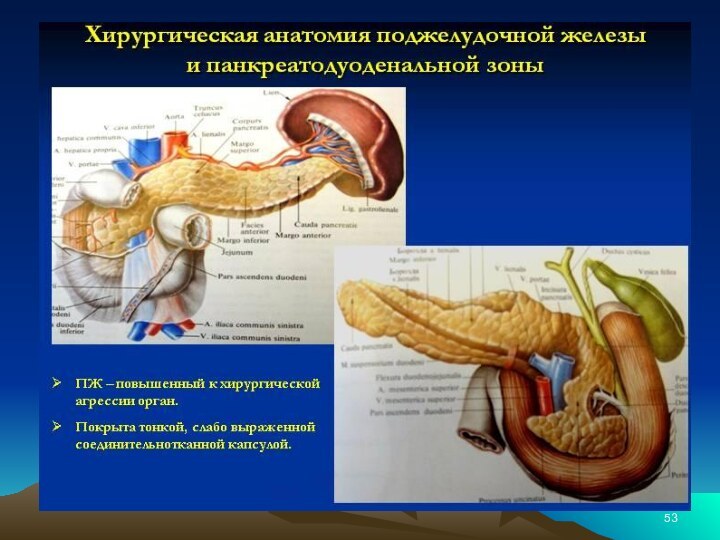
Слайд 6 Поджелудочная железа и двенадцатиперстная кишка 1 — селезенка; 2 —
брюшная аорта; 3 — нижняя полая вена; 4 — воротная вена; 5
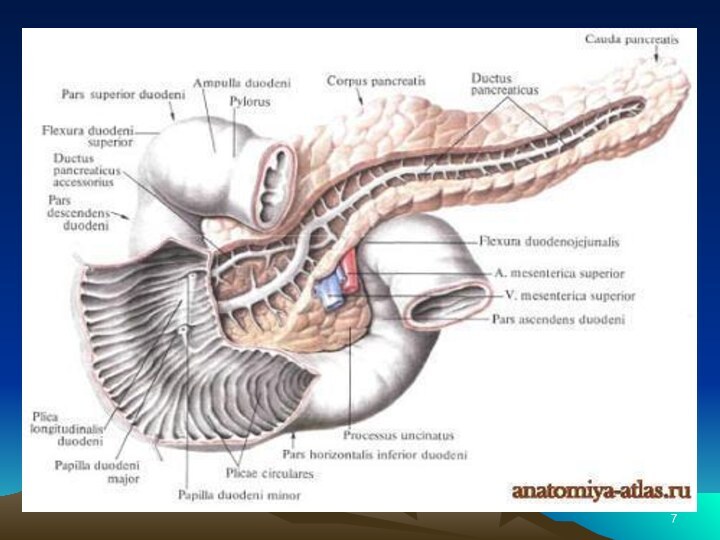
— верхний край поджелудочной железы; 6 — верхняя часть двенадцатиперстной кишки; 7 — хвост поджелудочной железы; 8 — тело поджелудочной железы; 9 — верхний изгиб двенадцатиперстной кишки; 10 — передний край поджелудочной железы; 11 — нижний край поджелудочной железы; 12 — тощая кишка; 13 — головка поджелудочной железы; 14 — нисходящая часть двенадцатиперстной кишки; 15 — восходящая часть двенадцатиперстной кишки; 16 — горизонтальная часть двенадцатиперстной кишки; 17 — нижний изгиб двенадцатиперстной кишкиСлайд 8 Поджелудочная железа, pancreas — крупная железа, расположенная на
задней стенке живота позади желудка, на уровне нижних грудных
(XI-XII) и верхних поясничных (I, II) позвонков. Основная масса железы выполняет внешнесекреторную функцию — это экзокринная часть поджелудочной железы, pars exocrina pancreatis; выделяемый ею секрет через выводные протоки поступает в двенадцатиперстную кишку.
Слайд 9
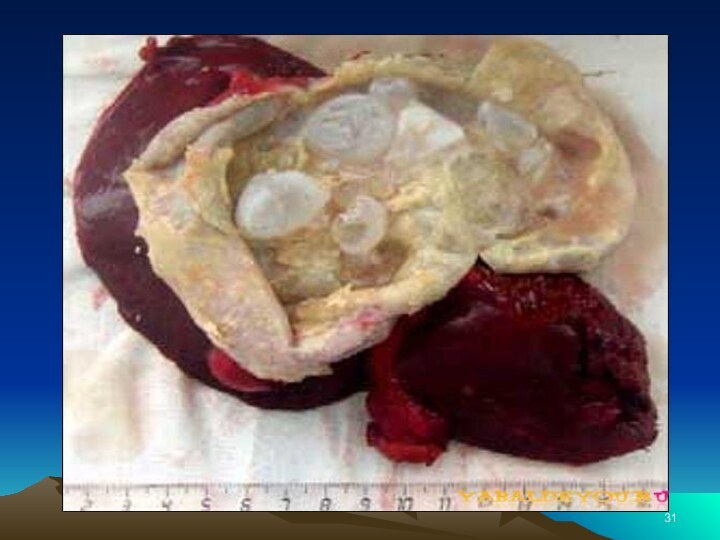
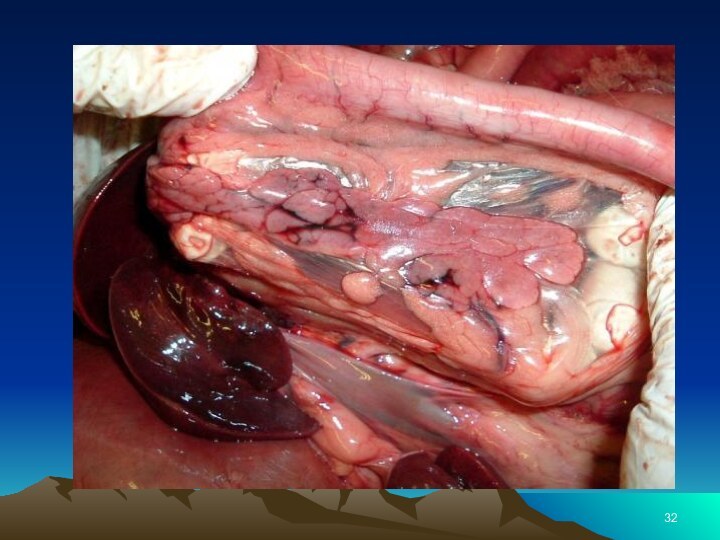
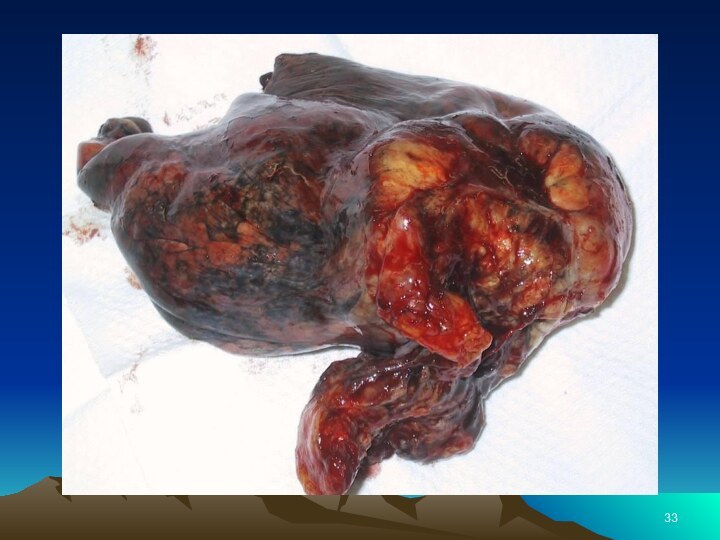
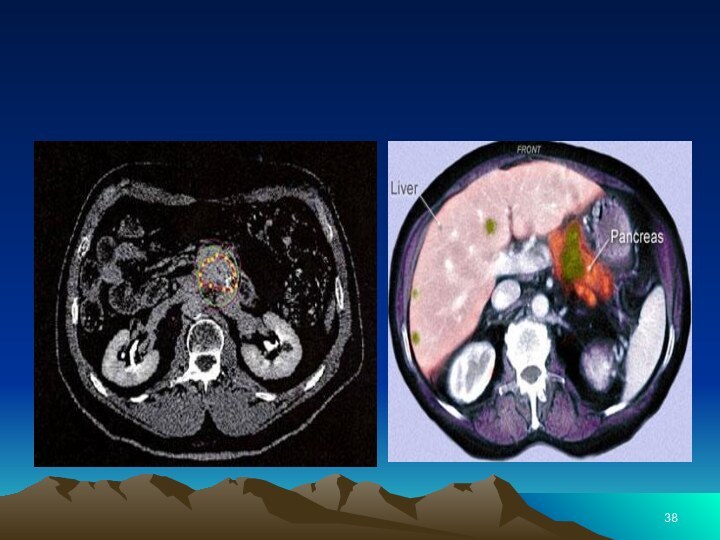
Описание болезни
Рак поджелудочной железы — злокачественное
новообразование — злокачественное новообразование, исходящее из эпителия — злокачественное новообразование, исходящее из эпителия железистой ткани или
протоковподжелудочной железы. Рак поджелудочной железы занимает четвертое место среди злокачественных новообразований желудочно-кишечного тракта (после рака желудка, рака толстой кишки и рака пищевода) и составляет 2–3% от всех раковых опухолей. Значительно чаще наблюдается у мужчин, главным образом в возрасте старше 50 лет.Слайд 10 Рак поджелудочной железы (РПЖ) является грозным онкологическим заболеванием.
На момент установления диагноза 55-75% больных РПЖ имеют нерезектабельные
опухоли. Пятилетняя выживаемость составляет 0,4 - 3,0% и наблюдается только у пациентов, диаметр опухоли у которых не превышает 2 см. Средняя продолжительность жизни радикально оперированных больных находится в пределах от 6 до 30 мес. Прогрессирование заболевания, как правило, сопровождается нарастанием боли и при локализации опухоли в головке поджелудочной железы (ПЖ) - дуоденальной и желчной обструкцией.
Слайд 11
Статистика РПЖ
Среди опухолей желудочно-кишечного тракта
РПЖ на 5-ом месте по заболеваемости и смертности. Соотношение
мужчин к женщинам, заболевшим РПЖ 1,3:1.Рак поджелудочной железы наиболее распространен в экономически развитых странах и, наоборот, реже встречается в африканских странах, Индии, Вьетнаме, Южной Америке. Возможно, что разница в заболеваемости не истинная и обусловлена трудностями распознавания.
Слайд 12 Рак поджелудочной железы чаще встречается в развитых странах, в которых
на его долю приходится около 3% от общего числа злокачественных опухолей.
Больших различий в уровне заболеваемости между отдельными странами не установлено, что говорит об отсутствии регионарных особенностей внешней среды, которые оказывали бы существенное влияние на возникновение опухоли. Наиболее высокий уровень заболеваемости отмечен в некоторых штатах США, Канаде. Израиле, Японии, однако он не более чем в 1,5–2 раза превышает забо-леваемость в большинстве европейских стран.
Слайд 13
Эпидемиология РПЖ
Точные причины возникновения
рака поджелудочной железы неизвестны. Однако, накопилось достаточно данных, свидетельствующих
о роли тех или иных средовых влияний, способствующих появлению этого заболевания.Наиболее доказательны материалы по значению курения. Риск у выкуривающих одну пачку сигарет в день в 4 раза выше, чем у не курящих. Прекращение курения не снижает риск РПЖ до уровня тех, кто никогда не курил. При курении более 40 сигарет в день риск развития РПЖ повышается в 10 раз.
Слайд 14
Эпидемиология РПЖ
Считается, что основную
ответственность несут нитрозоамины, содержащиеся в табаке, которые попадают в
панкреас, реагируют с ДНК и активируют специфические онкогены ( К-ras).Показана прямая зависимость между смертностью от рака поджелудочной железы и уровнем потребления мясных продуктов.
Наоборот, имеются данные о защитном эффекте в отношении РПЖ фруктово-овощной диеты.
Слайд 15
Эпидемиология РПЖ
Значение алкоголя в
возникновении РПЖ не доказано .
Среди адвентистов седьмого дня - религиозной секты, не употребляющей алкогольные напитки, заболеваемость РПЖ не отличается от стандартов основного населения США. В некоторых исследованиях утверждается защитная роль столового вина. Якобы, у регулярно его пьющих РПЖ развивается статистически достоверно реже. В механизме защиты значение придается фланоидам, содержащимся в виноградном вине и обладающими антиоксидантным эффектом. В споре о роли алкоголя в происхождении РПЖ есть компромиссные суждения. Они сводятся к ответственности алкоголя за развитие хронического панкреатита. Это заболевание является фоновым, предрасполагающем к возникновению рака (о чем позднее).
Крайне противоречивы сведения о роли потребления кофе.
Слайд 16
Этиология
Заболеваемость раком поджелудочной железы ежегодно увеличивается. Эта
болезнь занимает шестое место по распространённости среди онкологических заболеваний среди взрослого
населения. Поражает преимущественно людей пожилого возраста, одинаково часто мужчин и женщин[1].Факторами риска рака поджелудочной железы являются:
употребление спиртных напитков
курение
обилие жирной и острой пищи
сахарный диабет
цирроз печени
Слайд 17
К предраковым заболеваниям относятся:
Аденома поджелудочной железы
Хронический панкреатит
Киста поджелудочной
железы
Обычно опухоль поражает головку железы (50-60 % случаев), тело (10 %),
хвост (5-8 % случаев). Также наблюдается полное поражение поджелудочной железы — 20-35 % случаев. Опухоль представляет собой плотный бугристый узел без чётких границ, на разрезе — белый или светло-жёлтый.
Слайд 18
Предрасполагающие болезни и состояния
Диабет: была показана связь
между двумя болезнями, лишь при диабете, имевшем короткую историю
(несколько месяцев), вероятнее рак поджелудочной железы приводит к вторичному диабету.Хронический панкреатит, особенно застарелый, повышает риск развития РПЖ в 2 раза чаще по сравнению с контрольной когортой. В одном международном исследовании оказалось, что среди 2015 пациентов с хроническим панкреатитом (анамнез в среднем 7,5 лет) рак поджелудочной железы возник у 2,7%.
Слайд 19
Патология рака поджелудочной железы
Протоковая аденокарцинома, самая частая
форма рака. Такой морфологический вариант встречается у 80% больных
РПЖ. Средний размер опухоли при диагностике - 5 см. Медиана выживаемости - 16 недель. 1 год живут 17% больных, 5 лет - 1%. В 61% опухоль локализуется в головке, в 18% в теле и 21% - в хвосте.Гигантоклеточные аденокарциномы (6% случаев).
Железисто-плоскоклеточный рак (4%).
Муцинозная аденокарцинома (2%).
Муцинозная цистоаденокарцинома (1 %).
Ацинарный рак (гроздевидный) (1,5%).
Слайд 20
Стадирование рака
поджелудочной железы
По системе
TNM градации Т различаются следующим образом:
Т1- первичная опухоль
не распространяется за пределы поджелудочной железы. На самом деле клинически ранние раки поджелудочной железы являются биологически поздними. К моменту выявления опухоли самых малых размеров, клон раковых клеток уже прошел не менее 30 удвоений. Несовместимость с жизнью отмечается после 40 удвоений. Таким образом, опухоль уже просуществовала три четверти "отмеренной ей жизни" к моменту первичной диагностики.
Слайд 21
Стадирование рака
поджелудочной железы
Т2 - ограниченное распространение
на двенадцатиперстную кишку, желудок и желчный проток.
Т3 -
распространение рака по окружающим органам, исключающее возможность резекции. Градации N и M стандартные.
Слайд 22
Симптомы рака
поджелудочной железы
Ранние
признаки:
эпигастральные вздутия ( 31%),
общее недомогание,
слабость (23%),
запор (13%).
Маскирует заболевание развитие диабета, нередко подозревают болезни желчного пузыря, язвенную болезнь желудка.
Слайд 23
Симптомы рака
поджелудочной железы
Основные симптомы рака поджелудочной железы - желтуха
и боли. Эти симптомы отмечаются у 90% заболевших.Желтуха - признак опухолевого поражения головки поджелудочной железы, является следствием сдавления дистальной части общего желчного протока. При раке тела панкреас желтуха регистрируется лишь у 7% заболевших. При раке хвоста желтуха может быть обусловлена метастазами в печень. Безболевая желтуха не типична для РПЖ. Среди симптомов, сопровождающих желтуху - зуд, темная моча, светлый кал. Пальпируется увеличенный желчный пузырь ( в 29%) - симптом Курвуазье.
Слайд 24
Симптомы рака
поджелудочной железы
Боли - наиболее мучительный симптом РПЖ. При
раке хвоста и тела они регистрируются у 87% пациентов, при раке головки -в 72%. Связаны боли либо со сдавлением нервного сплетения позади верхнебрыжеечной артерии, либо с метастазированием в забрюшинные лимфоузлы и прорастанием экстрапанкреатических нервных сплетений. Боли могут локализоваться либо в левом верхнем квадранте живота, либо в спине. Характер болей может меняться при перемене положения. Иногда боли грызущие, напоминающие симптомы язвенной болезни, могут быть прерывистыми, спастическими, усиливающимися в ночное время, сопровождаются гиперестезией кожи. От панкреатитов, при которых также наблюдаются похожие боли, РПЖ отличается отсутствием гипертермии и лейкоцитоза.
Слайд 25
Симптомы рака
поджелудочной железы
Третий важный симптом РПЖ - необъяснимая для пациентов
потеря веса, даже при сохранении аппетита. Наблюдается она у 92% больных с локализацией рака в головке и у 100% при поражении тела или хвоста. Потеря веса вероятнее всего связана со стеатореей. С калом выделяется повышенное содержание нейтрального жира, жирных кислот - из-за нарушения внешнесекреторной функции поджелудочной железы.
Слайд 26
Маркеры рака
поджелудочной железы
Наиболее часто используется маркер СА-19-9. Он не является
специфичным для РПЖ, повышен при раке печени в 67%, раке желудка в 62%, раке толстой кишки в 19%. Маркер почти всегда положителен при опухолях, превышающих размер в 3 см.Если уровень СА-19-9 больше 1000 Ед/мл опухоль имеет размеры > 5 см и только 5% этих больных резектабильны.
Слайд 27
Маркеры рака
поджелудочной железы
У половины больных
положительным может быть и маркер СА-125 (наиболее типичный для
рака яичников).При исследовании крови можно обнаружить ускорение СОЭ, анемию, повышенный с-реактивный белок. Альбумины обычно у больных РПЖ уменьшены. В сыворотке возможно увеличение амилазы (что говорит о сдавлении панкреатического протока), липазы, панкреатической рибонуклеазы, эластазы, ингибиторов трипсина.
Слайд 28
Гистологическая классификация
Гистологическая классификация приводится согласно 3
изданию
международной Гистологической классификации опухолей экзокринной части поджелудочной железы:
8041/3 Мелкоклеточная
карцинома, БДУ8042/3 Овсяно-клеточная карцинома
8043/3 Мелкоклеточная карцинома
8044/3 Мелкоклеточная карцинома, промежуточно-клеточный вариант
8045/3 Комбинированная мелкоклеточная карцинома (рак)
8046/3 Немелкоклеточная карцинома
8070/2 Плоскоклеточная карцинома in situ, БДУ
8070/3 Плоскоклеточная карцинома, БДУ
8140/3 Аденокарцинома, БДУ
8141/3 Скиррозная аденокарцинома
Слайд 29
Клиника рака головки поджелудочной железы
Желтушный период наступает после
прорастания или сдавления опухолью общего желчного протока. Он характеризуется стойкой
и интенсивной механической желтухой, кожным зудом, появлением обесцвеченного кала и темно-коричневой мочи, увеличением размеров печени и желчного пузыря, вызванные застоем желчи. Чем ближе к протоку располагается опухоль, тем раньше возникает желтуха и тем больше возможность радикального лечения. Наряду с желтухой больных беспокоит боль в подреберье или надчревной области, нарастают похудание, слабость, исчезает аппетит. При прорастании двенадцатиперстной кишки или сдавлении ее опухолью появляется чувство перепол-нение желудка, рвота съеденной пищей. Возникает и прогрессирует печеночная недостаточность.
Слайд 34
Диагностические мероприятия (алгоритм):
Общий анализ крови, мочи;
Биохимический анализ
крови (общий белок, мочевина, креатинин, общий и прямой билирубин,
щелочная фосфатаза, трансаминазы, электролиты, глюкоза, ЛДГ, холестерин, фруктозофосфатальдолаза);Группа крови, резус-фактор;
Пальпация периферических лимоузлов, пальпаторное исследование прямой кишки, осмотр гинеколога (у женщин);
УЗИ органов брюшной полости, забрюшинного пространства, пункционная трепанбиопсия опухоли под УЗ-контролем;
Рентгенологическое исследование лёгких;
Слайд 35
Диагностические мероприятия (алгоритм):
КТ органов брюшной полости, забрюшинного пространства,
тонкоигольная пункционная аспирационная биопсия опухоли под КТ-контролем;
ФГДС исследование;
Рентгенологическое исследование
желудка (релаксационная дуоденография);Эндоскопическая РХПГ;
По показаниям: ФКС, ирригоскопия, МРТ, сцинтиграфия костей скелета, целиакография, определение антигена С19-9, карциноэмбрионального антигена (СЕА), соотношение cывороточного тестостерона к дегидротестостерону, чреспеченочная холангиоангиография, лапароскопия.
Слайд 36 Прежде чем начинать лечение рака поджелудочной железы, необходимо провести
диагностику заболевания. Главным методом определения онкологии является КТ. Однако
для окончательного диагноза необходимо провести пунктирование: биопсия с морфологическим исследованием под контролем КТ и УЗИ. Опухолевый маркер 19.9 СА не отличается большой информативностью. Однако желательно определить его на этапе диагностирования, потому что в ряде случаев эти данные могут понадобиться уже на этапе лечения.
Слайд 37
КТ-диагностика рака поджелудочной железы: современное
состояние проблемы
Проблема диагностики и
лечения рака поджелудоч-
ной железы (ПЖ) остается актуальной для современной
клинической
онкологии. Заболеваемость раком ПЖ не-уклонно растет как в нашей стране, так и за рубежом. Не-
смотря на совершенствование методов диагностики, хи-
рургической техники, появление новых противоопухоле-
вых препаратов, разработку комбинированных и ком-
плексных методов лечения больных раком ПЖ, общая
5-летняя выживаемость не превышает 5—20%
Слайд 39
3-ий Международный семинар
по многосрезовой компьютерной томографии (МСКТ),
3D визуализации,
виртуальной эндоскопии
6-8 июня 2002, Рим
Слайд 40
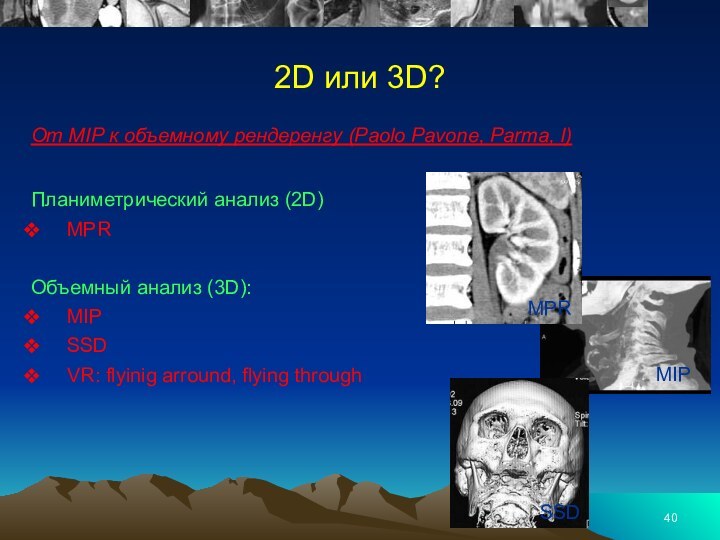
2D или 3D?
От MIP к объемному рендеренгу (Paolo
Pavone, Parma, I)
Планиметрический анализ (2D)
MPR
Объемный анализ (3D):
MIP
SSD
VR: flyinig arround,
flying throughMPR
MIP
SSD
Слайд 41
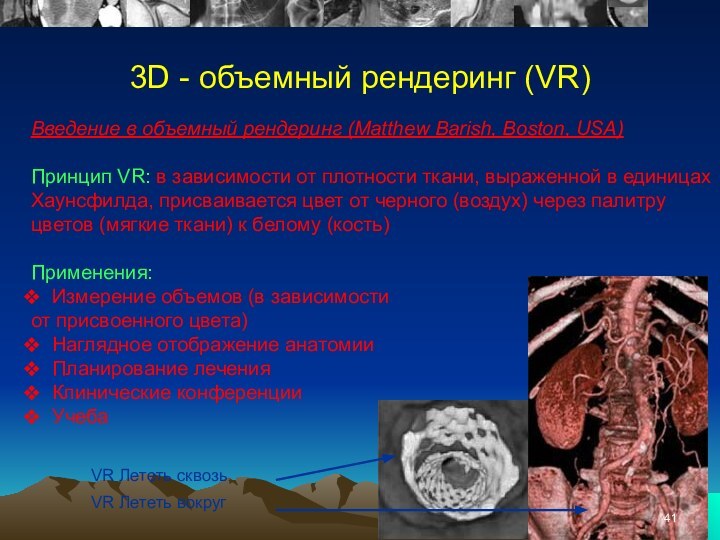
3D - объемный рендеринг (VR)
Введение в объемный рендеринг
(Matthew Barish, Boston, USA)
Принцип VR: в зависимости от плотности
ткани, выраженной в единицах Хаунсфилда, присваивается цвет от черного (воздух) через палитру цветов (мягкие ткани) к белому (кость)Применения:
Измерение объемов (в зависимости
от присвоенного цвета)
Наглядное отображение анатомии
Планирование лечения
Клинические конференции
Учеба
VR Лететь сквозь
VR Лететь вокруг
Слайд 42
Стратегии контрастного усиления при МСКТ
Объемная МСКТ: общие принципы
и доза облучения (James Brink, New Haven, USA)
Для снижения
дозы:Tube current modulation (SIEMENS)
Focal spot tracking (GE Light Speed): доза больше на 105% при 4х1,25 и на 10% при 4х5 (без focal spot tracking доза возрастает на 238 и 67% соответственно)
При увеличении числа детекторных блоков с 4 до 16 снижение рассеивания по краям
Ultrafast ceramic detector (SIEMENS) – снижение дозы на 30%
Слайд 43
Стратегии контрастного усиления при МСКТ
Объемная МСКТ: принципы назначения
контрастного вещества и расчета времени начала сканирования (James Brink,
New Haven, USA)Объем КВ зависит от веса пациента:
80 кг - 100 мл,
80-150 кг - 150 мл,
> 150 кг - 200 мл
Повышение скорости введения КВ:
Лучше усиление аорты
Не влияет на усиление печени
Лучше временное разделение артериальной и портовенозной фаз (1мл/сек - 18 сек, 4мл/сек - 41 сек)
Концентрация КВ:
400 мг/мл - полные пациенты, тонкие срезы
Слайд 44
Стратегии контрастного усиления при МСКТ
Эффективное использование КВ при
МСКТ (Friedrich Knollmann, Berlin, D)
Saline flash (NaCl):
Более выраженный
пик контрастного усиленияУменьшается расход КВ на 20 мл
Двухфазная инъекция:
36 мл, 6 мл/сек 64 мл, 2,5 мл/сек – лучше контрастирование аорты и периферических сосудов чем при однофазном введении 100 мл со скоростью 4,5 мл/сек
Слайд 45 МСКТ с криволинейными мультипланарными реконструкциями при опухолях поджелудочной
железы (Lawrence Chow, Stanford, USA)
Протокол при раке поджелудочной железы:
Нативная фаза – срез 10 мм после дачи 900 мл воды Поздняя артериальная – задержка 40 сек, 1,25 мм
Портовенозная – задержка 80 сек
В 11% случаев изоденсивный рак - вспомогательные признаки:
Деформация контура
Прерывание панкреатического протока
Дистальная атрофия
Лишь 10-15% пациентов имеют резектабельнй рак поджелудочной железы. Из них 30-50% - positive margine
Клинические применения: поджелудочная железа
Слайд 46
Одно из наиболее ценных преимуществ
МДКТ —
возможность мультипланарной реконструкции
(МПР) изображений и создания трехмерных изображе-
ний. МПР
позволяет достичь хорошего качества изобра-жения с высоким разрешением, изучить зоны интереса во
фронтальной, сагиттальной и других плоскостях на осно-
ве заданной кривой, делая изображение более наглядным
и привычным для клиницистов. МПР, выполненные в
различных плоскостях, помогают детализировать топо-
графоанатомические соотношения.
Слайд 47 Трехмерное моделирование на основе
МДКТ с болюсным контрастным усилением делает возможным создание объемных
изображений анатомических зон, в которых показаны соотношения патологического очага, сосудов и окружающих органов. Именно эти реконструкции позволяют хирургамнаглядно оценить получаемые при КТ изображения, увидеть нужные объекты в таких ракурсах, которые в реальных условиях, на операционном столе, недостижимы (например, сзади, ≪изнутри≫ и т.д.).Изображения, полученные после обработки данных,
значительно расширяют диагностические возможности
КТ, улучшают визуализацию панкреатических сосудов и
протоков ПЖ.
Слайд 48
Наиболее часто используемые методы
постпроцессорной обработки данных: проекция макси-
мальной
интенсивности, объемные построения, проек-
ции минимальной интенсивности и криволинейные пло-
скости.
В литературе встречается множество данных отом, что МПР изображений значительно повысила диа-
гностические способности МДКТ в выявлении опухолей
ПЖ, особенно малых размеров. Использование МДКТ-ангиографии с трехмерной
реконструкцией изображений дает возможность выявить
пути парапанкреатической, периневральной и лимфати-
ческой инвазии аденокарциномы ПЖ.
Слайд 49
При раке
панкреатобилиарной области парапанкреатические лим-
фатические сосуды поражаются довольно
часто, что имеет
прогностическое значение. Однако в литературе очень
мало данных
посвящено КТ-визуализации нормальной ипатологически измененной парапанкреатической лимфа-
тической системы. При поражении раком головки ПЖ
инфильтрация наиболее часто обнаруживается вдоль об-
щей печеночной артерии, а при поражении тела и хвоста
ПЖ — вокруг чревного ствола. Знание нормальной КТ-
анатомии лимфатической системы области ПЖ позволяет
выявлять ее патологические изменения, что существенно
для точного стадирования рака.
Слайд 50
Проведение МДКТ-ангиографии ПЖ стало неотъем-
лемой частью подготовки к
любой операции на органах
панкреатобилиарной области. При предоперационной
оценке главными задачами
являются: локализация адено-карциномы ПЖ, стадирование и определение локальной
резектабельности и анатомических вариантов расположе-
ния сосудов в данной зоне.
КТ — метод выбора при диагностике и оцен-
ке резектабельности рака поджелудочной железы, а со-
вместное использование дополнительных методов иссле-
дования (МРТ, эндоУЗИ, ПЭТ/КТ) позволит улучшить
точность диагностики и избежать ошибок при стадирова-
нии и оценке резектабельности опухоли.
Слайд 51
Общие принципы лечения
Лечение рака поджелудочной железы (далее – ПЖ) может быть
хирургическим, химиотерапевтическим, химиолучевым, комбинированным или симптоматическим. В выборе метода леченияисходят из данных предоперационной инструментальной оценки наиболее вероятной морфологической сущности опухоли, ее резектабельности, учитывают возраст больного, его соматический статус, наличие таких осложнений, как механическая желтуха, нарушение эвакуации из желудка, кишечная непроходимость. Важнейшим фактором является локализация опухоли, предрасполагающая различный объем операции.Все современные методы хирургического лечения рака ПЖ можно подразделить на радикальные и паллиативные.
Слайд 52
Хирургическое лечение рака поджелудочной железы
Споры по поводу роли хирургии при РПЖ на ослабевают
и продолжаются в течение многих лет. Есть крайние точки зрения - отказ от радикальных операций совсем и требование расширения объемов и показаний хирургического лечения.Первые считают, что после паллиативных вмешательств больные живут комфортабельнее и дольше, чем после радикальных резекций (ведущих к полной реконструкции верхнего отдела желудочно-кишечного тракта) и при которых высока послеоперационная летальность и неудовлетворительны отдаленные результаты.
Вторые исходят из того, что послеоперационная летальность, благодаря развитию анестезиологии и реанимации сократилась, а шанс выжить имеют лишь радикально прооперированные больные.
Слайд 54
Хирургическое лечение рака поджелудочной железы
Отсутствие
отдаленных метастазов и рентгенологических или клинических признаков нерезектабильности -
основание для предложения больному хирургического лечения.Для больных с желтухой преобладает тактика предварительного проведения желчеразгрузочных операций, якобы поскольку на фоне билирубинемии частота осложнений после радикальных вмешательств увеличивается.
Слайд 55
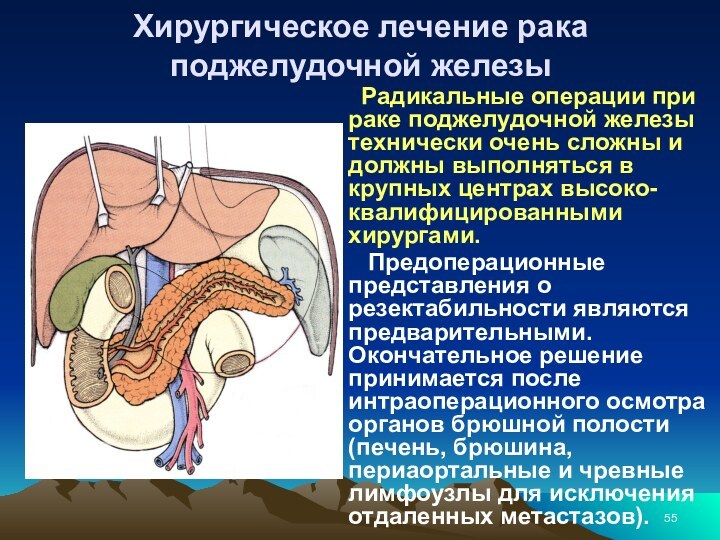
Хирургическое лечение рака поджелудочной железы
Радикальные
операции при раке поджелудочной железы технически очень сложны и
должны выполняться в крупных центрах высоко-квалифицированными хирургами.Предоперационные представления о резектабильности являются предварительными. Окончательное решение принимается после интраоперационного осмотра органов брюшной полости (печень, брюшина, периаортальные и чревные лимфоузлы для исключения отдаленных метастазов).
Слайд 56
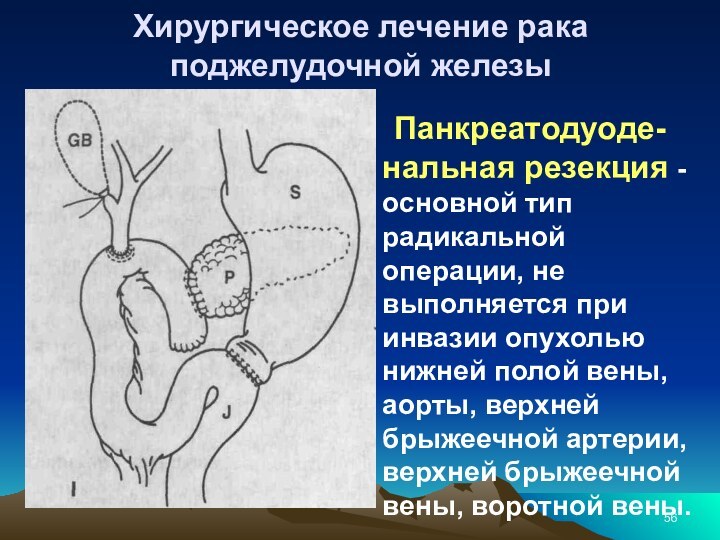
Хирургическое лечение рака поджелудочной железы
Панкреатодуоде-нальная
резекция - основной тип радикальной операции, не выполняется при
инвазии опухолью нижней полой вены, аорты, верхней брыжеечной артерии, верхней брыжеечной вены, воротной вены.
Слайд 57
Хирургическое лечение рака поджелудочной железы
В
обзоре публикаций девяностых годов (13 сообщений) подводятся итоги выполнения
панкреатодуоденаль-ных резекций у 1238 больных. Средняя их выживаемость равна 15,5 месяцев. 5 лет выжили 11,1%.
Слайд 58
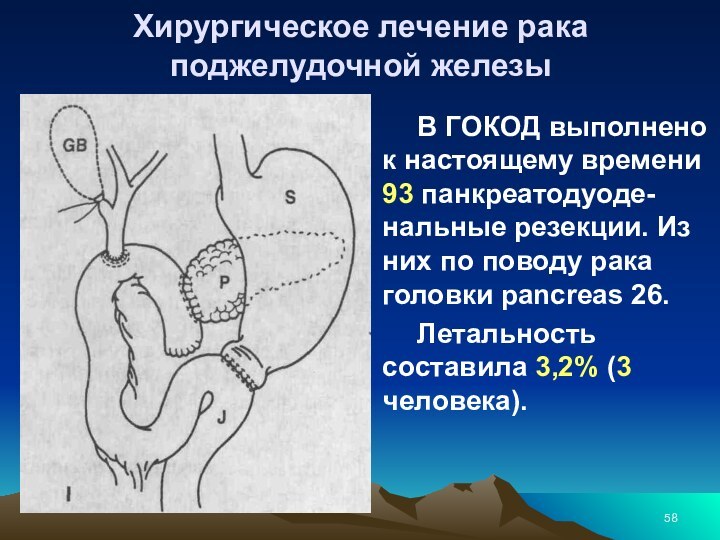
Хирургическое лечение рака поджелудочной железы
В ГОКОД выполнено к настоящему времени 93 панкреатодуоде-нальные резекции.
Из них по поводу рака головки pancreas 26.Летальность составила 3,2% (3 человека).
Слайд 59
Хирургическое лечение нерезектабельного рака поджелудочной железы
В поздних случаях РПЖ развивается сдавление опухолью двенадцатиперстной
кишки и как следствие этого, мучительная рвота. Паллиативным вмешательством при этой ситуации является наложение гастроэнтеростомии. Часто гастроеюностомия выполняется профилактически (без симптомов рвоты) во время желчеразгрузочной операции.Последние 10-15 лет отвод желчи при сдавленном общем желчном протоке осуществляют с помощью пластиковых, резиновых или металлических трубчатых стентов, вводимых чрескожно транспеченочно или эндоскопически. Эти манипуляции легче переносятся больными, чем наложение хирургических анастомозов, но послеоперационная летальность остается высокой (25%) за счет частого развития инфекционных холангитов. Помимо резиновых стентов используются и металлические.
Слайд 60
Хирургия, тем
не менее, используется с паллиативными целями у многих больных
для контроля желтухи, непроходимости, болей.При желчеразгрузочных манипуляциях важно руководствоваться следующими принципами:
а) нужно выяснить уровень и причину непроходимости внепеченочных желчных путей, установить возможность радикального удаления опухоли;
б) нельзя приступать к созданию билиодигестивных соустий без уверенности в полной проходимости соединяемых полых органов;
в) билиодигестивный анастомоз должен располагаться в 3-4 см от границы опухоли;
г) этот анастомоз не должен быть узким.
Слайд 61
Паллиативные операции при раке ПЖ
Низкая резектабельность при раке ПЖ делает практически неизбежным применение
ряда паллиативных вмешательств, имеющих симптоматический смысл и облегчающий самочувствие и состояние больных. Из всего многообразия клинического проявления рака ПЖ паллиативные хирургические вмешательства, как правило, выполняются только при трех наиболее тяжелых осложнениях заболевания: механической желтухе, дуоденальной непроходимости, нестерпимых (некупируемых) болях.
Слайд 62
1. Билиарная декомпрессия при механической желтухе.
1.1. Показания:
как первый
этап лечения больных резектабельным раком ПЖ, осложненным механической желтухой;
при
нерезектабельном раке ПЖ, но при отсутствии внутрипеченочных метастазов, разобщающих сегментарные желчные протоки в обеих долях печени.1.2. При выборе метода желчеотведения необходимо учитывать:
уровень опухолевой обструкции билиарного дерева;
распространенность опухолевого поражения и состояние больного, то есть
планируется ли после билиарной декомпрессии удаление опухоли;
прогнозируемое время жизни больного после желчеотведения, если радикальная операция не планируется;
угроза осложнений и качество технологического исполнения того или иного метода желчеотведения.
Слайд 63
2. Интраоперационные методы декомпрессии желчных протоков.
2.1. Применяемые в
настоящее время билиодигестивные анастомозы:
холецистоеюноанастомоз;
холецистогастроанастомоз;
холецистодуоденоанастомоз;
холедоходуоденоанастомоз;
холедохоэнтероанастомоз;
гепатикоэнтероанастомоз.
2.2. Анастомозы с желчным пузырем наиболее
просты и безопасны. Однако формирование их может быть выполнено только при достаточно высоком (более 1 см от края опухолевой инвазии) уровне впадения пузырного протока в общий желчный проток.2.3. Анастомозы с общим желчным протоком – более сложный и рискованный вид желчной декомпрессии при нерезектабельном раке ПЖ.
Слайд 64 2.3. Анастомозы с общим желчным протоком – более
сложный и рискованный вид желчной декомпрессии при нерезектабельном раке
ПЖ.2.4. Гепатикоеюноанастомоз имеет наиболее широкие показания. При этом в соустье с тощей кишкой может участвовать как общий печеночный проток, так и печеночные протоки более мелкого калибра. Анастомоз лучше формировать с мобилизованной по Ру петлей тощей кишки, так как это практически исключает рецидив желтухи и холангит в позднем периоде. Указанный анастомоз предпочтителен среди больных неоперабельным билиопанкреатодуоденальным раком, осложненным механической желтухой, с прогнозируемым
временем жизни больного более 6 месяцев.
Слайд 65 Выполнение холецистогастро- и холецистодуоденоанастамоза допустимы лишь в единичных
случаях в качестве вынужденного вмешательства, например при обширном метастазировании
опухоли в лимфатические узлы корня брыжейки тонкой кишки, а также при крайне тяжелом состоянии больных, когданужно максимально сократить продолжительность операции.
137.3. Наружное дренирование выполняется в виде:
холецистостомии (может осуществляться как лапароскопическая холецитостомия (ЛХС), так и чрескожная чреспеченочная холецистостомия под контролем УЗИ, КТ);
гепатикостомии;
эндоскопического билиарного дренирования и стентирования;
чрескожного чреспеченочного дренирования желчных протоков.
Слайд 66
Этот тип оперативного вмешательства крайне неблагоприятен у тяжелых
больных,
поскольку заведомо обрекает их на существование наружного желчного свища.
Однако иногда эта операция – единственно возможный способ сохранения жизни больным.137.4. Для устранения непроходимости двенадцатиперстной кишки ис-
пользуют в основном гастроэнтероанастомоз. Более оправдано применение
переднего впередиободочного гастроэнтероанастомозана на длинной петле с межкишечным соустьем, что продиктовано опасностью инвазивного роста опухоли или ее метастазирования в брыжейку поперечной ободочной кишки и возможным вовлечением в неопластический процесс созданного соустья.
Слайд 67
Химиотерапия
1. Кальция фолинат 20 мг/м2 в вену
в течение 10 мин;
флуороурацил 425 мг/м2 в вену в
течение 10 мин.Препараты вводят в 1–5-й день 6 курсов. Интервал между курсами – 4 недели.
2. Гемцитабин 1000 мг/м2 (инфузия в вену в течение 30 мин) в 1-й, 8-й и
15-й дни, 6 курсов. Интервал между курсами – 4 недели.
3. Гемцитабин 1000 мг/м2 (инфузия 30 мин) раз в неделю в течение 7 не-
дель. После 2-недельного перерыва – 3 еженедельных введения, затем – 2-недельный перерыв, 3 еженедельных введения и т.д.
Слайд 68
4. FOLFIRINOX:
оксалиплатин 85 мг/м2 в вену в
течение 2 часов;
кальция фолинат 400 мг/м2 в вену в
течение 2 часов;иринотекан 180 мг/м2 через 30 мин в вену в течение 90 мин через
Y-коннектор;
флуороурацил 400 мг/м2 инфузия в вену струйно в течение 46 часов после
введения оксалиплатина.
Повторные курсы – через 2 недели.
Слайд 69
Химиолучевая терапия
1. Химиотерапия:
флуороурацил 500 мг/м2 внутривенно струйно в
1–3-й день первой и последней (обычно 1-й и 5-й)
недель лучевой терапии.2. Проводится 3D конформная лучевая терапия на фоне проведения
химиотерапии в РОД 1,8 Гр, СОД 45–54 Гр (при необходимости с оптимизацией дозы, то есть с использованием модуляции интенсивности дозы (IMRT), на пос-
леоперационное ложе опухоли, проекцию регионарных лимфатических узлов;
ложем опухоли считается проекция опухоли на заднюю стенку живота).
Слайд 70 Ложе опухоли и края резекции определяются по данным
предоперационной компьютерной томографии, по локализации скрепочного шва, маркировке границ
клипсами во время операции. В случаях выполнения хирургического вмешательства химиолучевая терапия проводится через 6–8 недель после операции.3. Лучевая терапия обычно проводится с двух (AP–PA) или нескольких противоположных полей с защитой спинного мозга (максимум СОД не более
45 Гр при резектабельных опухолях или при адъювантном облучении; при нерезектабельных опухолях или при предоперационном облучении – максимум
СОД не более 45 Гр в объеме облучения спинного мозга не более 0,03 см3), ограничением облучения печени (средняя СОД не должна превышать 30 Гр при нерезектабельных опухолях или при предоперационном облучении и 25 Гр – при
резектабельных опухолях или при адъювантном облучении), почек (общий объем почечной паренхимы, включаемый в зону облучения, не должен превышать
Слайд 71 2/3 одной почки), сердца
(не более 30% миокарда получают дозу в 40 Гр),
желудка, двенадцатиперстной кишки, тонкой кишки (максимум СОД не более 55Гр; не более 30% объема каждого из указанных органов получает дозу в интервале 45–55 Гр при нерезектабельных опухолях или при предоперационном об-лучении; не более 10% объема каждого из указанных органов получает дозу в интервале 50–54 Гр при резектабельных опухолях или при адъювантном облучении). При использовании боковых полей дозы, подводимых с одного бокового поля, не должны превышать 20 Гр.
У всех пациентов применяется положение «лежа на спине» при симуляции
и лечении.
Слайд 72 Главная цель современной лучевой терапии - направленное уничтожение
раковых клеток, которое осуществляется при воздействии на опухоль заряженных
высокой энергией рентгеновских лучей или других видов ионизирующего излучения. Высокодозная радиотерапия разрушает генетическую информацию злокачественных клеток и опухоль погибает.
Слайд 74
модуляция интенсивности полей излучения (технология RapidArc)
модифицированная по интенсивности
лучевая нагрузка (IMRT)
обязательное трехмерное виртуальное планирование полей облучения (3D),
что достигается благодаря использованию мультилепесткового коллиматора, который позволяет сформировать дозное поле любой необходимой формыузконаправленная фокусная лучевая терапия (линейный ускоритель или Кибер-Нож)
Слайд 75
Индивидуальная программа лучевого лечения рака поджелудочной железы
Программа радиотерапии
(лучевого лечения) рака всегда назначается в зависимости от вида
злокачественной опухоли, ее расположения и многих других, не менее важных, факторов, таких как: стадия болезни, распространенность ракового процесса, предыдущее лечение и его результаты, общее состояние здоровья и наличие сопутствующих болезней.Слайд 76 Для воздействия на экзокринные опухоли поджелудочной железы (аденокарцинома)
существует несколько наиболее распространенных вариантов радиотерапевтического лечения, которые описаны
ниже. Эффективность лучевой терапии в лечении нейроэндокринных опухолей поджелудочной железы пока не доказана.Слайд 77 Лучевая терапия рака поджелудочной железы чаще всего проводится
вместе с химиотерапией перед операцией, как предоперационная поддержка (неоадъювантная
терапия) или после операции, для локального контроля рецидива опухоли (адъювантная терапия), потому что в 50% случаев, даже после полного оперативного удаления опухоли, рак поджелудочной железы имеет склонность к рецидивированию или метастазированию.Слайд 78 К сожалению, только 15-20% больных раком поджелудочной железы
подлежат оперативному лечению. Лучевую терапию одновременно с химиотерапией назначают
и на начальных этапах лечения болезни.Слайд 79 Комбинированное применение лучевой терапии одновременно или поочередно с
химиотерапией является всемирно принятым методом лечения неоперабельных раковых опухолей
поджелудочной железы. Например, если на ранних стадиях болезни обнаружены метастазы в такие органы, как печень и легкие, то лучевая терапия позволяет избавить пациена от длительных сеансов химиотерапии и ее побочных эффектов. Таким пациентам обычно назначается 3-4 сеанса химиотерапии для уничтожения метастазов, а после этого проводится комбинированная схема лучевого лечения одновременно с химиотерапией.Слайд 80 В некоторых случаях, у пациентов с метастазирующей формой
рака поджелудочной железы, используется паллиативная лучевая терапия. Главная цель
паллиативного лучевого лечения состоит в уменьшении или в полном уничтожении таких тяжелых симтомов и проявлений рака, как боль, тошнота, рвота или кровотечение.
Слайд 81
Как действует лучевая терапия (радиотерапия)
Высокоэнергетическое рентгеновское излучение и
большие дозы ионизирующих частиц способны убивать или предотвращать размножение
раковых клеток, которые размножаются гораздо быстрее, чем здоровые клетки организма. Современное оборудование для лучевого лечения обеспечивает точность доставки дозы излучения, минимальное повреждение здоровых тканей и возможность эффективного воздействия даже на крупные опухолевые образования.Слайд 82 Во время предварительного планирования лучевого лечения, специалисты-радиологи досконально
расчерчивают виртуальную модель опухоли и выбирают индивидуальные параметры облучения.
Это очень важно, потому что в результате радиотерапии опухоль должна получить необходимую дозу облучения, которая приведет к гибели раковых клеток.Слайд 83 Самым распространенным видом лучевого воздействия на злокачественные опухоли
поджелудочной железы является наружная (дистанционная) радиотерапия, при которой излучение
создают внешние источники. Программа радиотерапевтического лечения включает определенное число сеансов с фиксированными дозами облучения, которые проводятся через равные промежутки времени, как правило, ежедневно, в течение 5-6 недель (режим стандартного фракционирования).Слайд 84 При раке поджелудочной железы используются также новейшие методы
радиотерапии, такие как стереотаксическая радиотерапия с использованием методики Кибер-нож
и технология лучевого воздействия RapidArc с модуляцией интенсивности, которые обеспечивают прицельное облучение опухоли за небольшое число сеансов.Слайд 85 Технология RapidArc основана на использовании высокоточных линейных ускорителей
совместно с компьютерной томографией. В режиме реального времени RapidArc
позволяет направлять на раковую опухоль облучение в 10 раз большей мощности, чем у аппаратов предыдущего поколения, не поражая при этом здоровые органы. Использование системы RapidArc значительно сокращает общую продолжительность курса лучевого лечения (до 80%).
Слайд 86
Побочные эффекты лучевой терапии
Перед началом лучевой терапии врач-радиолог
даст Вам подробную информацию о возможных побочных эффектах и
мерах их устранения. Побочные эффекты могут возникать уже во время курса лучевой терапии или после окончания лучевого лечения. Во время лучевой терапии важен ежедневный врачебный контроль состояния пациента, который позволяет, при развитии выраженных побочных эффектов, вовремя остановить или изменить программу лучевого лечения.Слайд 87 Побочные эффекты радиотерапии можно разделить на две большие
группы: острые и хронические. Слабость и потерю аппетита можно
назвать самыми распространенными побочными эффектами лучевой терапии. Тошноту, рвоту и диарею также можно включить в список наиболее частых побочных эффектов. Практически всегда у пациентов во время лучевого лечения присутствуют реакции со стороны кожи.Слайд 88 Острые последствия лучевого лечения возникают уже через 4-5
недель после начала курса радиотерапии и постепенно исчезают в
течении 2-3-х недель после окончания лечения. Хронические или отсроченные реакции на лучевое лечение проявляются гораздо позже, когда лечение уже закончено, и справиться с ними гораздо сложнее.
Слайд 89
Варианты лучевого лечения рака поджелудочной железы
Для лечения различных
видов рака используется несколько видов лучевой терапии: дистанционная (наружная)
радиотерапия, контактная радиотерапия (брахитерапия) и стереотаксическая радиохирургия. Лечение рака поджелудочной железы чаще всего проводится с использованием новейших методик дистанционной радиотерапии, таких как:
Слайд 90
Методы лечения рака: лучевая терапия (радиотерапия)
Новейшие технологии лучевой
терапии, такие как стереотаксическая радиохирургия (Кибер-нож) и высокоточные линейные
ускорители последнего поколения (модифицированный линейный ускоритель, технология RapidArc) позволяют проводить лучевое лечение рака с максимальной эффективностью и с минимальным повреждением здоровых тканей и органов.Слайд 91 Лучевая терапия при Cr поджелудочной железы по эффективности
занимает II место после радикальной операции
Показания к ЛТ:
1.
Местнораспространенный Cr поджелудочной железы после оперативного и гистологического подтверждения
диагноза (пробная лапаротомия или билиодигестивный
анастомоз)
2. Неоперированные больные (при гистологической
верификации)
3. Больные после паллиативной резекции по поводу
Cr поджелудочной железы или трансдуоденальной
папиллоэктомии по поводу Cr фатерова соска в
ближайшие сроки после операции (до 1 месяца)
4. Больные с Reci Cr поджелудочной железы после
радикальной операции
Слайд 92
Абсолютные противопоказания к ЛТ
выраженная диарея
язвенная болезнь желудка
или
двенадцатиперстной кишки
механическая желтуха
наличие отдал выраженная раковая
кахексияенных Mts (кроме единичного
mts в левой доле печени)
кровотечение из опухоли
лейкопения < 3,5·109/л,
тромбоцитопения < 150·109/л
Слайд 93
Предоперационное облучение применяется в
настоящее время редко. Известно
исследование в
раковом центре в Филадельфии. Из 27 больных,
подвергнутых предоперационному облучению 50 Гр,
удалось прооперировать 13 человек. 60% из них выжили
1 год, 43% - 3 года.
Слайд 94
Интраоперационное облучение как самостоятельный
метод также не находит
широкого применения. Во время
лапаротомии устанавливают неоперабельность
опухоли, затем
ē10-15 мЭВ однократно облучают в дозе 20-30 Гр поле 10х10, средняя продолжительность жизни
5,5 месяцев. Высок риск развития осложнений –
кровотечение, панкреонекроз. Для улучшения
результатов возможно уменьшение РОД 10-20 Гр, с
последующей дистанционной ЛТ СОД 50 Гр. При этом
средняя выживаемость составляет 16 месяцев,
ремиссия в течении года у 82% больных.
Слайд 95
Эффективность внутритканевой лучевой терапии
опухолей панкреас невелика, средняя
продолжи-
тельность жизни 6-7 месяцев, % осложнений такой же как
и при интраоперационной ЛТ. Используют J125 (общая доза 50Гр).
Возможно проведение послеоперационной ЛТ в
дозе 40-50 Гр через 1 месяц после резекции опухоли, что приводит к увеличению средней продолжительности жизни до 20 месяцев.
При нерезектабельных опухолях поджелудочной железы наиболее целесообразно проведение
дистанционной ЛТ + введение 5Fu по 250 mg за 30
минут до ЛТ (Σ 4,5 Гр).
Слайд 96
При этом в зону лучевого воздействия на
I
этапе (после КТ-топометрии) включают опухоль и
регионарные лимфоузлы трех
уровней (панкреатодуоденальные, верхние и нижние
панкреатические, ворот селезенки, чревные,
парааортальные) РОД 2 Гр СОД 40-50 Гр, затем
после трехнедельного перерыва ЛТ на опухоль
РОД 2 Гр СОД 20 Гр.
Медиана выживаемости – 15 месяцев.
Слайд 97
Одним из направлений улучшения результатов при
неоперабельном раке
поджелудочной железы является
сочетание ЛТ и химиопрепаратов.
По литературным данным сочетание
Гемзар 1000 mg/m² 1,8,15 дни + ЛТ 30 Гр за 15 фракций, в 27% случаев дало объективное улучшение.
Комбинация ЛТ 60 Гр + FAP (фторурацил+DOXO+цисплатин)
обеспечило медиану выживаемости в 15 месяцев в группе из 32 больных местнораспространенным раком поджелудочной железы.
Комбинация FEP (фторурацил+эпирубицин+цисплатин) вместе
с ЛТ СОД 63 Гр обусловили одногодичную выживаемость в
42% случаев.
Слайд 98 При нерезектабельных опухолях оценивалось введение химиопрепаратов одновременно с
облучением
Слайд 99
При монотерапии используют:
5Fu в различных режимах 500 mg/m²,1000
mg/m² в/в 5 дней
Митомицин С 5-6 mg/m² каждые
4 неделиДоксорубицин 60-75 mg/m² 1 раз/3 недели
Ифосфамид 1000 mg/m² 5 дней подряд каждые 3 недели
Кампто в/в 350 mg/m² 1 раз/3 недели
Паклитаксел 200 mg/m² 1 раз/3 недели
Гемзар 1000 mg/m² 1,8,15 дни
Слайд 100
Возможно проведение комбинированной химиотерапии:
Фторурацил 600 mg/m² 1,2,5,6 и 9 недели
FAM
– Доксорубицин 30 mg/m² 1 раз/нед. 1,5,9 неделиМитомицин С 10 mg/m² 1 раз/нед. 1 и 9 недели
Медиана выживаемости 11,6 недели
Митомицин С 12 mg/m² 1-й день
MFL - Фторурацил 400 mg/m² 1-5 день
Лейковорин 200 mg/m² 1-5 день
Эффект 33% случаев
Фторурацил 500 mg/m² в/в 1-5 день
FCD - Цисплатин 30 mg/m² в/в 1-5 день
Доксорубицин 80 mg/m² в/в 1день
Слайд 101
При проведении комбинированной химиотерапии
по сравнению с режимом
монотерапии отмечается
увеличение выживаемости пациентов (17% против 9%)
В течение
3-х лет (2002-2004 гг.) в радиологическом отделении ГОКОД пролечено 59
пациентов с Cr pancreas.
В 2002 году 2 пациенткам проведена
субтотальная дистальная резекция поджелудочной
железы, затем послеоперационный курс ЛТ на
линейном ускорителе СОД 50 Гр на ложе опухоли и
зоны регионарного метастазирования + 6 курсов ПХТ.
Пациенты живы, без рецидивов.
ЛТ по радикальной программе + 5Fu – 35 пациентам.
Только ЛТ – 20 пациентам.
Слайд 102
Лечение по стадиям
1. Стадия IА–В: хирургическое лечение;
адъювантная химиотерапия
(6 курсов химиотерапии по схеме флуороурацил + кальция фолинат);
химиолучевая
терапия при R1 резекции.2. Стадия IIA–B, III:
хирургическое лечение при резектабельных опухолях;
адъювантная химиотерапия (6 курсов химиотерапии по схеме флуороурацил + кальция фолинат);
химиолучевая терапия при нерезектабельных, а также в случаях при R1–2
резекции;
паллиативные хирургические вмешательства.
Слайд 103
3. Стадия IV:
химиотерапия;
паллиативные хирургические вмешательства;
симптоматическая терапия.
4. Рецидив рака
ПЖ:
химиотерапия;
паллиативные хирургические вмешательства;
химиолучевая терапия.
Слайд 104
Наблюдение, сроки и объем обследования
1. Режим наблюдения:
первый год
– 1 раз в 3 месяца;
второй год – 1
раз в 6 месяцев;в последующем (пожизненно) – 1 раз в год.
2. Объем наблюдения:
физикальное обследование;
лабораторное исследование;
опухолевый маркер СА 19-9;
инструментальное исследование (УЗИ брюшной полости,забрюшинного
пространства и малого таза, рентгенологическое исследование легких);
консультация смежных специалистов (гинеколог);
фиброколоноскопия, ирригоскопия, компьютерная томография, МРТ, сцинтиграфия костей скелета, лапароскопия, КТ – по показаниям.
Слайд 105
Метастазирование.
Метастазирование при раке поджелудочной железы происходит лимфогенным, гематогенным и
имплантационным. При гематогенном метастазировании чаще всего поражаются печень, почки, легкие, кости,
другие органы. Имплантационное метастазирование характерно распространением метастазов по брюшине (карциноматоз брюшины, раковый асцит).Слайд 106 Метастазирует рак поджелудочной железы рано, чаще
в регионарные лимфатические узлы и печень. Возможно также метастазирование
в легкие, кости, брюшину, плевру, надпочечники и др.Слайд 107 Лимфогенное метастазирование происходит в несколько этапов, на каждом из
которых поражаются лимфатические узлы различной локализации. На первом этапе
метастазы проникают в головку поджелудочной железы; на втором этапе затрагиваются ретропилорические и гепатодуоденальные лимфатические узлы; на третьем этапе поражаются чревные и верхнебрыжечные лимфоузлы; на четвертом этапе метастатическому поражению подвергаются забрюшинные (парааортальные) лимфатические узлы.
Слайд 108
Профилактика рака поджелудочной железы:
необходимо отказаться от курения;
ликвидация негативного
воздействия внешней среды;
безотлагательное врачевание хронического панкреатита и сахарного диабета;
если
имеются наследственные формы панкреатита, необходимо также осуществлять постоянные профилактические осмотры.
Слайд 109
Прогноз.
При опухолях панкреато-дуоденальной зоны прогноз серьезный, ибо раннее
распознавание этих опухолей в большинстве случаев затруднено и выполнение
радикальных вмешательств возможно лишь в ограниченном числе случаев.Почти у 70% больных диагноз ставят поздно. Результаты лечения таких больных в связи с этим очень плохие. В США аденокарцинома поджелудочной железы занимает 4 место в структуре онкологической смертности.
Слайд 110
Заключение
Рак поджелудочной железы - трагичная глава клинической онкологии
по исходам болезни.
Поражают отдаленные результаты . Медиана выживаемости больных
по американским данным - 4,1 месяца, пять лет выживают менее 5% заболевших. Соотношение показателей смертности к заболеваемости по данным ВОЗ равняется 0,99.Большое значение имеют паллиативные хирургические вмешательства для контроля желтухи и при сдавлении опухолью двенадцатиперстной кишки.
Слайд 111
Заключение
Возможно улучшение отдалённых результатов радикальных хирургических
вмешательств будет достигнуто в применении предоперационного облучения с последующей
после агрессивной операции адъювантной химиотерапией.Именно такой вариант комплексного лечения РПЖ предложен в нашем протоколе для утверждения в НИИО в качестве стандарта.