служит резервуаром для всех биохимических реакций клетки. При участии
воды происходит теплорегуляция[Вода
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть


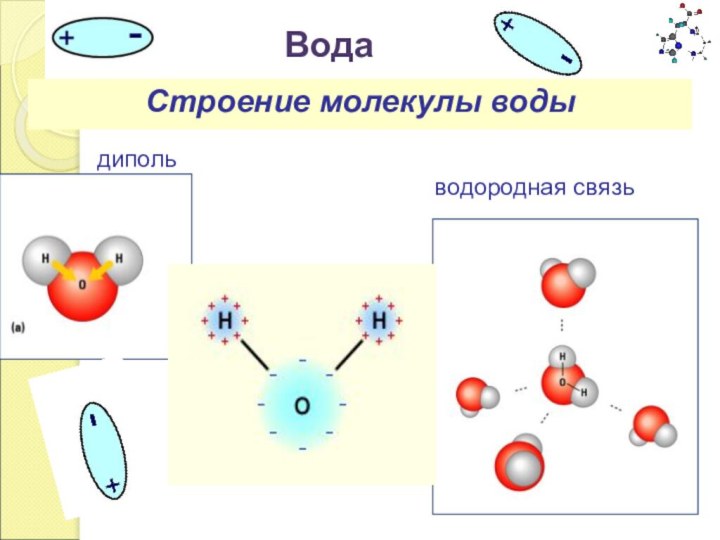







Вода
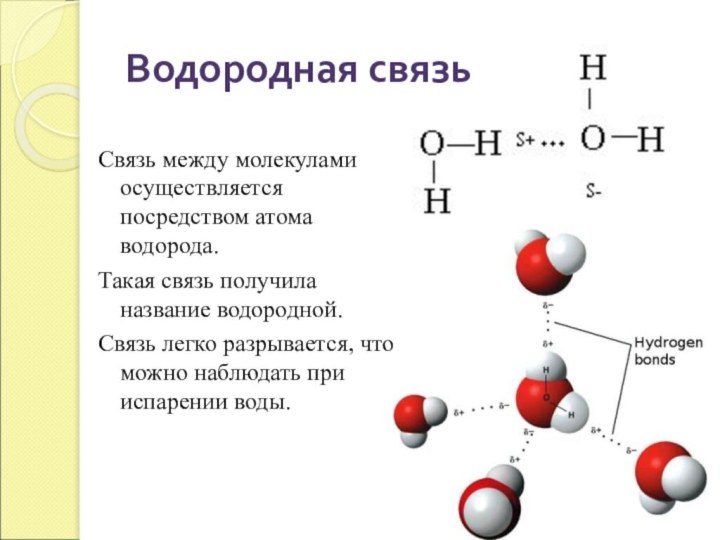
Водородная связь
Аномалии воды
Функции воды