- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Антропогенное воздействие на биосферу. Рост техносферы в XX веке
Содержание
- 2. Содержание лекции Рост техносферы в XX
- 3. Рост техносферы в XX векеТехносфера – это
- 4. Виды воздействия человека на окружающую средуПо способу
- 5. Загрязнение окружающей средыЗагрязнение – поступление в естественную
- 6. АэрополлютантыТвёрдые частицы (пыль, дым, сажа),Оксид углерода (CO),
- 7. СмогСмог (фотохимический туман) – многокомпонентная смесь газов
- 8. Кислотные осадки Кислотными осадками называются
- 9. Экологический вред кислотных осадков Нарушение
- 10. Озоновые дыры
- 11. Скачать презентацию
- 12. Похожие презентации
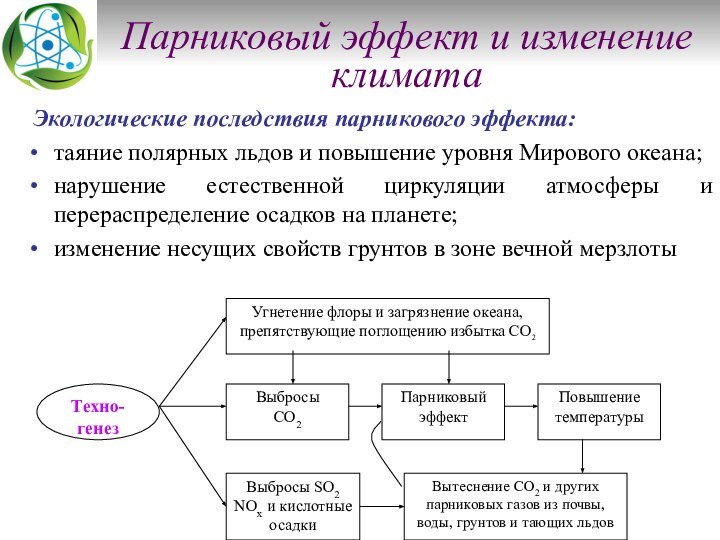
Содержание лекции Рост техносферы в XX веке. Виды воздействия человека на окружающую среду. Загрязнение атмосферы и его глобальные следствия: кислотные осадки, изменение концентрации озона в стратосфере и образование озоновых дыр, парниковый эффект и изменение








Слайд 3
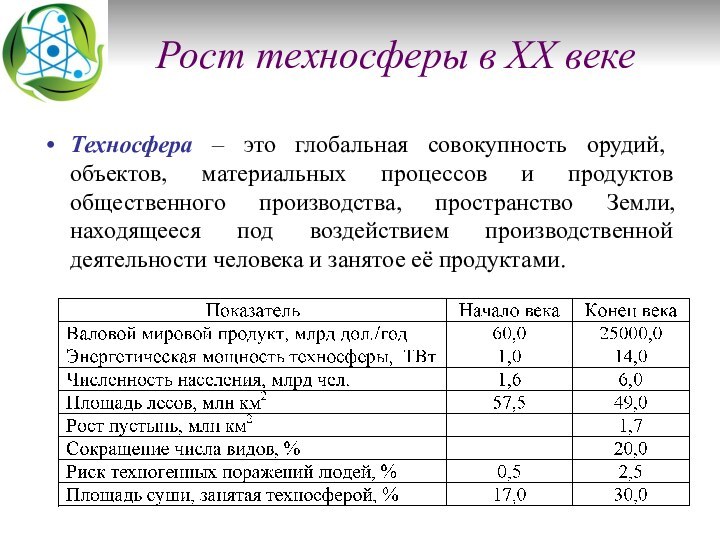
Рост техносферы в XX веке
Техносфера – это глобальная
совокупность орудий, объектов, материальных процессов и продуктов общественного производства,
пространство Земли, находящееся под воздействием производственной деятельности человека и занятое её продуктами.
Слайд 4
Виды воздействия человека на окружающую среду
По способу реализации:
прямое воздействие – это непосредственное, но отнюдь не желаемое
и планируемое;опосредованное воздействие - непреднамеренное изменение природной среды в результате цепи природных реакций, каждая из которых влечёт за собой изменение других, не связанных с нею первичных и вторичных явлений, вследствие хозяйственных мероприятий, называются.
Сумму прямых и опосредованных влияний человека на окружающую среду называют антропогенным (от греч. anthropos – человек, genos – происхождение) воздействием.
Совместное воздействие нескольких факторов может быть аддитивным, кумулятивным или синергическим
Слайд 5
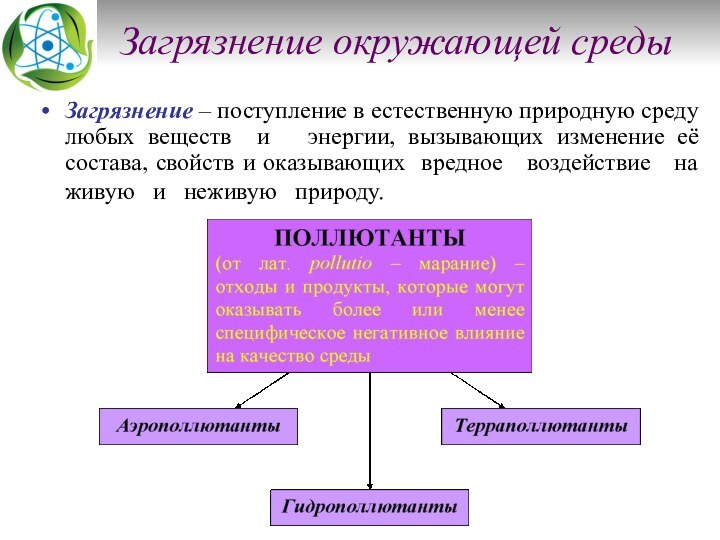
Загрязнение окружающей среды
Загрязнение – поступление в естественную природную
среду любых веществ и энергии, вызывающих изменение её
состава, свойств и оказывающих вредное воздействие на живую и неживую природу.
Слайд 6
Аэрополлютанты
Твёрдые частицы (пыль, дым, сажа),
Оксид углерода (CO), углекислый
газ (CO2),
Диоксид серы (SO2),
Оксиды азота (NO и
NO2), Углеводороды,
Соединения фосфора,
Сероводород (H2S),
Аммиак (NH3),
Хлор и фтористый водород (HF).
Общая масса загрязнений, выбрасываемых в атмосферу:
в мире около 800 млн т/год,
в России 48 млн т/год,
в Свердловской области 434 кг/чел·год.
Слайд 7
Смог
Смог (фотохимический туман) – многокомпонентная смесь газов и
аэрозольных частиц.
Условия образования смога:
- безветрие или
очень слабый обмена воздуха в приземном слое;- наличие высокой концентрации углеводородов, оксидов азота и серы;
- интенсивная солнечная радиация.
NO2 + hν → NO + O*
O* + O2 → O3
O3 + углеводороды → органические соединения
перекисной природы
Фотооксиданты – источник свободных радикалов, отличающихся особой реакционной способностью.
Слайд 8
Кислотные осадки
Кислотными осадками называются дожди,
туманы, снег, которые имеют pH < 7 (pH =
- lg [H+]).Суммарные (брутто) реакции химических превращений в атмосфере:
Величины pH атмосферных осадков:
- около 150 тыс. лет назад при образовании ледяного покрова Гренландии 6,0÷7,6;
- во второй трети XX века в Германии, США и Японии 4,0÷4,5; в Шотландии и Норвегии 2,5÷2,7;
- в 1981 г. в Китае зафиксированы осадки pH = 2,25.
Слайд 9
Экологический вред кислотных осадков
Нарушение процессов
в живых организмах, связанных с действием ферментов, гормонов, регулирующих
обмен веществ, рост и развитие.Деградация лесов, особенно хвойных.
Разрушение зданий и сооружений вследствие ускорения коррозии металлов, нарушения целостности лакокрасочных покрытий и стёкол.
Снижение плодородия почв и обострение дефицита питательных веществ как результат усиления процесса выщелачивания биогенов и снижения активности редуцентов и азотфиксаторов.
Выщелачивание тяжёлых металлов из почв и горных пород, ранее находившихся в нерастворимых соединениях, повышение их токсичности.
Слайд 10
Озоновые дыры
Реакции
образования озона:
Эколого-биологическое значение озона:
служит охранным щитом от жёсткого
ультрафиолета;экзотермическая реакция разложения озона приводит к нагреванию стратосферы и сохранению тепла в нижних слоях атмосферы из-за конвективного переноса тепла.
Реакции дополнительного разрушения озона за счёт действия веществ естественного и антропогенного происхождения:
O2 + hν → O + O (λ < 175 нм);
O2 + O + М (О2/N2) → O3 + М*;
O3 + О→ 2O2 + 392 кДж;
O3 + hν→ O + O2 (λ < 310 нм).
Реакции разрушения озона:





























