- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по физике на тему Количество теплоты в термодинамике (11 класс)
Содержание
- 2. Цели урока:Повторить основные формулы.Научиться применять полученные знания
- 3. Основные формулы2. Внутренняя энергияУравнение состояния идеальногогаза (Менделеева – Клапейрона)одноатомного газадвухатомного газа3. Работа газа4. Работа внешних сил
- 4. const
- 6. 5. Количество теплотыпри нагревании и охлаждениипри горениипри плавлении и кристаллизации при парообразованиии конденсацииПовторениеОсновные формулы
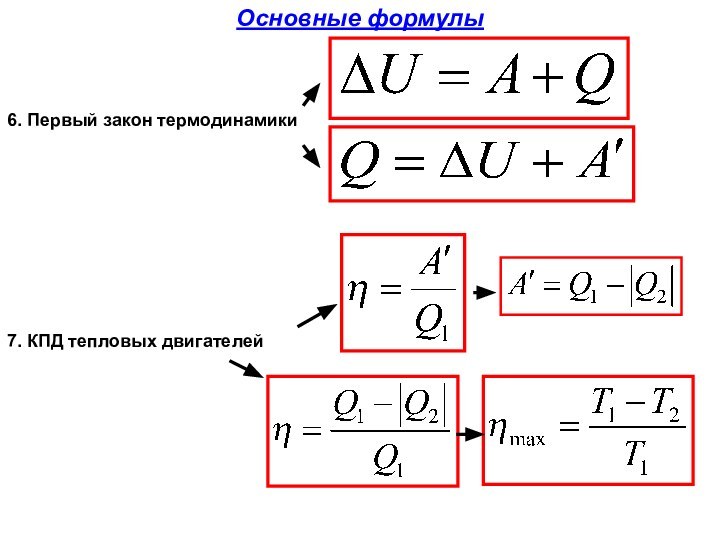
- 7. 6. Первый закон термодинамики7. КПД тепловых двигателейОсновные формулы
- 8. Задача 1. Идеальный газ переходит из состояния
- 9. Задача 2. Найти работу тепловой машины за
- 10. Задача 3. Какую работу – положительную или
- 11. Задача 4. В сосуд, содержащий воду массой
- 12. Задача 5. Какова внутренняя энергия 5 моль
- 13. Задача 6. В стальном баллоне находится гелий
- 14. Задача 7. Какова внутренняя энергия гелия, заполняющего
- 15. Задача 8. На рисунке приведён график зависимости
- 16. Задача 9. Какую работу совершает идеальный газ
- 17. Задача 10. Для приготовления ванны вместимостью 200
- 18. Решение.Количество теплоты, полученное холодной водой:Количество теплоты, отданное
- 19. Запишем уравнение теплового баланса:илиПреобразуем выражение и выразим конечную температуру t.Ответ: t = 57 0C
- 20. Задача 11. При изотермическом расширении идеальным газом
- 21. Задача 12. В закрытом баллоне находится газ.
- 22. Задача 13. Для изобарного нагревания газа, количество
- 23. Задача 14. Тепловой двигатель получает от нагревателя
- 24. Задача 15. Идеальная тепловая машина получает от
- 25. Задача 16. Какое максимальное теоретически возможное значение
- 26. Задача 17. В паровой турбине расходуется дизельное
- 27. Желаю успеха в решении задач!
- 28. Скачать презентацию
- 29. Похожие презентации





















Слайд 2
Цели урока:
Повторить основные формулы.
Научиться применять полученные знания для
решения задач.
слайды, ЭУ 10 кл.
Слайд 3
Основные формулы
2. Внутренняя энергия
Уравнение состояния идеального
газа (Менделеева –
Клапейрона)
одноатомного газа
двухатомного газа
3. Работа газа
4. Работа внешних сил
Слайд 6
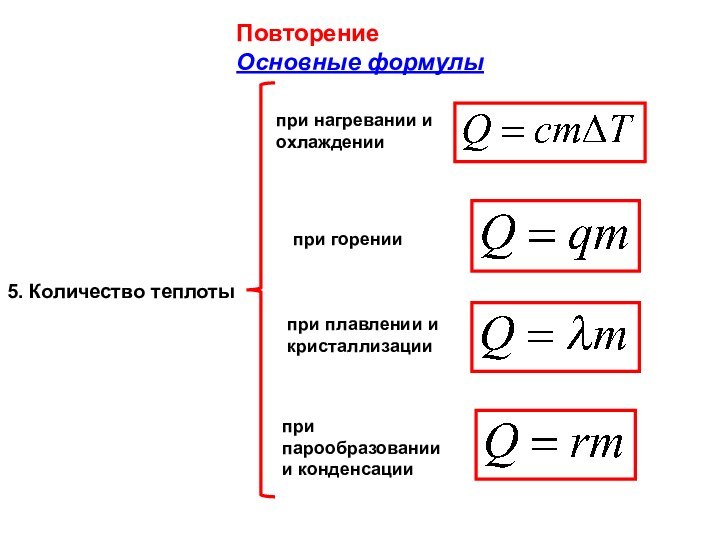
5. Количество теплоты
при нагревании и охлаждении
при горении
при плавлении
и
кристаллизации
при
парообразовании
и конденсации
Повторение
Основные формулы
Слайд 8 Задача 1. Идеальный газ переходит из состояния 1
в состояние 4 так, как показано на рисунке. Вычислите
работу, совершаемую газом.Дано:
Найти: А‘ - ?
Решение.
Ответ: А' = 2,4 кДж.
Слайд 9
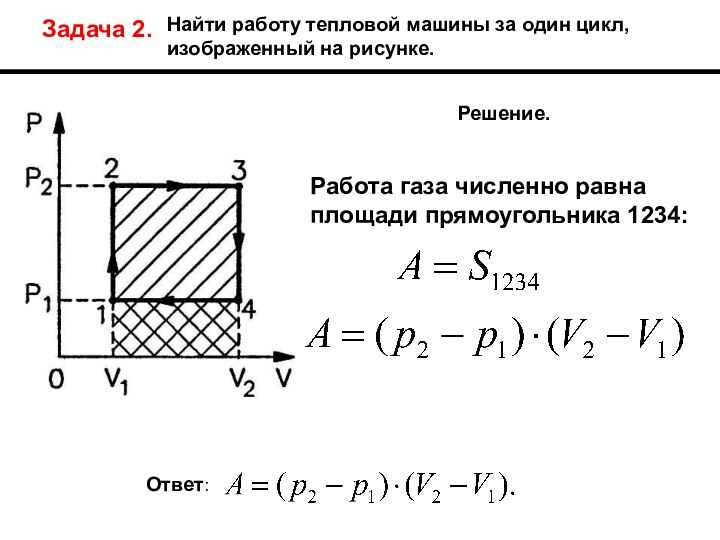
Задача 2.
Найти работу тепловой машины за один
цикл,
изображенный на рисунке.
Решение.
Работа газа численно равна
площади прямоугольника
1234:Ответ:
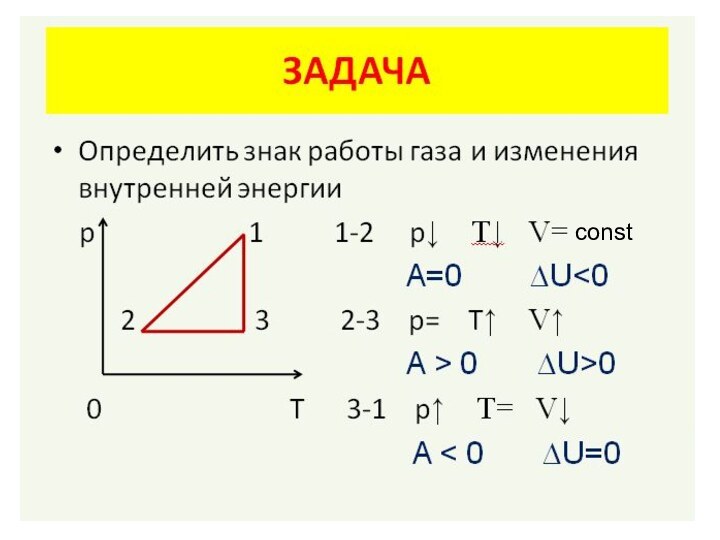
Слайд 10 Задача 3. Какую работу – положительную или отрицательную
–
совершает газ за один цикл (см. рисунок)? На
каких участках количество теплоты поглощается, отдаётся?
Решение.
Перенесём этот график на диаграмму р(V).
1-2: T=const, p↑ → V↓ - изотермическое сжатие.
2-3: p=const, T↑ → V↑ - изобарное расширение.
3-1: p↓ и T↓ → V=const – изохорное охлаждение.
С помощью диаграммы р(V) определим работу газа.
А = рΔV.
Работа равна площади фигуры, ограниченной графи-
ком процесса, осью OV и прямыми V=V1 и V=V2.
Таким образом за один цикл газ совершает
положительную работу.
Газ поглощает количество теплоты на участке 2-3 (при расширении), отдаёт количество теплоты при сжатии – участок 1-2 и при охлаждении – участок 3-1.
Ответ: А' > 0; Q23 > 0; Q12 < 0; Q31 < 0.
Слайд 11 Задача 4. В сосуд, содержащий воду массой 1,5
кг при температуре
15 0С, впускают водяной пар массой 200
г при температуре 100 0С. Какая общая температура установится после конденсации пара?
Дано: “СИ” Решение.
m1 = 1,5 кг
m2 = 200 г 0,2 кг
t1 = 15 0C 288 К
t2 = 100 0C 373 К
c = 4200 Дж/(кг∙К)
r = 2,3∙106 Дж/кг
t - ?
100 0С
15 0С
t
Q1
Q2
Q3
Количество теплоты, выделившееся
при конденсации пара:
Количество теплоты, выделившееся при охлаждении воды, полученной из пара:
Количество теплоты, полученное
холодной водой:
Слайд 12 Задача 5. Какова внутренняя энергия 5 моль кислорода
при 10 0С?
Дано:
“СИ”ν = 5 моль
t = 10 0C 283 K
R = 8,31 Дж/(моль К)
U - ?
Решение.
Кислород О2 – двухатомный газ.
- количество вещества.
Ответ: U = 1,04 кДж
Слайд 13 Задача 6. В стальном баллоне находится гелий массой
0,5 кг при температуре 10 0С. Как изменится внутренняя
энергия гелия, если его температура повысится до 30 0С?
Дано: “СИ” Решение.
m = 0,5 кг
t1 = 10 0С T1 = 283 K
t2 = 30 0C T2 = 303 K
M = 4*10-3 кг/моль
R = 8,31 Дж/(моль К)
ΔU - ?
Найдём изменение внутренней энергии:
Ответ: ΔU =31,2 Дж.
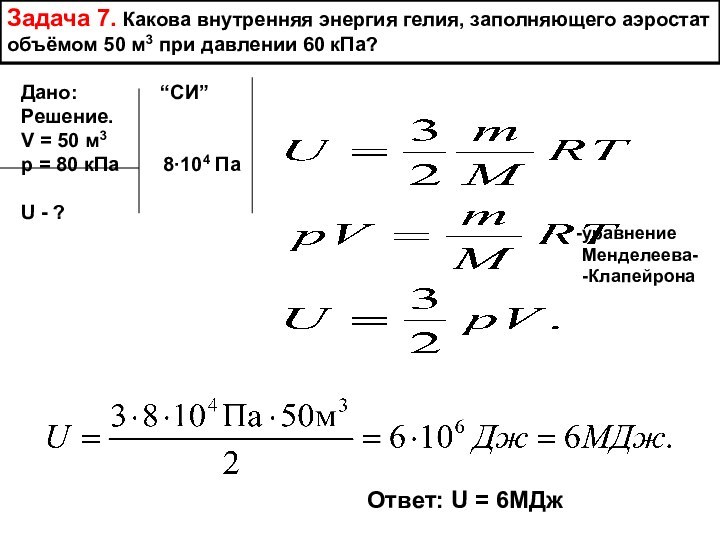
Слайд 14 Задача 7. Какова внутренняя энергия гелия, заполняющего аэростат
объёмом 50 м3 при давлении 60 кПа?
Дано:
“СИ” Решение.V = 50 м3
р = 80 кПа 8∙104 Па
U - ?
уравнение
Менделеева-
-Клапейрона
Ответ: U = 6МДж
Слайд 15 Задача 8. На рисунке приведён график зависимости давления
газа от объёма. Найдите работу газа при расширении.
Дано:
Найти: А'
-?Решение.
Газ расширяется изобарно, поэтому работа газа:
А' = pΔV = p(V2 – V1).
Значения р, V1 и V2 найдём из графика:
р = 7∙105 Па
V1 = 2∙10-3 м3
V2 = 9∙10-3 м3. Тогда:
Ответ: А' = 4,9 кДж
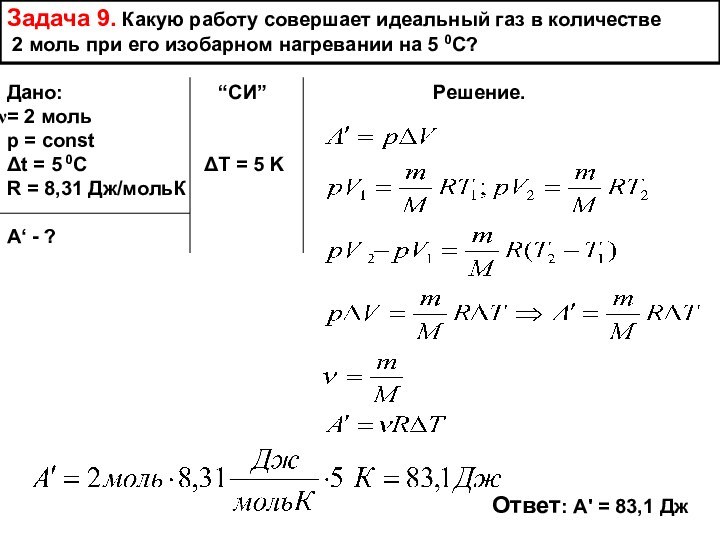
Слайд 16 Задача 9. Какую работу совершает идеальный газ в
количестве
2 моль при его изобарном нагревании на 5
0С?Дано: “СИ” Решение.
= 2 моль
p = const
Δt = 5 0C ΔT = 5 K
R = 8,31 Дж/мольК
А‘ - ?
Ответ: А' = 83,1 Дж
Слайд 17 Задача 10. Для приготовления ванны вместимостью 200 л
смешали холодную воду при температуре 10 0С с горячей
водойпри температуре 60 0С. Какие объёмы той и другой воды надо взять,
чтобы температура установилась 40 0С?
Дано: “СИ”
V = 200 л 0,2 м3
t1хол = 10 0С T1хол = 283 К
t2гор = 60 0С T2гор = 333 K
t = 40 0C T = 313 K
ρ = 103 кг/м3
с = 4200Дж/(кгК )
V1 - ?
V2 - ?
Примечание: холодную и горячую воду можно
рассматривать как замкнутую систему тел, так как
при данных условиях нет теплообмена с
окружающей средой.
Слайд 18
Решение.
Количество теплоты, полученное холодной водой:
Количество теплоты, отданное горячей
водой:
или
Уравнение теплового баланса:
Ответ: V1 = 80 л
V2 = 120 л
Слайд 19
Запишем уравнение теплового баланса:
или
Преобразуем выражение и выразим конечную
температуру t.
Ответ: t = 57 0C
Слайд 20
Задача 11. При изотермическом расширении идеальным газом
совершена
работа 15 кДж. Какое количество теплоты сообщено газу?
Дано:
“СИ” Решение.А' = 15 кДж 1,5∙104 Дж
Т = const
Q - ?
По I закону термодинамики:
При изотермическом процессе (Т = const)
внутренняя энергия газа не меняется, то есть
Тогда газ совершает механическую работу за счёт сообщенного ему
количества теплоты:
Таким образом, газу сообщено количество теплоты, равное
Ответ: Q = 15 кДж.
Слайд 21 Задача 12. В закрытом баллоне находится газ. При
охлаждении его внутренняя энергия уменьшилась на 500 Дж. Какое
количество теплоты отдал газ? Совершил ли он работу?Дано: Решение.
ΔU = - 500 Дж
Q - ?
А‘ - ?
Газ находится в закрытом баллоне, следовательно,
объём газа не меняется, то есть V = const и ΔV = 0.
Газ работу не совершает, так как
По I закону термодинамики
Таким образом, при изменении внутренней энергии газ отдаёт
количество теплоты, равное (знак «-» показывает,
что газ выделяет количество теплоты).
Ответ: Q = -500 Дж; А' = 0.
Слайд 22
Задача 13. Для изобарного нагревания газа, количество вещества
которого
400 моль, на 300 К ему сообщили количество теплоты
5,4 МДж. Определите работу газа и изменение его внутренней энергии.Дано: “СИ” Решение.
р = const
ν = 400 моль
ΔТ = 300 К
Q = 5,4 МДж 5,4∙106 Дж
А‘ - ?
ΔU - ?
Запишем первый закон термодинамики:
Работа газа при постоянном давлении:
Изменение внутренней энергии системы:
Ответ: А' = 1МДж; ΔU = 4,4 МДж.
Слайд 23 Задача 14. Тепловой двигатель получает от нагревателя за
одну
секунду 7200 кДж теплоты и отдаёт холодильнику 5600 кДж.
КаковКПД теплового двигателя?
Дано: “СИ” Решение.
Q1 = 7200 кДж 7,2 ∙ 106 Дж
Q2 = 5600 кДж 5,6 ∙ 106 Дж
η - ?
По определению КПД тепловой машины:
Ответ: η = 22%.
Слайд 24
Задача 15. Идеальная тепловая машина получает от нагревателя,
температура которого 500 К, за один цикл 3360 Дж
теплоты. Найтиколичество теплоты, отдаваемое за один цикл холодильнику, температура которого 400 К. Найти работу машины за один цикл.
Дано:
Т1 = 500 К
Q1 = 3360 Дж
Т2 = 400 К
Q2 - ?
A‘ -?
Решение.
или
Работа машины за один цикл:
;
Ответ: Q2 = 2688 Дж; А' = 672 Дж.
Слайд 25 Задача 16. Какое максимальное теоретически возможное значение КПД
может иметь турбина, в которой используют пар с температурой
600 0С, а отвод тепла осуществляется с помощью речной воды, обеспечивающей холодильнику температуру 27 0С? Каковы основные пути повышения КПД тепловых машин?Дано: “СИ” Решение.
t1 = 600 0C 873 K
t2 = 27 0C 300 K
η - ?
Основной способ увеличения КПД – повышение температуры
нагревателя Т1 и понижение температуры холодильника Т2.
Ответ: ηмах = 66%.
Слайд 26 Задача 17. В паровой турбине расходуется дизельное топливо
массой 0,35 кг на 1 кВт∙ч мощности. Температура поступающего
в турбину пара 250 0С, температура холодильника 30 0С. Вычислите фактический КПД турбины и сравните его с КПД идеальной тепловой машины, работающей при тех же температурных условиях.Дано: “СИ” Решение.
А‘ = 1 кВт∙ч 1∙103 Вт ∙ 3600с = 3,6 ∙ 106 Дж
m = 0,35 кг
q = 42∙106 Дж/кг
t1 = 250 0С T1 = 523 K
t2 = 30 0C T2 = 303 K
η - ?
ηmax - ?
Для реальной тепловой машины:
где q – удельная теплота сгорания
топлива.
КПД идеальной
тепловой машины: