Слайд 2
Краткие рекомендации по использованию презентации
Учебный предмет: физика
Возрастная
группа (класс): учащиеся 10 классов
Материал презентации сопровождает урок
изучения нового материала по теме «Уравнение состояния идеального газа»
Цель: вывести уравнение Клапейрона-Менделеева и применить полученные знания при решении задач.
1 слайд – Титульный
2 слайд – Краткие рекомендации
3 слайд – Тема урока
4-23 слайды – Тестовая работа (вхождение в тему урока)
24-35 слайды – Актуализация знаний
36 слайд – Формулировка цели деятельности учащихся на уроке
37-40 слайды – Открытие нового знания
41-43 слайд –Первичное закрепление, самостоятельная работа с самопроверкой по эталону
44 слайд –Домашнее задание
45-47 слайды – Рефлексия деятельности
48 слайд – Список литературы и Интернет–ресурсов
Слайд 3
Уравнение состояния идеального газа
Слайд 4
Проверочный тест
Внимательно прочитайте вопрос, выберите правильный ответ
и нажмите на него.
Удачи!
Слайд 5
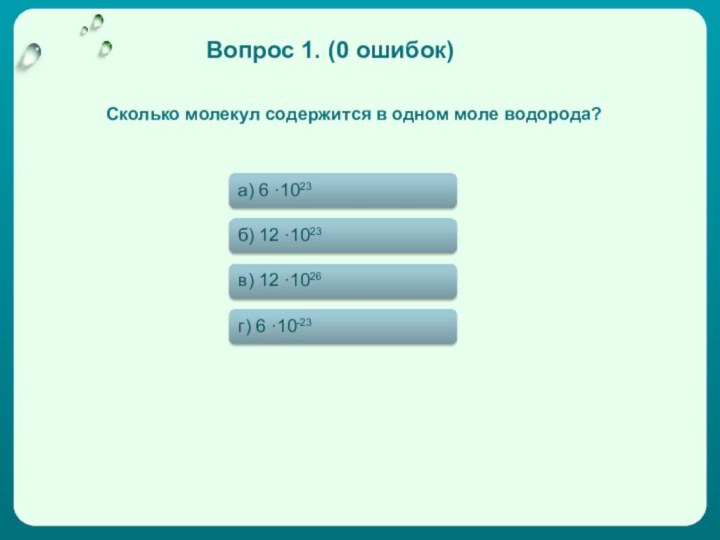
Сколько молекул содержится в одном моле водорода?
Вопрос 1.
(0 ошибок)
а) 6 ·1023
б) 12 ·1023
в) 12 ·1026
г) 6
·10-23
Слайд 6
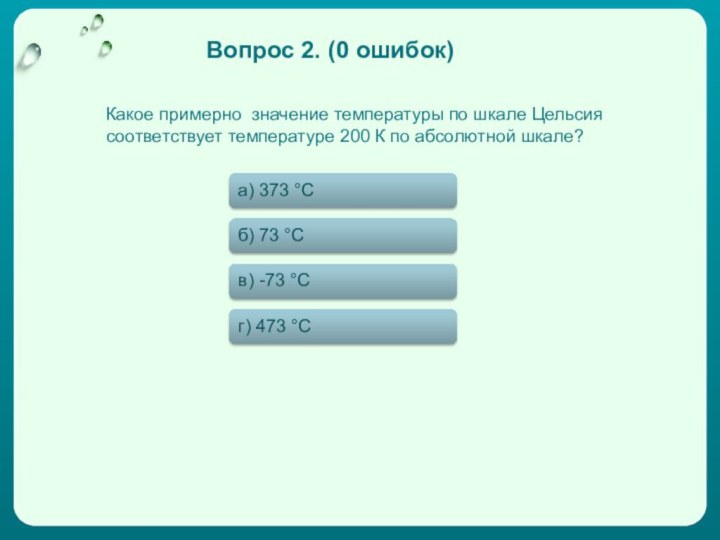
Какое примерно значение температуры по шкале Цельсия соответствует
температуре 200 К по абсолютной шкале?
Вопрос 2. (0 ошибок)
а)
373 °С
б) 73 °С
в) -73 °С
г) 473 °С
Слайд 7
Какое примерно значение температуры по шкале Цельсия соответствует
температуре 200 К по абсолютной шкале?
Вопрос 2. (1 ошибка)
а)
373 °С
б) 73 °С
в) -73 °С
г) 473 °С
Слайд 8
В молекулярной физике используется понятие «идеальный газ». Это
понятие применимо тогда, когда можно пренебречь
Вопрос 3. (0 ошибок)
а)
Потенциальной энергией частиц
б) Кинетической энергией частиц
в) Массой частиц
г) Потенциальной энергией частиц и их размерами
Слайд 9
В молекулярной физике используется понятие «идеальный газ». Это
понятие применимо тогда, когда можно пренебречь
Вопрос 3. (1 ошибка)
а)
Потенциальной энергией частиц
б) Кинетической энергией частиц
в) Массой частиц
г) Потенциальной энергией частиц и их размерами
Слайд 10
В молекулярной физике используется понятие «идеальный газ». Это
понятие применимо тогда, когда можно пренебречь
Вопрос 3. (2 ошибки)
а)
Потенциальной энергией частиц
б) Кинетической энергией частиц
в) Массой частиц
г) Потенциальной энергией частиц и их размерами
Слайд 11
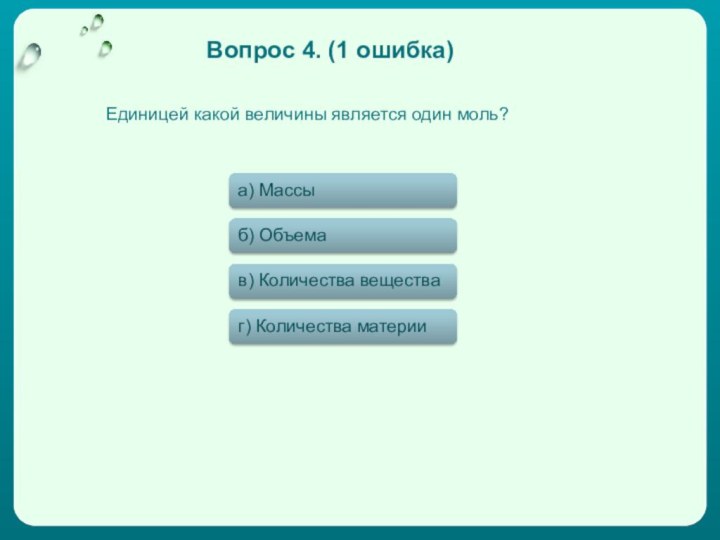
Единицей какой величины является один моль?
Вопрос 4. (0
ошибок)
а) Массы
б) Объема
в) Количества вещества
г) Количества материи
Слайд 12
Единицей какой величины является один моль?
Вопрос 4. (1
ошибка)
а) Массы
б) Объема
в) Количества вещества
г) Количества материи
Слайд 13
Единицей какой величины является один моль?
Вопрос 4. (2
ошибки)
а) Массы
б) Объема
в) Количества вещества
г) Количества материи
Слайд 14
Единицей какой величины является один моль?
Вопрос 4. (3
ошибки)
а) Массы
б) Объема
в) Количества вещества
г) Количества материи
Слайд 15
Каким выражением определяется средняя кинетическая энергия поступательного движения
молекулы идеального газа?
Вопрос 5. (0 ошибок)
a) 2/3nE
б) nkT
в) 3/2kT
г)
1/2nm0v
Слайд 16
Каким выражением определяется средняя кинетическая энергия поступательного движения
молекулы идеального газа?
Вопрос 5. (1 ошибка)
a) 2/3nE
б) nkT
в) 3/2kT
г)
1/2nm0v
Слайд 17
Каким выражением определяется средняя кинетическая энергия поступательного движения
молекулы идеального газа?
Вопрос 5. (2 ошибки)
a) 2/3nE
б) nkT
в) 3/2kT
г)
1/2nm0v
Слайд 18
Каким выражением определяется средняя кинетическая энергия поступательного движения
молекулы идеального газа?
Вопрос 5. (3 ошибки)
a) 2/3nE
б) nkT
в) 3/2kT
г)
1/2nm0v
Слайд 19
Каким выражением определяется средняя кинетическая энергия поступательного движения
молекулы идеального газа?
Вопрос 5. (4 ошибки)
a) 2/3nE
б) nkT
в) 3/2kT
г)
1/2nm0v
Слайд 24
И все доступно,
Все открыто,
И ничего еще не жаль.
И
надо мной плывет, как рыба,
Огромный сонный дирижабль!
А. Жигулин
Слайд 25
Каким газом наполняют дирижабли?
Слайд 26
Гелий ( He) – это инертный одноатомный газ,
без цвета, вкуса и запаха.
В обычных условиях гелий по
своим свойствам близок к идеальному газу
Слайд 27
Идеальный газ – это газ, взаимодействия между молекулами
которого пренебрежимо мало.
Что называется идеальным газом?
Слайд 28
От чего зависит давление газа?
от концентрации молекул,
n
от температуры,
T
Слайд 29
Как зависит давление идеального газа
от n и
T?
p=nkT
Слайд 30
Концентрация – это число частиц в единице объема
[n]
= 1 м-3
Что такое концентрация?
Слайд 31
Какая формула позволяет вычислить число молекул N?
Слайд 32
Это число атомов
в 1 моль вещества
NA=6,02·1023 моль-1
Что называют постоянной
Авогадро?
Слайд 33
Чему равна постоянная Больцмана?
Слайд 34
p - давление
V - объем
T - температура
Макроскопические параметры,
характеризующие состояние системы:
Слайд 35
Уравнение состояния –
это уравнение, определяющее связь температуры,
объема и давления тел.
Слайд 36
Сформулируйте
цель вашей деятельности,
исходя из определения уравнения
состояния.
Цель:
Вывести закон, связывающий между собой макроскопические параметры.
Слайд 37
План работы
Запишите формулу зависимости давления газа от
концентрации и температуры;
В уравнение поставьте значение концентрации и запишите
полученные результаты;
Перенесите все макропараметры влево;
Запишите формулу для числа частиц и подставьте ее в выражение, полученное Клапейроном;
В правой части NA и k. Их произведение назвали универсальной газовой постоянной и обозначили R. (Вычислите значение R и выведите единицу измерения R);
Подставьте R в предыдущую формулу;
Оставьте в левой части только p и V;
Сформулируйте уравнение состояния идеального газа.
Слайд 38
Связь давления идеального газа и температуры
Число частиц
Универсальная газовая
постоянная
Уравнение состояния идеального газа
R=6,02·1023моль-1·1,38 ·1023Дж/К = 8,31 Дж/(К·моль)
Слайд 39
Проанализируйте полученные уравнения:
М – молярная масса
Какая форма уравнения
состояния содержит больше информации: уравнение Клапейрона или уравнение Менделеева-Клапейрона?
Содержит
больше информации уравнение Менделеева-Клапейрона, потому что оно записывается для газа произвольной массы, а уравнение Клапейрона – для газа данной массы.
Назовите единственную в этом уравнении величину, зависящую от рода газа?
Слайд 40
Знание уравнения состояния позволяет определить:
Одну из величин, характеризующих
состояние, например температуру, если известны две другие величины (используют
в термометрах);
Как будут происходить в системе различные процессы при определенных внешних условиях;
Как меняется состояние системы, если она совершает работу или получает теплоту от окружающих тел.
Слайд 41
Задача 1. Определите массу воздуха в классе, где
вы занимаетесь, при температуре 20 oС и нормальном атмосферном
давлении. (Молярную массу воздуха принять равной 0,029 кг/моль).
!!! Вам понадобится для измерения объема комнаты рулетка.
СИ
293 К
Дано:
t= 20 °C
рo = 101325 Па
М = 0,029 кг/моль
m - ?
Слайд 42
Задача 2. Плотность некоторого газообразного вещества
равна 2,5
кг/м3 при температуре 10 oС и нормальном атмосферном давлении.
Найдите молярную массу этого вещества.
СИ
283 К
Дано:
t= 10 °C
рo = 101325 Па
ρ =2,5 кг/м3
М - ?
Ответ: 0,058 кг/моль.
Слайд 43
Задача 3. Объем 1 моль водорода в сосуде
при температуре Т и давлении р равен V1. Объем
4 моль водорода при том же давлении и температуре 2Т равен V2. Чему равно отношение V2/V1? (Водород считать идеальным газом.)
Дано:
р1=р2=p
Т2=2Т1
ν2=4 ν1
Найти:
Ответ: 8
Слайд 44
Домашнее задание
§68, упр.13(6,7)
по желанию: составить тест по теме
«Уравнение состояния идеального газа»
(не менее пяти заданий)
Слайд 45
Сегодня на уроке я …
Деятельность, выполненная мною успешно…
У
меня на уроке получилось…
Мне было трудно…
Теперь я знаю …
Поставленная
на уроке цель …
Теперь я могу…
Подведем итоги
Слайд 46
Во всем мне хочется дойти
До самой сути
В работе,
в поисках пути,
В сердечной смуте.
До сущности прошедших дней,
До их
причины,
До оснований, до корней,
До сердцевины…
Б.Пастернак























![Уравнение состояния идеального газа Концентрация – это число частиц в единице объема[n] = 1 м-3Что такое концентрация?](/img/tmb/6/591274/2c8d61dd504fe95b3023c37a3d35899a-720x.jpg)