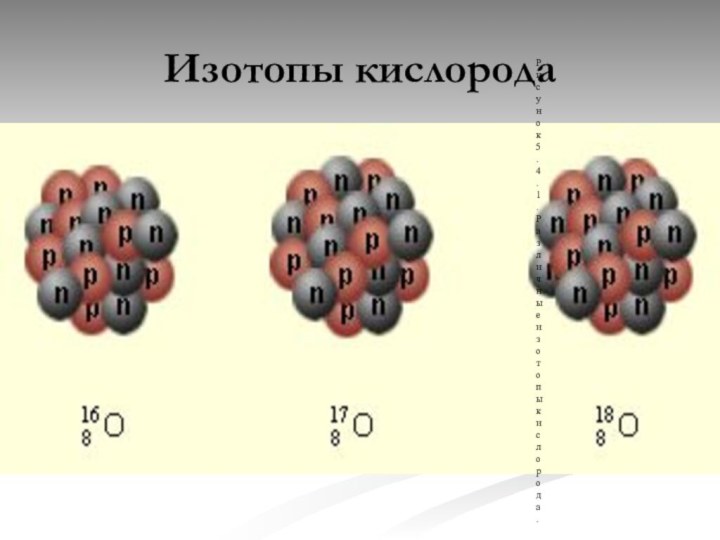
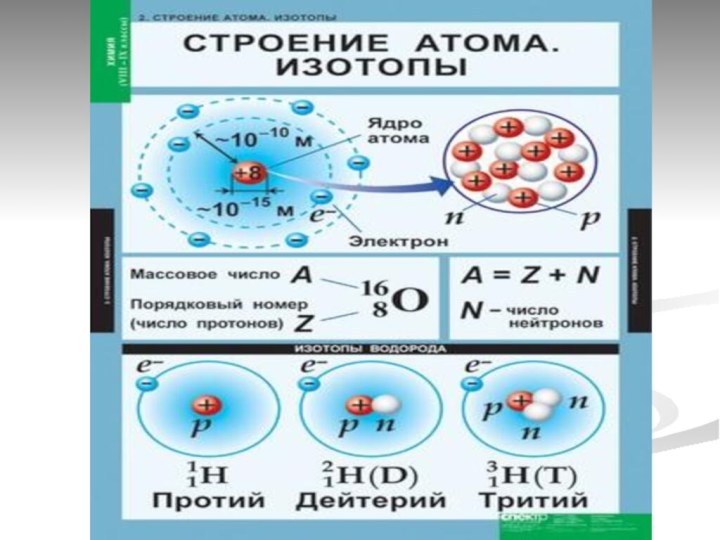
разновидности одного химического элемента, у которых ядра атомов содержат
одинаковое число протонов и поэтому занимают одно и тоже место в периодической системе Менделеева.Изотопы - вещества тождественные по химическим свойствам, но имеющие разные радиоактивные свойства и разную относительную атомную массу.