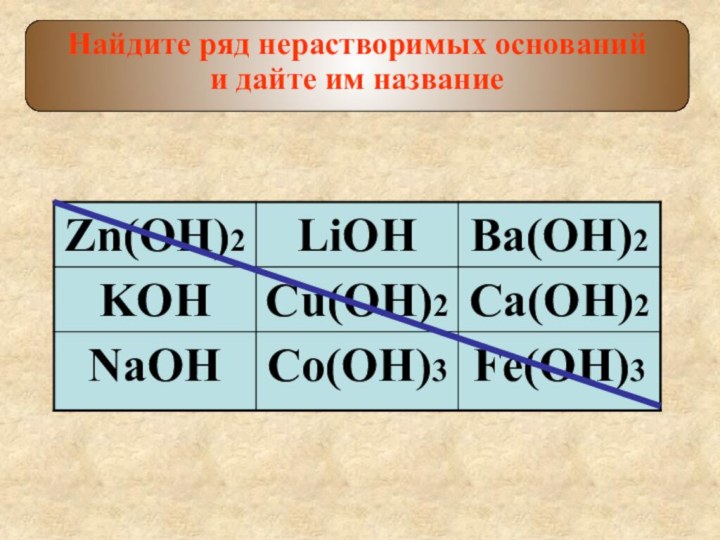
б) HC1 в)
CuC12 г) SO3
2. Лакмус в растворе, полученном при взаимодействии оксида серы (IV) с водой:
а) синий б) красный в) фиолетовый г) малиновый
3. С раствором серной кислоты взаимодействует:
а) оксид магния в) оксид фосфора
б) оксид углерода г) сера
4. Соляная кислота не взаимодействует с металлом:
а) алюминием б) железом в) серебром г) цинком
5. Пара ионов, которая может одновременно находится в растворе:
а) H+ и SiO2 б) Cu 2+ и ОН- в) Н+ и SO42- г) Ag+ и C1-
6. Пара веществ взаимодействующих друг с другом:
а) H2SO4 и SiO2 в) Сu и H3PO4
б) CuO и Na2O г) НС1 и NaOH
ПРОВЕРЬ СЕБЯ