моделировании электронного строения молекул H2O, координационно-связанных с атомом Ti(III),
выполняющим роль акцептора электронной плотности.Соответственно, решались следующие задачи:
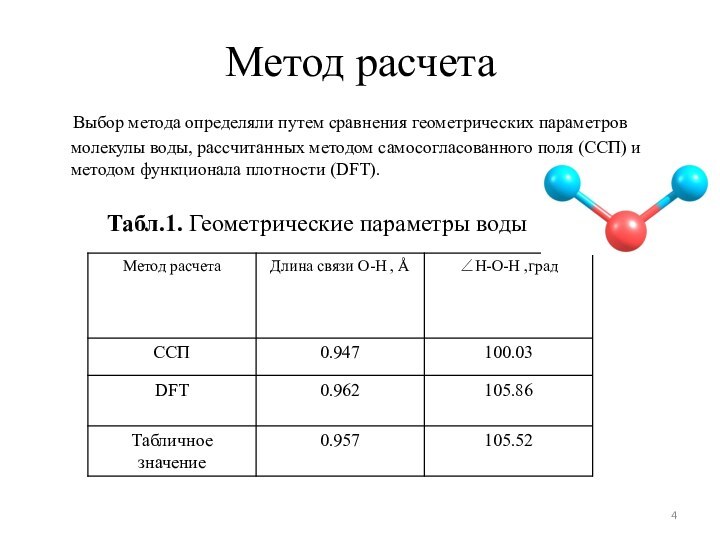
выбор метода расчета, наиболее точно передающего геометрическую структуру молекулы H2O;
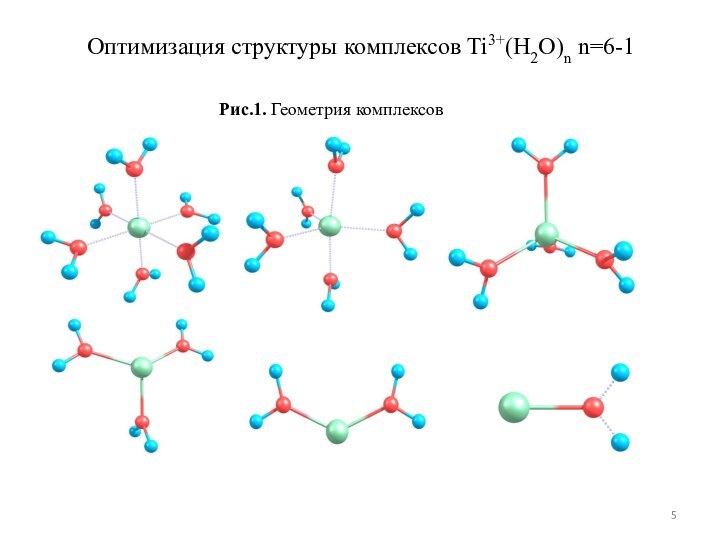
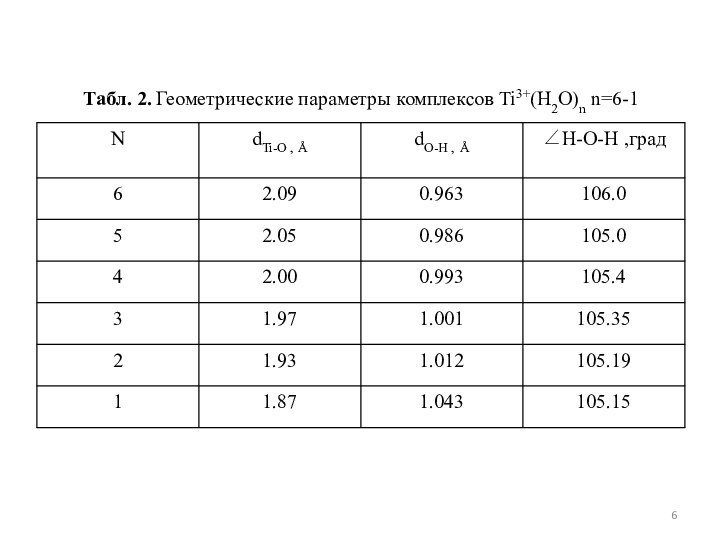
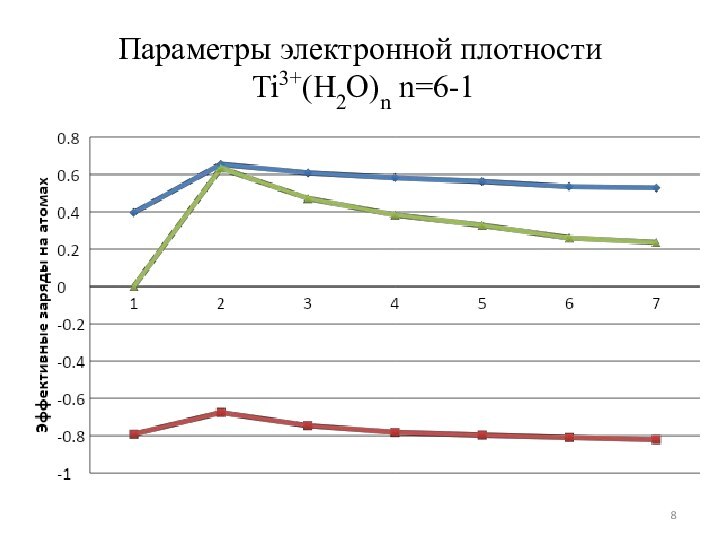
расчет в едином приближении модельных структур Ti(III)·nH2O (n=1-6);
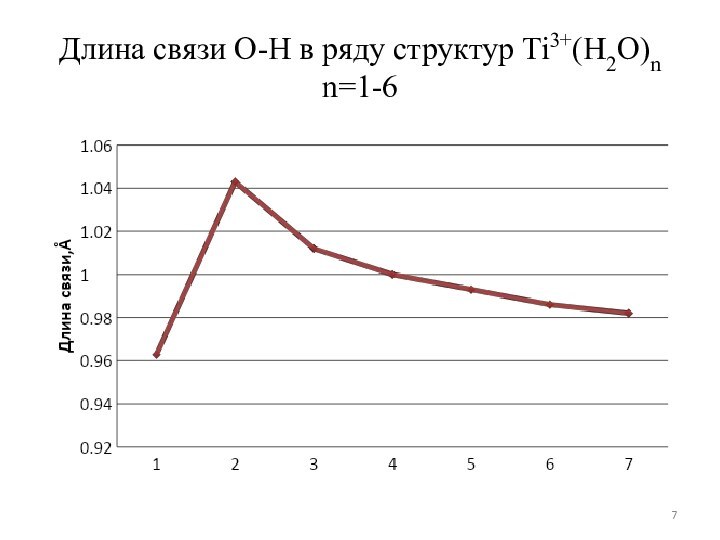
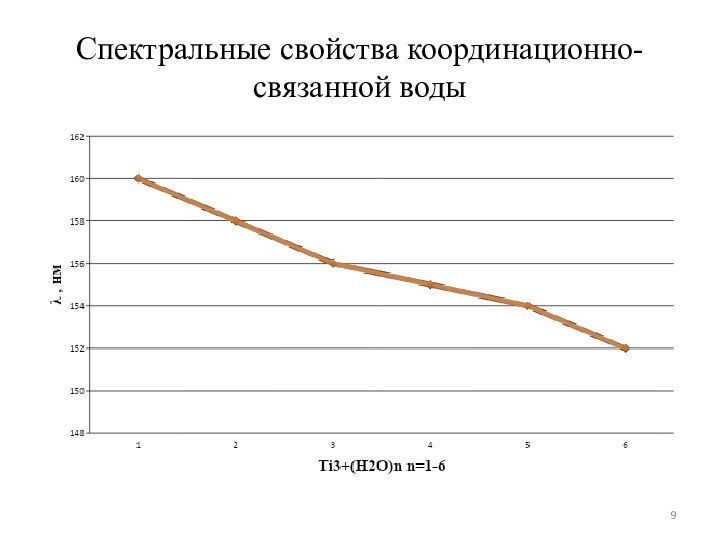
анализ полученных результатов с целью определения степени возмущения электронной структуры молекулы H2O и соответствующего смещения области ее фоточувствительности.