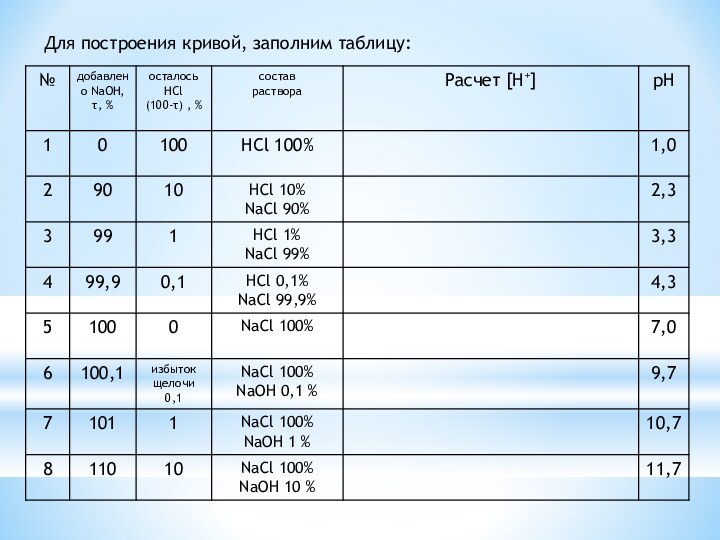
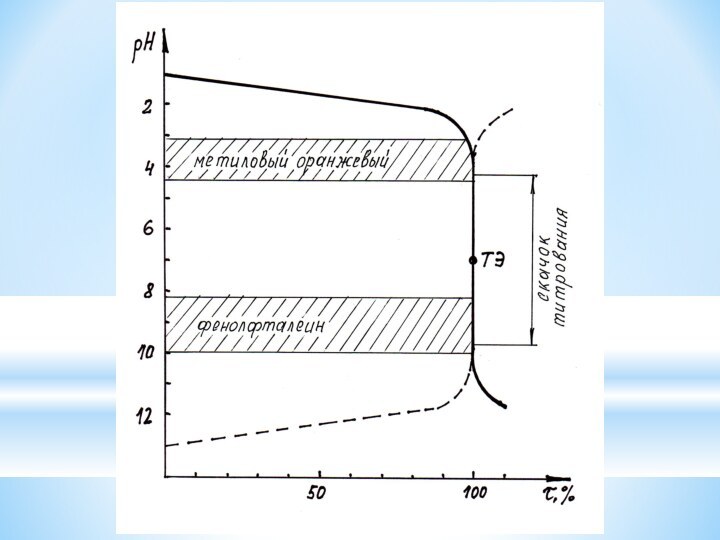
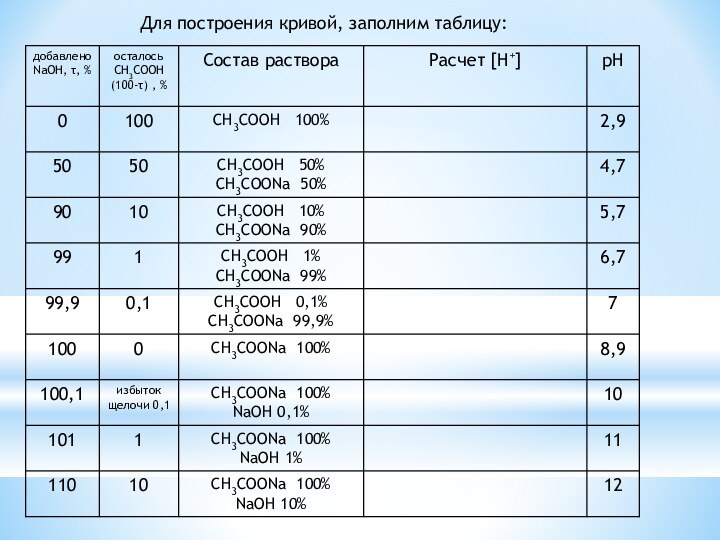
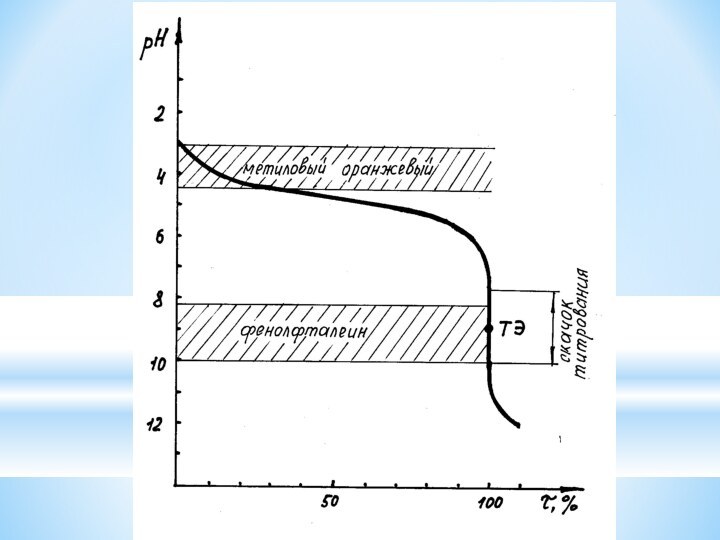
рН = f (V) или от степени оттитрованности рН
= f (τ)Степень оттитрованности (τ) – это отношение объема
прибавленного титранта к объему титранта, необходимого для достижения точки эквивалентности
Расчет кривых титрования необходим для правильного
выбора индикатора