- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Жёсткость воды и здоровье человека
Содержание
- 2. Вода .Одно из самых распространённых веществ в
- 3. Без воды невозможно существование живых организмов. Около
- 4. В природных водах постоянно присутствуют ионы Ca2+
- 5. Общая жёсткость воды определяется содержанием в ней
- 6. Жёсткость бывает временной и постоянной. Временную жёсткость
- 7. Постоянная жёсткость обусловливаются присутствием в природной воде растворимых хлоридов и сульфатов кальция и магния.
- 8. По содержанию в воде ионов Ca2+ и
- 9. Жёсткость воды в различных городах разная. И
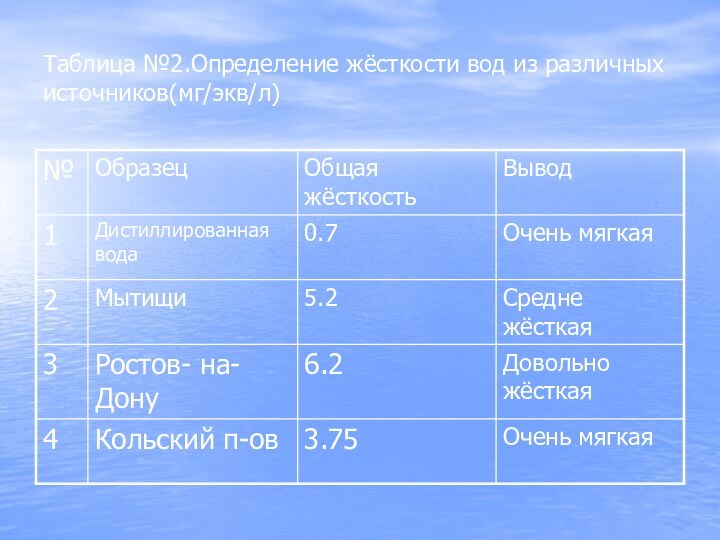
- 10. Таблица №2.Определение жёсткости вод из различных источников(мг/экв/л)
- 11. В последнее время появилось множество смягчителей воды,
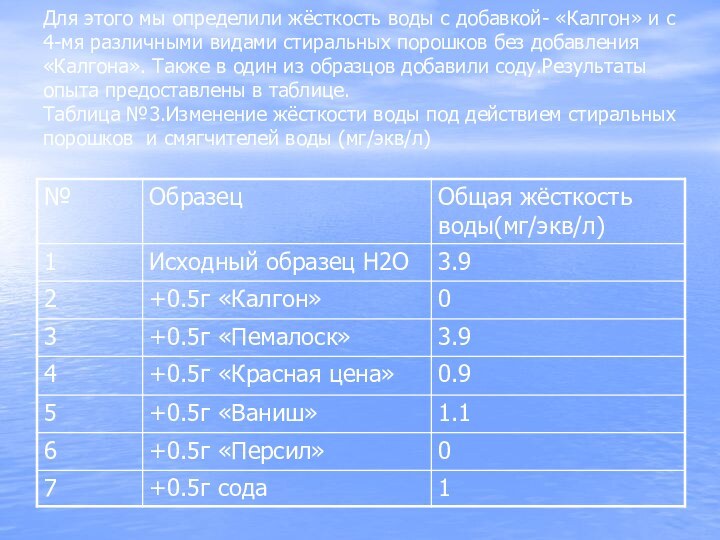
- 12. Для этого мы определили жёсткость воды с
- 13. Как видно из полученных данных «Калгон» действительно
- 14. Во многих семьях используют фильтры для очистки
- 15. Таблица№4. Изменение жёсткости воды под действием фильтров(мг/экв/л)
- 16. Скачать презентацию
- 17. Похожие презентации
Вода .Одно из самых распространённых веществ в природе. Гидросфера занимает 71% поверхности Земли. Воде принадлежит важнейшая роль в геологической истории планеты. Она- обязательный компонент практически всех технологических процессов как промышленных так сельско- хозяйственных.














Слайд 3 Без воды невозможно существование живых организмов. Около 65%
человеческого тела составляет вода
А какую красоту она нам
подарила! Водопады, гейзеры, океаны, моря, реки- за всё это мы должны благодарить воду. Дождь, снег, град- всё это вода.Почему же вода из разных источников имеет разный вкус, в ней по разному пенится мыло и на стенках чайников оседает разная накипь?
Слайд 4 В природных водах постоянно присутствуют ионы Ca2+ и
Mg2+, которые обуславливают общую жёсткость. Основной источник их поступления
в воду- растворение пород, содержащих известняки, доломит, гипс, сложные алюмосиликаты. Жёсткая вода образует плотные слои накипи на внутренних стенах паровых котлов и кипятильников, в ней плохо развариваются пищевые продукты, при стирке белья в жёсткой воде расходуется больше мыла.Слайд 5 Общая жёсткость воды определяется содержанием в ней ионов
Ca2+ и Mg2+.В сумме карбонатная и некарбонатная жёсткость воды
даёт жёсткость общую.Слайд 6 Жёсткость бывает временной и постоянной. Временную жёсткость обуславливают
в растворимом виде гидрокарбонаты металлов, остающихся в воде. При
кипячении воды гидрокарбонаты разлагаются и выпадают в осадок. Нарастания таких осадков на стенках паровых котлов, труб неминуемо ведёт к авариям. Это является серьёзной причиной необходимости устранения жёсткости воды.Слайд 7 Постоянная жёсткость обусловливаются присутствием в природной воде растворимых
хлоридов и сульфатов кальция и магния.
Слайд 8 По содержанию в воде ионов Ca2+ и Mg2+
воды делятся на следующие группы: Таблица№1.Типы вод в зависимости
от содержания ионов Ca2+ и Mg2+ («Основы химического анализа»В. И. Астафуров).Слайд 9 Жёсткость воды в различных городах разная. И чтобы
это проверить мы собрали образцы водопроводной воды из 3-ёх
городов России. Естественно что содержание ионов Ca2+ и Mg2+ в водопроводной воде отражает их содержание в природных водах. После анализа мы получили следующие данныеСлайд 11 В последнее время появилось множество смягчителей воды, защищающих
стиральные машины от накипи. Одновременно производители стиральных порошков ввели
компоненты предотвращающие образование накипи, в состав большинства стиральных препаратов.Так стоит ли, покупая стиральный порошок, приобретать ещё и смягчитель воды к нему?