Слайд 2
Регенеративной, т. е. с извлечением вещества из адсорбента
и его утилизацией.
Деструктивной, при которой извлеченные из сточных
вод вещества уничтожаются вместе с адсорбентом.
Эффективность адсорбционной очистки достигает 80-95%.
Адсорбцию используют для обезвреживания сточных вод от фенолов, гербицидов, пестицидов, ароматических нитросоединений, ПАВ красителей и др.
Слайд 3
В общем случае процесс адсорбции складывается из трех
стадий:
1) переноса вещества из сточной воды к поверхности
зерен адсорбента (внешнедиффузионная область),
2) собственно адсорбционный процесс,
3) перенос вещества внутри зерен адсорбента (внутридиффузионная область).
Процесс адсорбционной очистки сточной воды ведут при интенсивном перемешивании адсорбента с водой. При смешивании адсорбента с водой используют активный уголь в виде частиц 0,1 мм и меньше. Процесс проводят в одну или несколько ступеней.
Слайд 4
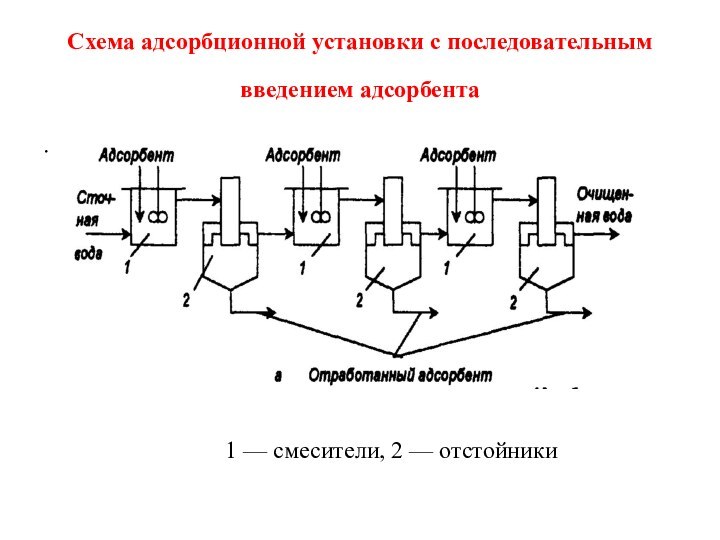
Схема адсорбционной установки с последовательным введением адсорбента
.
1
— смесители, 2 — отстойники
Слайд 5
Расход адсорбента для одноступенчатого процесса определяют из уравнения
материального баланса:
где m — расход адсорбента; Q — объем
сточных вод; Сн и Ск — начальная и конечная концентрации загрязненной сточной воды; а — коэффициент адсорбции
Конечная концентрация загрязнений в сточной воде после очистки в установке с п ступенями рассчитывается по формуле:
где Кm - коэффициент распределения, равный
Слайд 6
где - Ср равновесная концентрация вещества
Регенерация адсорбента.
Адсорбированные вещества из угля извлекают десорбцией насыщенным или перегретым
водяным паром, либо нагретым инертным газом. Температура перегретого пара при этом (при избыточном давлении 0,3-0,6МПа равна 200-300°С, а инертных газов 120-140°С. Расход пара при отгонке легколетучих веществ равен 2,5-3 кг на 1 кг отгоняемого вещества, для высококипящих — в 5-10 раз больше. После десорбции пары конденсируют и вещество извлекают из конденсата.
Слайд 7
Ионный обмен.
Ионообменная очистка применяется для извлечения из
сточных вод металлов (цинка, меди, хрома, никеля, свинца, ртути,
кадмия, ванадия, марганца и др.), а также соединений мышьяка, фосфора, цианистых соединений и радиоактивных веществ. Метод позволяет рекуперировать ценные вещества при высокой степени очистки воды. Ионный обмен широко распространен при обессоливании в процессе водоподготовки.
Слайд 8
Сущность ионного обмена.
Ионный обмен представляет собой процесс
взаимодействия раствора с твердой фазой, обладающей свойствами обменивать ионы,
содержащиеся в ней, на другие ионы, присутствующие в растворе.
Вещества, составляющие эту твердую фазу, носят название — ионитов. Они практически не растворимы в воде.
Те из них, которые способны поглощать из растворов электролитов положительные ионы, называются катионитами, отрицательные ионы — анионитами.
Первые обладают кислотными свойствами, вторые — основными. Если иониты обменивают и катионы, и анионы, их называют амфотерными.
Слайд 9
Поглотительная способность ионитов характеризуется обменной емкостью, которая определяется
числом эквивалентов ионов, поглощаемых единицей массы или объема ионита.
Различают:
1) Полная емкость — это количество поглощаемого вещества при полном насыщении единицы объема или массы ионита
2) Статическая емкость — это обменная емкость ионита при равновесии в данных рабочих условиях.
3) Динамическая обменная емкость — это емкость ионита до "проскока" ионов в фильтрат, определяемая в условиях фильтрации.
Слайд 10
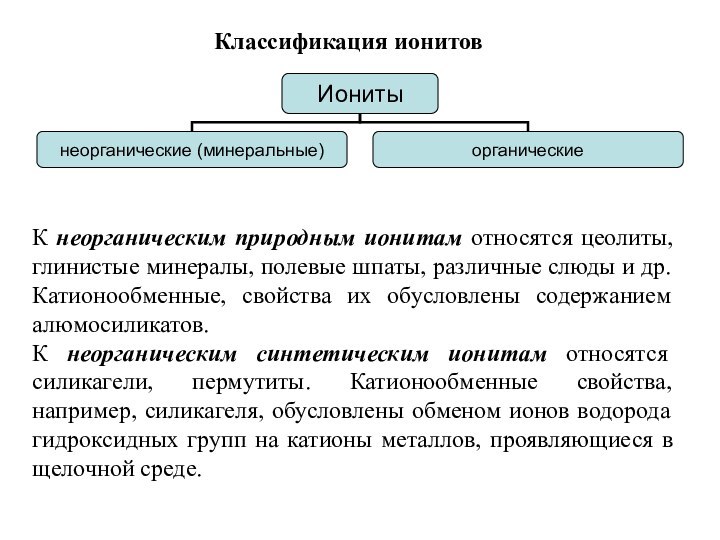
Классификация ионитов
К неорганическим природным ионитам относятся цеолиты, глинистые
минералы, полевые шпаты, различные слюды и др. Катионообменные, свойства
их обусловлены содержанием алюмосиликатов.
К неорганическим синтетическим ионитам относятся силикагели, пермутиты. Катионообменные свойства, например, силикагеля, обусловлены обменом ионов водорода гидроксидных групп на катионы металлов, проявляющиеся в щелочной среде.
Слайд 11
Органические природные иониты — это гуминовые кислоты почв
и углей. Они проявляют слабокислотные свойства.
К органическим искусственным
ионитам относятся ионообменные смолы с развитой поверхностью. Синтетические ионообменные смолы представляют собой высокомолекулярные соединения, углеводородные радикалы которых образуют пространственную сетку с фиксированными на ней ионообменными функциональными группами.
Пространственная углеводородная сетка (каркас) называется матрицей, а обменивающиеся ионы — противоионами. Каждый противоион соединен с противоположно заряженными ионами, называемыми фиксированными или анкерными.
Слайд 12
При сокращенном написании ионита матрицу обозначают в общем
виде (R), а активную группу указывают полностью. Например, сульфокатиониты
записывают как:
RS03H.
где R — матрица,
Н — противоион,
S03 — анкерный ион.
Сильноосновные иониты содержат четвертичные аммониевые основания (R3NOH)
Катиониты в качестве противоионов могут содержать не ионы водорода, а ионы металлов, т. е. находиться в солевой форме. Точно также и аниониты могут находиться в солевой форме, если в качестве противоионов они содержат не ионы гидроксида, а ионы тех или иных кислот.
Слайд 13
Реакция ионного обмена протекает следующим образом:
а) при
контакте с катионитом
RS03H+NaСI= RS03Na + HСI
б) при контакте с
анионитом
ROH+ NaСI= R СI+ NaOH
В общем виде эти реакции можно представить следующим образом:
Реакция идет до установления ионообменного равновесия.
Слайд 14
Процесс переноса вещества может быть представлен в виде
нескольких стадий:
1) перенос ионов А из ядра потока
жидкости к внешней поверхности пограничной жидкой пленки, окружающей зерно ионита;
2) диффузия ионов через пограничный слой;
3) переход иона через границу раздела фаз в зерно смолы;
4) диффузия ионов А внутри зерна смолы к ионообменным функциональным группам;
5) собственно химическая реакция двойного обмена ионов А и В;
6) диффузия ионов В внутри зерна ионита к границе раздела фаз;
7) переход ионов В через границу раздела фаз на внутреннюю поверхность пленки жидкости;
8) диффузия ионов В через пленку;
9) диффузия ионов В в ядро потока жидкости.
Слайд 15
Регенерация ионитов.
Катиониты регенерируют 2-8% растворами кислот. При
этом они переходят в Н-форму.
Регенерационные растворы — элюаты
содержат катионы.
Отработанные аниониты регенерируют 2-6% растворами щелочи. Аниониты при этом переходят в ОН-форму.
Элюаты содержат в сконцентрированном виде все извлеченные из сточных вод анионы.