— це органічні сполуки, до складу молекул яких входить
карбоксильна функціональна група:–
Насичені одноосновні карбонові кислоти містять одну карбоксильну групу й ординарні карбон-карбонові зв’язки.
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть






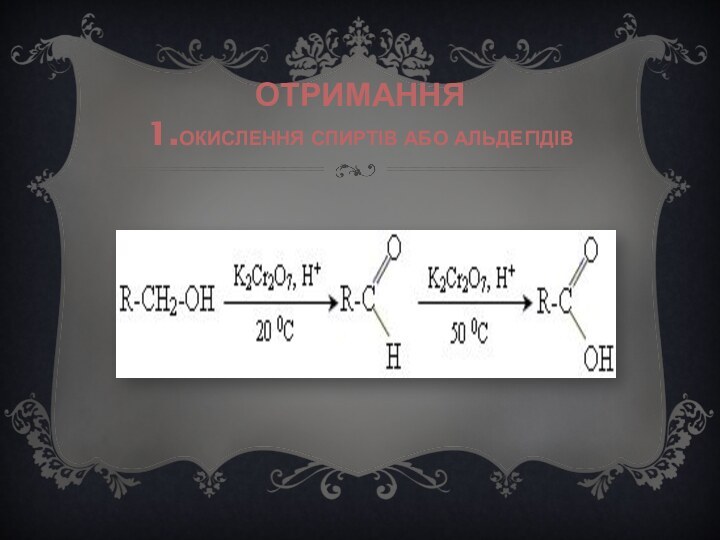













Фізичні властивості карбонових кислот.
Оцтова кислота — за кімнатної температури безбарвна рідина з різким характерним запахом. Температура кипіння 11 8°. Розчиняється у воді в будь-яких кількостях.
• класифікація за будовою вуглеводневого радикалу
насичені карбонові кислоти, наприклад: мурашина кислота, оцтова кислота.
ненасичені карбонові кислоти, наприклад: акрилова кислота*
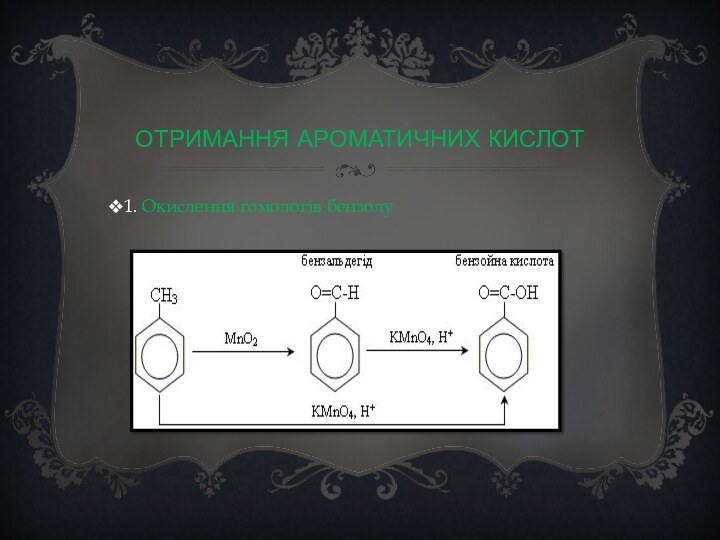
ароматичні карбонові кислоти, наприклад: бензойна кислота*
Класифікація карбонових кислот
Хімічні
Властивості
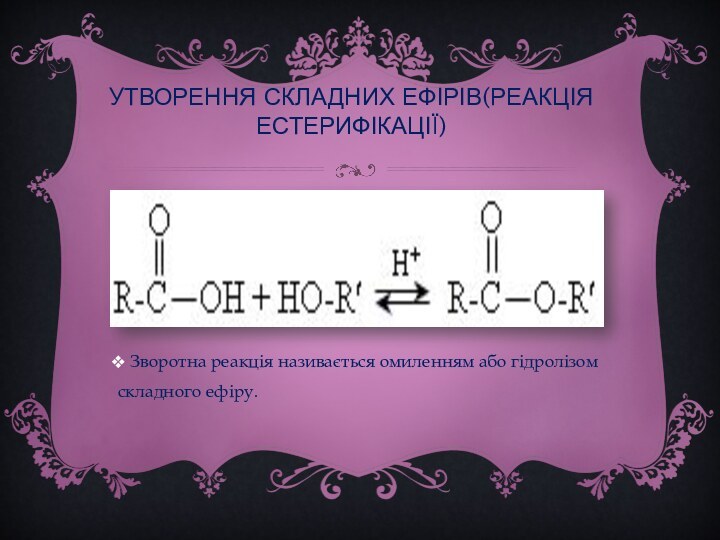
Естери, їх
Поширення
В природі
Жири