- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему ВОЗБУДИТЕЛЬ ТУБЕРКУЛЁЗА
Содержание
- 2. введениеТуберкулёз- инфекционная, хронически протекающая болезнь человека, животных,
- 3. Классификациятуберкулез у человека вызывают Mycobacterium tuberculosis (человеческий
- 4. В основу классификации микобактерий положены как морфологические,
- 5. Идентификация микобактерий представляет большие трудности. Участились случаи
- 6. К потенциально патогенным видам для людей принадлежат
- 7. M.tuberculosis образуют первичный рост при посеве патологического
- 8. M.avium отличаются от бычьего и человеческого видов
- 9. M.africanum вызывает туберкулез у людей в тропической
- 10. M.simiae – фотохромогенные, ниацонотрицательные, каталазо- и пероксидозаположительные.
- 11. M.intracellularae – палочки от коротких до длинных.
- 12. Локальные поражения обычно выявляют в почках мышей,
- 13. M.phlei – короткие палочки длиной 1 -2
- 14. M.ulcerans – выделены из кожных поражений людей
- 15. Клиническая картинаПервичный туберкулёзинфекционное заболевание, вызываемое микобактериями туберкулёза
- 16. Диссеминированный туберкулёз развивается при распространении микобактерий в
- 17. Вторичный туберкулёз Характерные признаки. Органный характер поражения
- 18. Течение и прогноз. Начало заболевания протекает скрыто.
- 19. Очаговый туберкулёз лёгких — малая клиническая форма. Он
- 20. Кавернозный туберкулёз лёгких характеризуется наличием сформированной каверны, отображаемой
- 21. Фиброзно-кавернозный туберкулёз лёгких — наиболее неблагоприятная гиперхроническая форма;
- 22. Микобактерии задерживаются в органах с наиболее развитым
- 26. ЛечениеЛечение туберкулёза, особенно внелёгочных его форм, является сложным делом, требующим много времени и комплексного подхода.
- 27. Трёхкомпонентная схема лечения. На заре противотуберкулёзной химиотерапии
- 28. Пятикомпонентная схема лечения. Во многих центрах, специализирующихся
- 29. Сопутствующая терапия ИммуномодуляторыДетоксикацияДругие препаратыХирургические методы лечения туберкулёза
- 30. Скачать презентацию
- 31. Похожие презентации
введениеТуберкулёз- инфекционная, хронически протекающая болезнь человека, животных, в том числе птиц, особенно кур. Патологоанатомически он характеризуется образованием туберкул (бугорков) и творожисто-перерожденных туберкулёзных очагов. Возбудителей туберкулёза человека и КРС открыл Р.КОХ в 1882г. Птичий вид установили Штраус



























Слайд 3
Классификация
туберкулез у человека вызывают Mycobacterium tuberculosis (человеческий вид),
Mycobacterium bovis (бычий вид) ,Mycobacterium avium-intracellulare (птичий вид), myc.murium
(мышей) и myc. Poikilotermum (рыб, змей, лягушек). Эти виды микобактерий способны проникать, жить и размножаться в организме человека и животных. Их присутствие обусловливает специфические морфологические и функциональные изменения в органах и тканях, которые клинически проявляются как инфекционное заболевание — туберкулез.Слайд 4 В основу классификации микобактерий положены как морфологические, так
и биологические признаки. Виды микобактерий различаются между собой как
по воздействию на организм человека или животного, так и по способности использовать те или иные питательные вещества, образовывать пигмент, по росту при различных температурах. При разграничении различных видов особое значение придают внешнему виду колоний, которые могут быть бесцветными или окрашенными, прозрачными или плотными, гладкими или шероховатыми, обладать медленным ростом и т.д.Слайд 5 Идентификация микобактерий представляет большие трудности. Участились случаи выделения
из патологического материала нетуберкулезных (атипичных) микобактерий, являющихся самостоятельными видами.
Род микобактерий включает в себя более 30 видов. К патогенным видам относят выше перечисленные.Слайд 6 К потенциально патогенным видам для людей принадлежат M.konsasii,
M.marinum, M.scrofulaceum, M.xeponi, M.ulcerans, M.fortuitum, M.chelonei. Остальные 16 видов
непатогенны для человека.Некоторые виды атипичных микобактерий вызывают у свиней патоморфологические изменения в лимфатических узлах, неотличимые от изменений, обусловленных микобактериями туберкулеза, у других животных – сенсибилизацию их к туберкулину. Каждый из видов микобактерий наиболее опасен для того вида животных, в котором он приобрел патогенные свойства.
M.bovis дают первичный рост в виде мелких гладких колоний на 30-45-60-ый день. При пассажах рост наблюдают на 14-21-ый день. Колонии не имеют пигмента, имеют белый или сероватый цвет. На жидкой среде образуют тонкую пленку. Температурный оптимум 37 – 38 С, при температуре 22 и 45 С - не растут. Патогенны для крупного рогатого скота, свиней, овец, коз, верблюдов, буйволов, оленей, маралов, собак, кошек и других видов животных, а также человека.
Слайд 7 M.tuberculosis образуют первичный рост при посеве патологического материала
на 21-45-60-ый день. Пассажированные культуры растут быстрее – на
10-14-21-ый день. Рост на плотной яичной среде, содержащий глицерин, обычно пышный; культуры имеют кремовый цвет оттенок и растут в виде шероховатых R-колоний, но могут быть гладкие, сливающиеся между собой (S-вариант). На жидкой питательной среде микобактерии человеческого вида туберкулеза образуют морщинистую грубую пленку, а иногда даже придонный крошковатый рост. Температурный оптимум 37-38 С, при22 и 45 С не растут. В мазке, окрашенном по Цилю-Нильсену, морфологически представлены в виде полиморфных, тонких, спирто -, кислотоустойчивых палочек, часто изогнутых. Патогенны для человека, обезьян, морских свинок, мышей, собак, коше, попугаев. У крупного рогатого скота, как правило, обуславливают сенсибилизацию организма к туберкулину для млекопитающих и лишь изредка вызывают ограниченные изменения , преимущественно в лимфатических узлах, регионарных местам проникновения микобактерий.Слайд 8 M.avium отличаются от бычьего и человеческого видов морфологией
колоний. Они мягкие, слизистые, серовато – белые, изредка слегка
желто – пигментированные, иногда при посеве из патологическотго материала вырастают в виде приподнимающихся над поверхностью среды «лепешек» или «бубликов». Рост появляется к концу 15–20–30–ого дня, иногда позже, при пересевах к 7-10 дню. В субкультурах представлены в виде гладкого, влажного налета. Культуры лучше растут при 43-45 С. Морфологически M.avium в мазках из культур выглядят как тонкие кислотоустойчивые палочки, более длинные и полиморфные в мазках-отпечатках из органов зараженных кур и кроликов. Патогенны в основном для птиц, кроликов, белых мышей, могут вызывать патологические изменения в органах у свиней и других животных.Слайд 9 M.africanum вызывает туберкулез у людей в тропической Африке.
Систематическое положение как отдельного вида пока обсуждается.
M.microti служит причиной
естественного туберкулеза у полевых мышей.M.paratuberculosis в мазках из патологического материала располагаются кучками, гнездами и палисадами, редко – попарно, три, четыре и еще реже – одиночно. Чрезвычайно трудно растут на искусственных питательных средах и только при обязательном добавлении к ним так называемого фактора роста. Оптимальная температура роста 38 С. Первичный рост появляется через 30-60 дней, иногда позже, в виде мельчайших колоний, постепенно приобретающих бело-кремовый цвет и увеличивающихся. Патогенны для крупного рогатого скота, коз, верблюдов, овец, северных оленей.
M.konsasii – палочки от умеренно длинных до длинных, расширяются и имеют заметную поперечную исчерченность. На яичных средах образуют гладкие или шероховатые колонии через 7 дней или позже посева. Оптимальная температура роста 37 С. Относится к фотохромогенным микобактериям. Патогенны для человека. Вызывает хронические легочные заболевания у людей, сходные с туберкулезом.
Слайд 10 M.simiae – фотохромогенные, ниацонотрицательные, каталазо- и пероксидозаположительные. Патогенны
преимущественно для обезьян.
M.marinum вызывают у людей кожные гранулемы вследствие
ссадин при купании в бассейне. Культуры фотохромогенны.M.scrofulaceum – на яичных средах растут при 25-37 С в виде гладких колоний желтого или оранжевого цвета. Рост появляется через 7 дней после посева при выращивании в термостате при 37 С. Для животных незначительно патогенны, редко выявляют локализованные поражения печени и селезенки у крыс, хомяков и цыплят; у морских свинок, зараженных подкожно, в месте инокуляции появляются абсцессы и увеличиваются регионарные лимфатические узлы.
Слайд 11 M.intracellularae – палочки от коротких до длинных. На
яичных средах через 7 дней после посева образуют гладкие
непигментированные колонии при температуре 37 С. По мере старения колонии могут желтеть. Вызывают патологоанатомические изменения в лимфатических узлах свиней. Патогенны для цыплят.M.xeponi – длинные нитевидные палочки. Растут при температуре 40-45 С. Молодые культуры дают непигментированные шероховатые колонии; позднее появляется пигмент желтого цвета. Выделены от жабы. Потенциально патогенны для человека.
M.gastri – умеренно длинные и тонкие палочки. На яичных средах образуют гладкие и грубые колонии через 7 дней и более после посева. Растут при температуре 25-40 С. Выделяют из почв, вод, желудка человека.
M.terrae – умеренно длинные тонкие палочки. На яичных средах расьтут на 7 дней и более после посева в виде гладких или шероховатых колоний белого или темно-желтого цвета при температуре 37 С. Выделяют из почвы.
M.triviale – на яичных средах растут в виде шероховатых R-колоний.
M.fortuitum – палочки длиной от 1-3 мкм , кокковидные, утолщенные, иногда с нитевидными разветвлениями. На яичных средах рост отмечают через 2-4 дня после посева, колонии могут быть гладкими, полусферической формы. У морских свинок, кроликов и мышей редко вызывают генерализованную инфекцию даже при больших дозах заражения.
Слайд 12 Локальные поражения обычно выявляют в почках мышей, морских
свинок, кроликов, обезьян, цыплят. При заражении мышей в ухо
наблюдают феномен вытечки.Выделяют из лимфатических узлов крупного рогатого скота; обнаруживают в почве, в организме хладнокровных животных. Потенциально патогенны для человека.
M.chelonei – микроорганизмы разной морфологии размером от 0,2 - 0,5 до 1-6 мкм. Через 3-4 после посева на всех питательных средах появляются гладкие, ровные колонии, влажные, нехромогенные или имеющие кремовую окраску. Эти микобактерии вызывают проходящие поражения у мышей, морских свинок, хомяков и кроликов. Они обладают ограниченной патогенностью при внутрибрюшинном введении. Внутривенное заражение вызывает у мышей сильное поражение селезенки, печени легких и почек, у человека – патологические изменения в синовиальной ткани коленного сустава и поражения в ягодичной части, подобно абсцессам.
Слайд 13 M.phlei – короткие палочки длиной 1 -2 мкм.
В посевах на яичной среде через 2- дней растут
в виде шероховатых колоний темно-желтого или оранжевого цвета. Некоторые культуры дают гладкие мягкие или маслянистые колонии. Могут обуславливать сенсибилизацию крупного рогатого скота к туберкулинам.M.dienhoferi – короткие прямые палочки размером от 0,5 – 0,8 до 1-30 мкм часто с толстыми закругленными концами. через три дня после посева на яичныхсредах появляются колонии от серого до темно-желтого цвета,. Колонии обычно гладкие полусферические и блестящие. Оптимальный рост при температуре 22-37 С. Рост подавляется полностью при 42 С.
M.thamnopheos - длинные стройные палочки размером от 4до 7 мкм, слегка изогнутые. На яичных питательных средах через 5-7 дней появляются влажные непигментированные колонии, иногда окрашенные в розовый или оранжево-розовый цвет. Растут при температуре 10-35 С, не растут при температуре 37 С. Патогенны для змей, лягушек, ящериц и рыб, непатогенны для морских свинок, кроликов и домашней птицы.
M.flavescens – на яичных средах через 7-10 дней после посева образуют мягкие, окрашенные в оранжевый цвет колонии. Непатогенны для человека и животных.
M.nonchromogenicum – выделены от мышей.
Слайд 14 M.ulcerans – выделены из кожных поражений людей в
Австралии, Мексике, Новой Гвинеи, Африке и Малайских островах.
M.vaccae –
выделены из молочных желез коров. Найдены на лугах, пастбищах, в прудах, колодцах, иногда в кожных поражениях у коров.M.smegmatis – выделены из смегмы, найдены в почве и воде.
M.leprae – вызывает лепру у человека.
M.lepramurium- не растут in vitro, но могут экспериментально пассажироваться через крыс, хомяков, мышей. Вызывают лепру у крыс, мышей и некоторых других родственных им грызунов.
Слайд 15
Клиническая картина
Первичный туберкулёз
инфекционное заболевание, вызываемое микобактериями туберкулёза в
период первичного инфицирования (7—10% инфицированных), наиболее типичен для младенцев
и лиц, инфицированных ВИЧ-1. Характерные признаки. Лимфотропность. Несовершенство иммунного ответа. Параспецифические и обширные перифокальные реакции. Склонность к генерализации процесса, а в последующем (при формировании иммунитета) — возможность самоизлечения. Клинические формы. Туберкулёзная интоксикация у детей и подростков. ТВГЛУ. ПТК. Клиническая картина. Как правило, бессимптомное течение до развития осложнений. Неспецифический пневмонит обычно обнаруживают в средних или нижних отделах лёгких. Увеличенные лимфатические узлы в корнях лёгких в детском возрасте могут стать причиной нарушения проходимости бронхов. Осложнения. Сдавление органов средостения гиперплазированными лимфатическими узлами. Вовлечение плевры при субплевральной локализации туберкулёзного очага. Исходы. Кальцинаты лимфатических узлов и/или кальцинированный очаг в лёгком.
Слайд 16
Диссеминированный туберкулёз
развивается при распространении микобактерий в органы или
несколько органов гематогенным или лимфогенным путём с образованием очагов
продуктивного воспаления. Эта форма может носить черты как первичного, так и вторичного туберкулёза. Характерные признаки. Симметричность процесса по локализации (обычно преимущественно в верхних отделах лёгких). Симметричность процесса по времени (изменения изоморфны, каверна с одной стороны и очаги с другой позволяют исключить диссеминированный процесс). Течение. Острый диссеминированный туберкулёз лёгких выделен в отдельную форму — милиарный туберкулёз, развивающийся вследствие обширного гематогенного распространения туберкулёзной инфекции. Несвоевременная диагностика этой формы туберкулёза и отсутствие лечения приводят к гибели больного в течение нескольких месяцев (скоротечная чахотка). Клиническая картина (опережает рентгенологическую на 2—6 нед). Выделяют лёгочную (с преобладанием одышки и других лёгочных симптомов) и тифоидную (с преобладанием симптомов интоксикации вплоть до спутанности сознания) формы. Лихорадка неясного генеза, иногда с двугорбой температурной кривой, часто сопровождающейся анемией и спленомегалией. В детском возрасте милиарный туберкулёз может протекать молниеносно (внезапное начало, тяжёлая интоксикация, тахикардия и одышка). Гематогенные отсевы могут возникать одномоментно в различных органах (возможно поражение мозговых оболочек). Рентгенодиагностика. Двусторонняя симметричная тотальная мелкоочаговая диссеминация. Часто эту картину распознают на боковых снимках или на «мягких» рентгенограммах. Бактериоскопия и бактериологическое исследование мокроты малоинформативны (мокрота бывает не всегда и редко содержит микобактерий). Туберкулинодиагностика (см. ниже). Типична туберкулиновая анергия, и поэтому отрицательные кожные пробы не имеют дифференциально-диагностического значения. В наблюдениях in vitro в культуре лимфоцитов также была обнаружена анергия, связанная с супрессорной функцией моноцитов. При успешном лечении и стабилизации состояния больного ми-лиарным туберкулёзом туберкулиновая гиперчувствительность восстанавливается. Трансбронхиальной биопсией или биопсией печени часто подтверждают диагноз. Биопсия костного мозга положительна у 2/3 больных. Подострый и хронический диссеминированный туберкулёз — следствие повторного поступления в кровь микобактерий из первичного туберкулёзного фокуса, проявляются прежде всего симметричным поражением верхних отделов обоих лёгких. Дифференциальную диагностику проводят с саркоидозом и другими гранулематозами, пневмокониозом, канцероматозом, фиброзирующим альвеолитом и гемосидерозом. Подострый диссеминированный туберкулёз — «штампованные» или «очковые» каверны, образующиеся в верхних долях обоих лёгких. Хронический диссеминированный туберкулёз — старые очаги, кальцинаты, уменьшение в объёме верхних долей лёгких и подтянутость корней кверху. Симптомы — одышка и прогрессирующая лёгочно-сердечная недостаточность.
Слайд 17
Вторичный туберкулёз
Характерные признаки. Органный характер поражения (чаще с
поражением лёгких) с образованием очага, инфильтрата или каверны без
вовлечения в процесс лимфатических узлов. Поражение верхушечного, заднего апикального сегментов верхней доли и верхнего сегмента нижней доли (I, II и VI сегменты). Распространённость поражения варьирует от очагов и малых инфильтратов (не всегда проявляющихся клинически) до обширных процессов с полостными образованиями, фиброзом, истощением и лёгочно-сердечной недостаточностью. Наличие очагов-отсевов, появляющихся вслед за основным поражением. Данные объективного исследования информативны лишь при обширном поражении. Хрипы над верхушками, усиливающиеся после покашливания. Амфорическое дыхание (при наличии больших каверн). Укорочение перкуторного звука над верхушками лёгких.Слайд 18 Течение и прогноз. Начало заболевания протекает скрыто. Поражение
лёгкого развивается в течение нескольких недель При естественном развитии
процесса у трети пациентов отмечают длительное течение заболевания с периодами ремиссий и обострений. В процессе прогрессирования поражения лёгкого центральный некроз сопровождается развитием казеоза, названного так за внешнее сходство некротизированного материала с творожистыми массами, последние могут быть частично разжижены. Некротический материал может отторгаться через бронхи с образованием лёгочных каверн — полостных образований туберкулёзной природы. В это же время возможен бронхогенный отсев с развитием новых участков экссудативного воспаления. У некоторых больных процесс может захватывать сегмент или долю. Иногда бронхо-генное распространение туберкулёза происходит вследствие прорыва поражённого перибронхиального лимфатического узла в просвет бронха (аденогенный туберкулёз) С прогрессированием туберкулёза лёгкое утрачивает свою нормальную структуру — типичны развитие фиброза, уменьшение объёма лёгкого и подтягивание корней лёгких кверху. При своевременной химиотерапии недавно выявленный процесс заживает с относительно небольшими потерями лёгочной ткани В среднем 60% нелеченых пациентов умирают в течение 2,5 лет.Слайд 19 Очаговый туберкулёз лёгких — малая клиническая форма. Он может
носить характер вновь выявленного (мягко-очаговый) или инволютивного (фиброзно-очаговый) как
следствие обратного развития более тяжёлых форм. Выделение микобактерий больными, как правило, отсутствует. Диагноз подтверждают флюорографией или рентгенографией органов грудной клетки. Дифференциальную диагностику проводят с очаговой пневмонией, ранними стадиями опухолей и очаговым пневмосклерозом.Инфильтративный туберкулёз лёгких — самая распространённая форма вторичного туберкулёза, характеризующаяся наличием в лёгких инфильтрата. Может быть бессимптомной при бронхолобу-лярном инфильтрате либо протекать с достаточно выраженными симптомами туберкулёзной интоксикации, кашлем и даже кровохарканьем при лобите. Проявления других клинико-рентгенологических форм нарастают последовательно от сегментита, округлого инфильтрата, облаковидного инфильтрата и перисциссурита (с вовлечением междолевой борозды) до казеозной пневмонии, выделенной в настоящее время в отдельную клиническую форму и характеризующуюся поражением доли лёгкого и более массивным казеозным некрозом с последующим его распадом и отторжением, угнетением иммунных реакций (несмотря на бацилловыделение, туберкулиновые пробы гипо- или энергические, см. ниже). Дифференциальную диагностику проводят с пневмониями, раком лёгкого и эозинофильными инфильтратами.
Туберкулёма лёгкого — относительно благоприятная форма, характеризующаяся инкапсулированным казеозным фокусом диаметром более 1 см. Наиболее часто — результат инволюции экссудативно-казеозного фокуса у лиц с высоким уровнем специфического иммунитета (туберкулиновые пробы чаще гиперергические). Различают мелкие туберкулёмы (до 2 см в диаметре), средние (2—4 см) и крупные (более 4 см в диаметре). Дифференциальную диагностику проводят с доброкачественными и злокачественными опухолями, аневризмами сосудов, кистой эхинококка. Лечение консервативное и оперативное (резекция лёгкого).
Слайд 20 Кавернозный туберкулёз лёгких характеризуется наличием сформированной каверны, отображаемой на
рентгенограмме изолированной кольцевидной тенью в лёгком. Эта форма возникла
в период внедрения антибактериальной терапии, при ней существование туберкулёзной каверны может не сопровождаться обсеменением или выраженной инфильтрацией. Формирование каверны происходит при наличии инфиль-тративного или диссеминированного туберкулёза лёгких. Распад каверны проявляется кашлем с мокротой, влажными хрипами в лёгких, кровохарканьем, бактериовыделением. Сформированная каверна малосимптомна. Она хорошо видна на обзорной рентгенограмме или КТ органов грудной клетки. Полагают, что кавернозная форма существует до двух лет, в течение этого срока она либо излечивается (включая резекцию лёгкого), либо прогрессирует до фиброзно-кавернозного туберкулёза, либо осложняется (аспергиллома). Осложнения — лёгочное кровотечение, особенно при прогрессировании туберкулёза (наличие терминальных лёгочных артерий внутри каверн создаёт риск профузного лёгочного кровотечения из так называемых аневризм Расмуссена; другая причина кровотечения — развитие аспергилломы в хронически существующей туберкулёзной полости [включая санированные каверны], в этом случае кровотечение не связано с прогрессированием туберкулёза). Прорыв туберкулёзной каверны в плевральную полость может вести к туберкулёзной эмпиеме и бронхоплевральному свищу.Слайд 21 Фиброзно-кавернозный туберкулёз лёгких — наиболее неблагоприятная гиперхроническая форма; типичны
наличие толстостенных, нередко деформированных каверн, окружённых фиброзной тканью, деформации
бронхов, смещение органов средостения, постоянное или рецидивирующее бацилловыделение полирезистентных штаммов М. tuberculosis, развитие осложнений в виде кровохарканья и лёгочных кровотечений, амилоидоза, необратимой лёгочно-сердечной недостаточности, спонтанного пневмоторакса. Больные фиброзно-кавернозным туберкулёзом лёгких представляют наибольшую угрозу для здорового населения, требуют изоляции и длительной химиотерапии. Прогноз при этой форме туберкулёза часто неблагоприятный.Цирротический туберкулёз лёгких — конечная форма вторичного туберкулёза, возникающая в результате инволюции фиброзно-кавернозного, хронического диссеминированного, массивного инфильтративного туберкулёза, поражений плевры и ТВГЛУ с бронхолёгочным поражением. Характерно разрастание грубой соединительной ткани в лёгких и плевре. Это терминальная, но не самая опасная форма лёгочного туберкулёза (чаще всего больные олигобациллярны). Излечение таких больных проблематично, поскольку диффузия туберкулостатиков в изменённую ткань резко снижена. Локальные формы могут быть излечены хирургическим путём.
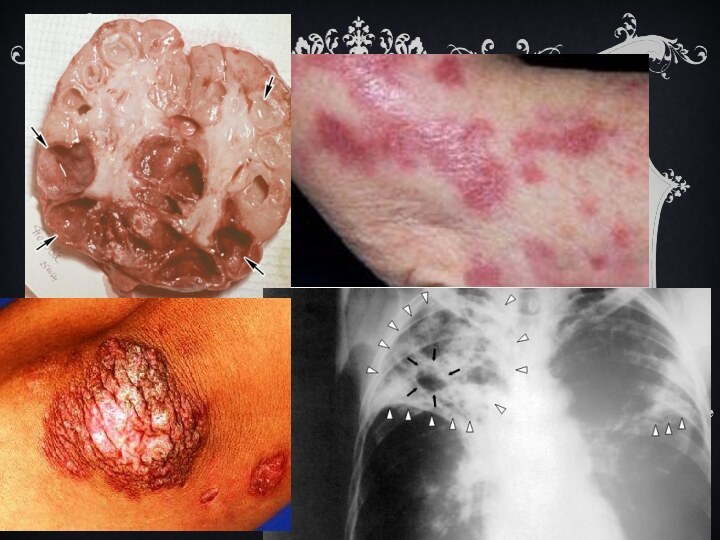
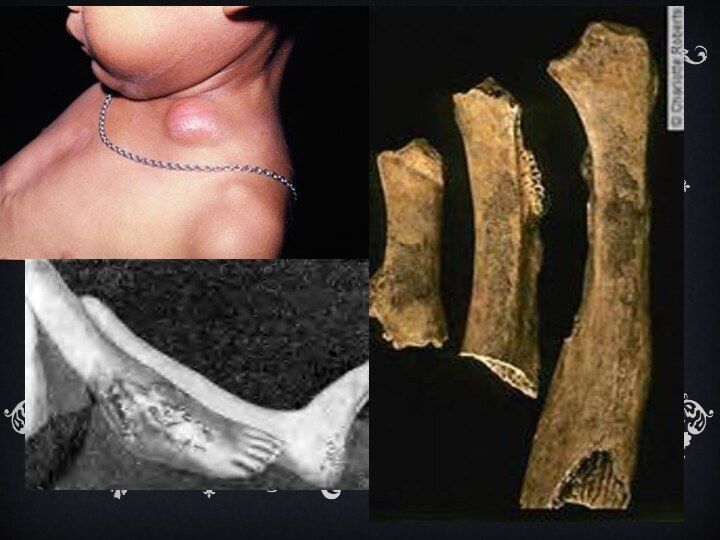
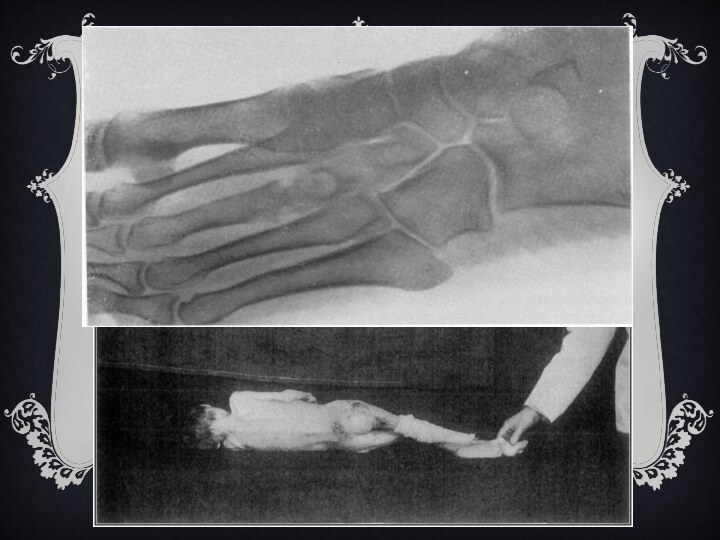
Слайд 22 Микобактерии задерживаются в органах с наиболее развитым микроциркуляторным
руслом: -легкие; - лимфатические узлы; - корковый слой почек; - эпифизы и метафизы
трубчатых костей; - ампуллярно-фимбриональные отделы маточных труб; - увеальный тракт глаза.
Слайд 26
Лечение
Лечение туберкулёза, особенно внелёгочных его форм, является сложным делом,
требующим много времени и комплексного подхода.
Слайд 27 Трёхкомпонентная схема лечения. На заре противотуберкулёзной химиотерапии была
выработана и предложена трёхкомпонентная схема терапии первой линии:
стрептомицин
изониазид
пара-аминосалициловая кислота (ПАСК).
Эта
схема стала классической. Она царствовала во фтизиатрии долгие десятилетия и позволила спасти жизни огромного числа больных туберкулёзом, однако почти исчерпала себя на сегодняшний день.Четырёхкомпонентная схема лечения
Одновременно в связи с повышением устойчивости выделяемых от больных штаммов микобактерий возникла необходимость усиления режимов противотуберкулёзной химиотерапии. В результате была выработана четырёхкомпонентная схема химиотерапии первой линии (DOTS — стратегия, используется при инфицировании достаточно чувствительными штаммами):
рифампицин или рифабутин
стрептомицин или канамицин
изониазид или фтивазид
пиразинамид либо этионамид
Эта схема была разработана Карелом Стибло (Нидерланды) в 1980-х годах. К концу двадцатого века система лечения т. н. препаратами первого ряда (включая изониазид, рифампицин,стрептомицин, пиразинамид и этамбутол) стала общепринятой в 120 странах мира, включая развитые страны.
Слайд 28 Пятикомпонентная схема лечения. Во многих центрах, специализирующихся на
лечении туберкулёза, сегодня предпочитают применять ещё более мощную пятикомпонентную
схему, добавляя к упомянутой выше четырёхкомпонентной схеме производное фторхинолона, например, ципрофлоксацин. Включение препаратов второго, третьего и выше поколения является основным при лечении лекарственноустойчивых форм туберкулёза. Режим лечения препаратами второго и выше поколения подразумевает как минимум 20 месяцев ежедневного приёма препаратов. Данный режим гораздо дороже, чем лечение препаратами первого ряда. Существенно ограничивающим моментом также является наличие огромного количества различного рода побочных эффектов от применения дополнительных препаратов.Если, несмотря на 4—5-компонентный режим химиотерапии, микобактерии всё же развивают устойчивость к одному или нескольким применяемым химиопрепаратам, то применяют:циклосерин, капреомицин и другие препараты, относящиеся ко второму (резервному) ряду вследствие своей токсичности для человеческого организма.





























