- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Ферменты. Классификация ферментов по структуре
Содержание
- 2. План лекции1. Определение2. Классификация3. Строение и функции4.
- 3. Ферменты (от лат. fermentatio – брожение) или
- 4. Классификация ферментов по структуре:1. Простые - состоят
- 5. 1. Оксидоредуктазы – катализируют окислительно-восстановительные реакции, осуществляя
- 6. Шифр ферментов1.1.1.27 - ЛДГВ каждом шифре 4
- 8. Структура ферментовПепси́н (др.-греч. πέψις — пищеварение) — протеолитический фермент класса
- 9. Пепсин
- 10. Активный центр ферментаЭтапы ферментативного катализа. I - этап
- 11. Фермент понижает энергию активации Еа, т.е. снижает
- 12. Уравнение Михаэ́лиса — Ме́нтен — основное уравнение ферментативной кинетики, описывает
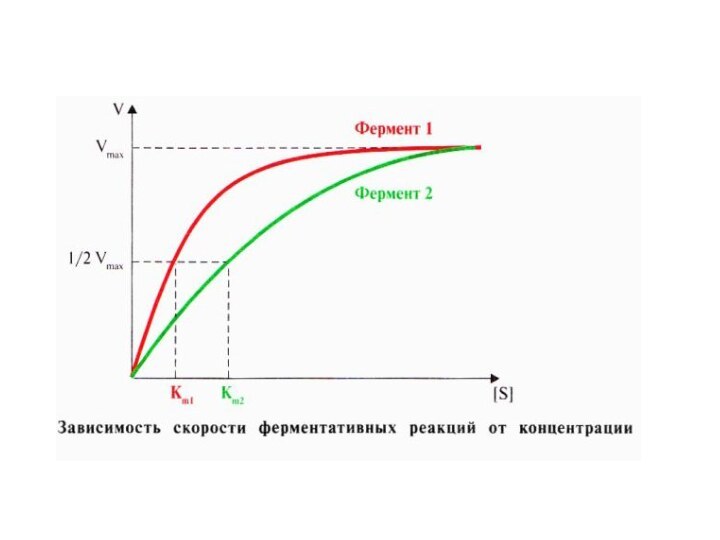
- 13. Кривая насыщения химической реакцииИллюстрирующая соотношение между концентрацией субстрата [S] и скоростью реакции V
- 14. СпецифичностьФерменты проявляют высокую специфичность по отношению к
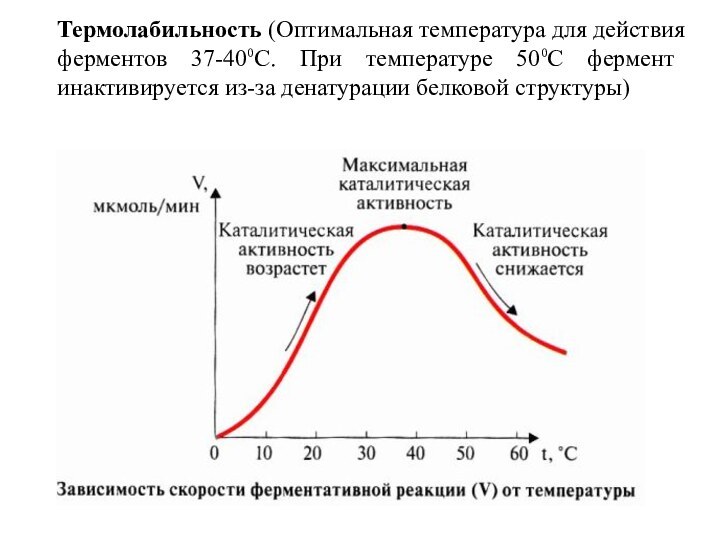
- 15. Термолабильность (Оптимальная температура для действия ферментов 37-40⁰С. При температуре 50⁰С фермент инактивируется из-за денатурации белковой структуры)
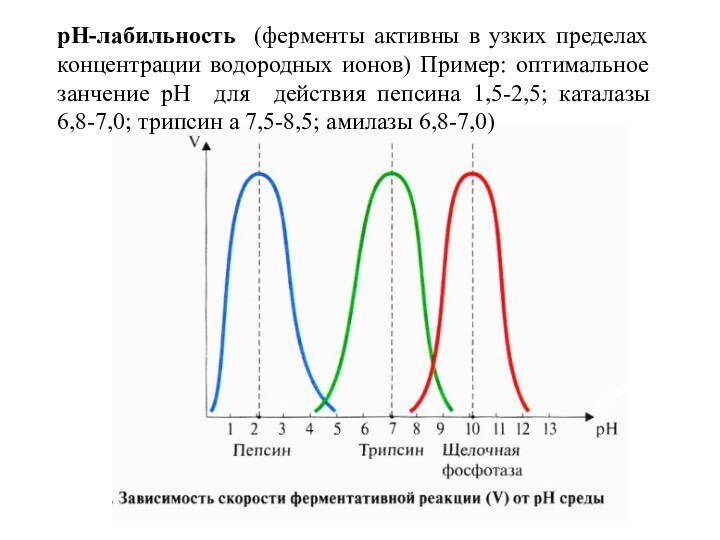
- 16. pH-лабильность (ферменты активны в узких пределах концентрации
- 18. Единицы измерения активности
- 19. Дегидрогеназы - аэробные (глютамат
- 20. ТрансферазыФерменты: Аминотрансферазы ФосфотрансферазыГликозилтрансферазыКоферменты: АТФ, ГТФ, УДФ, ЦДФ,
- 21. ГидролазыФерменты: Пептидгидролазы: - аминопептидазы
- 22. ЛиазыКоферменты: - Фосфопиридоксаль
- 23. ИзомеразыКоферменты: кобамидные коферменты (витамин B12)Цис-трансизомеразы - 5.2.Внутримолекулярные - 5.4.
- 24. Скачать презентацию
- 25. Похожие презентации








![Ферменты. Классификация ферментов по структуре Кривая насыщения химической реакцииИллюстрирующая соотношение между концентрацией субстрата [S] и скоростью реакции V](/img/tmb/15/1408422/935474c58304b64eb923471ad9a60033-720x.jpg)








Слайд 3 Ферменты (от лат. fermentatio – брожение) или энзимы
( от греч. en zyme – в дрожжах) –
это специфические белки глобулярной природы, которые присутствуют во всех живых организмах и играют роль биологических катализаторов.Наука о ферментах – энзимология.
Ферменты обычно белковые молекулы или молекулы РНК(рибозимы) или их комплексы, ускоряющие (катализирующие) химические реакции в живых системах. Реагенты в реакции, катализируемой ферментами, называются субстратами, а получающиеся вещества — продуктами.
Слайд 4
Классификация ферментов по структуре:
1. Простые - состоят только
из остатков аминокислот (гидролитические ферменты: пепсин, трипсин, лизоцим и
т.д.)2. Сложные (холоферменты) имеют в своем составе белковую часть, состоящую из аминокислот – апофермент, и небелковую часть – кофактор. Кофактор, в свою очередь, может называться коферментом или простетической группой. Примером могут быть сукцинатдегидрогеназа (содержит ФАД) (в цикле трикарбоновых кислот), аминотрансферазы (содержат пиридоксальфосфат), пероксидаза (содержит гем).
Также кофактором может быть ионы : Ca2+ · Cu2+ · Fe2+, Fe3+ · Mg2+ · Mn2+ · Mo · Ni2+ · Se · Zn2+
Слайд 5 1. Оксидоредуктазы – катализируют окислительно-восстановительные реакции, осуществляя перенос
Н и О (Пример: каталаза, перокидаза)
2. Трансферазы – катализируют
перенос группы атомов (метильной, фосфатной, аминной и т.д.) (Пример: АлАт, АсАт) 3. Гидролазы - катализируют расщипление сложных веществ на простые в присутствии воды. (Пример: амилаза)
4. Лиазы – катализируют обратимые реакции отщипления различных групп от субстратов негидролитическим путём (Пример: L-малат-гидролаза)
5. Изомеразы - катализируют реакции внутримолекулярных перестроек, т.е. превращение одного изомера в другой (Пример: глюкозо-6-фосфатизомераза)
6. Лигазы (синтетазы) катализируют реакции синтеза с использованием АТР (Пример: глутамат-аммиак-лигаза)
По типу катализируемых реакций
Слайд 6
Шифр ферментов
1.1.1.27 - ЛДГ
В каждом шифре 4 цифры:
1 - класс ферментов
2 - подкласс (указывает какая группировка
является донором)3 - подподкласс (указывает какая группировка является акцептором)
4 - порядковый номер фермента в подподклассе.
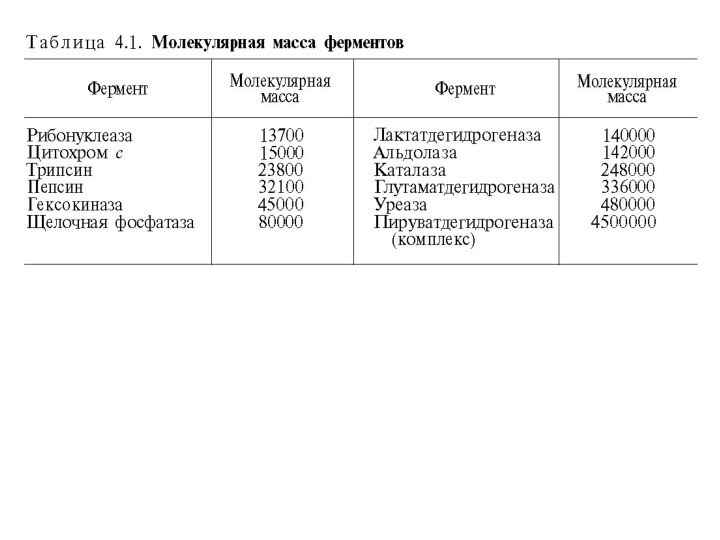
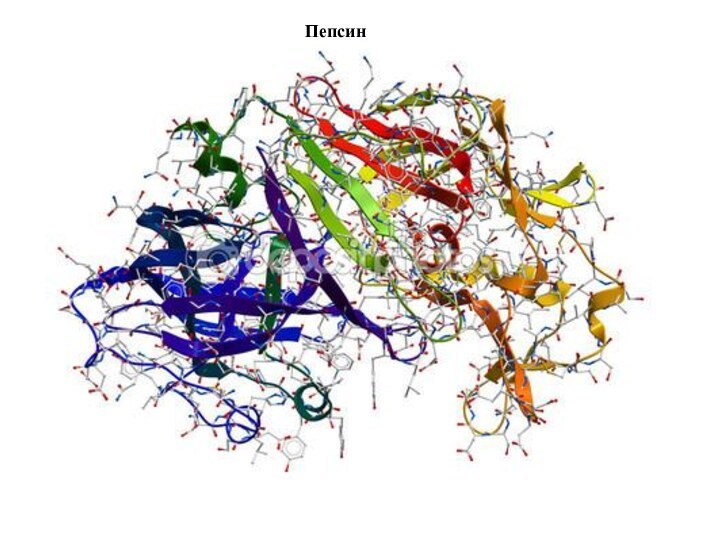
Слайд 8
Структура ферментов
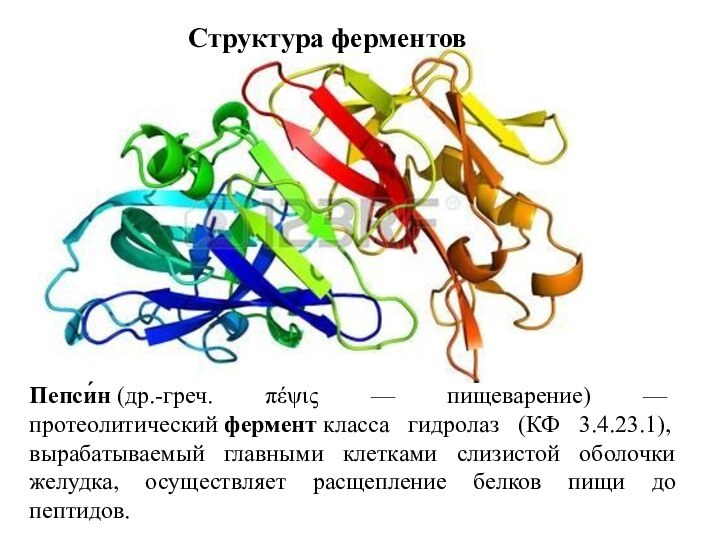
Пепси́н (др.-греч. πέψις — пищеварение) — протеолитический фермент класса гидролаз
(КФ 3.4.23.1), вырабатываемый главными клетками слизистой оболочки желудка, осуществляет
расщепление белков пищи до пептидов.
Слайд 10
Активный центр фермента
Этапы ферментативного катализа. I - этап сближения
и ориентации субстрата относительно активного центра фермента; II -
образование фермент-субстратного комплекса (ES) в результате индуцированного соответствия; III - деформация субстрата и образование нестабильного комплекса фермент-продукт (ЕР); IV- распад комплекса (ЕР) с высвобождением продуктов реакции из активного центра фермента и освобождением фермента.Механизм действия ферментов
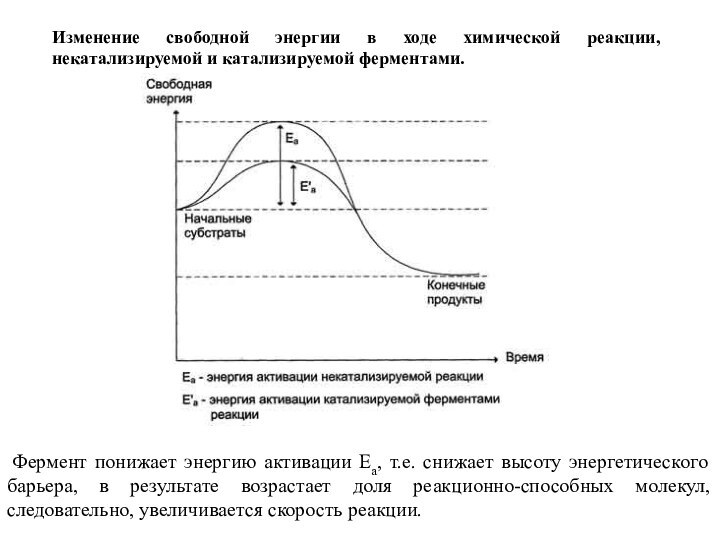
Слайд 11 Фермент понижает энергию активации Еа, т.е. снижает высоту
энергетического барьера, в результате возрастает доля реакционно-способных молекул, следовательно,
увеличивается скорость реакции.Изменение свободной энергии в ходе химической реакции, некатализируемой и катализируемой ферментами.
Слайд 12 Уравнение Михаэ́лиса — Ме́нтен — основное уравнение ферментативной кинетики, описывает зависимость
скорости реакции, катализируемой ферментом, от концентрации субстрата.
Для реакции:
S — концентрация субстрата
Слайд 13
Кривая насыщения химической реакции
Иллюстрирующая соотношение между концентрацией субстрата
[S] и скоростью реакции V
Слайд 14
Специфичность
Ферменты проявляют высокую специфичность по отношению к своим
субстратам (субстратная специфичность). Это достигается частичной комплементарностью формы, распределения
зарядов и гидрофобных областей на молекуле субстрата и в центре связывания субстрата на ферменте. Ферменты обычно демонстрируют также высокий уровень стереоспецифичности (образуют в качестве продукта только один из возможных стереоизомеров или используют в качестве субстрата только один стереоизомер), региоселективности (образуют или разрывают химическую связь только в одном из возможных положений субстрата) и хемоселективности (катализируют только одну химическую реакцию из нескольких возможных для данных условий).Виды:
-абсолютная
-относительная (групповая)
Слайд 15 Термолабильность (Оптимальная температура для действия ферментов 37-40⁰С. При
температуре 50⁰С фермент инактивируется из-за денатурации белковой структуры)
Слайд 16 pH-лабильность (ферменты активны в узких пределах концентрации водородных
ионов) Пример: оптимальное занчение рН для действия пепсина 1,5-2,5;
каталазы 6,8-7,0; трипсин а 7,5-8,5; амилазы 6,8-7,0)
Слайд 19
Дегидрогеназы
- аэробные (глютамат ДГ),
- анаэробные
Оксигеназы
- монооксигеназы
- диоксигеназыРедуктазы
Оксидоредуктазы
Коферменты:
НАД, НАДФ, ФАД, ФМН, коэнзим Q, липоевая кислота, глутатион, гем.
Кофактор: витамин С
Слайд 20
Трансферазы
Ферменты:
Аминотрансферазы
Фосфотрансферазы
Гликозилтрансферазы
Коферменты: АТФ, ГТФ, УДФ, ЦДФ, тетрогидрофолиевая
кислота,
фосфопиридоксаль, SH-Коэнзим А, ФАФС.
2.6.2.1 - АЛТ
Подкласс говорит о группе,
которую переносит фермент. Если группа азотистая - 2.6., если аминогруппа, то 2.6.2.
Слайд 21
Гидролазы
Ферменты:
Пептидгидролазы:
- аминопептидазы
- карбоксипептидаза
- дипептидазы
- пепсин- трипсин
- химотрипсин
Гликозидазы
Коферментов НЕТ.
Слайд 22
Лиазы
Коферменты:
- Фосфопиридоксаль
-
Тиаминпирофосфат
Если разрыв связи С-С, то 4.1.
С-О, то 4.2.С-N, то 4.3.
С-S, то 4.4.





























