Слайд 2
Русский ученый Д.И. Ивановский - первооткрыватель вирусов и
основоположник вирусологии
В 1892 году описал необычные свойства возбудителей болезни
табака – (табачной мозаики), который проходил через бактериальные фильтры и заражал здоровые растения, при этом он был не способен к культивированию.
12 февраля 1892 - отчет истории вирусологии.
Ф.Леффлер и П. Фрош (1898) - открытие вируса, вызывающего ящур у животных;
В. Рид и Дж. Кэррол (1901) - выделение вируса желтой лихорадки у людей;
Ф. д’Эррель и Ф. Туорт (1915−1917) обнаружили вирусы у бактерий (бактериофаги).
Слайд 3
Значение вирусологии как науки:
-
Ведущая роль вирусов в
инфекционной патологии
( примеры - вирус гриппа, ВИЧ - вирус
иммунодефицита человека, цитомегаловирус и другие герпесвирусы,) на фоне практически полного отсутствия средств специфической химиотерапии;
- использованием вирусов для решения многих фундаментальных вопросов биологии и генетики.
Вирусы как модель в фундаментальных вопросах молекулярной биологии (пример –результаты электронной микроскопии, обратная транскриптаза)
Слайд 4
Вирусы (от лат. virus – яд) наименьшие по
размерам агенты, имеющие геном, окруженный белковой оболочкой
Отличительные признаки:
●
облигатные внутриклеточные паразиты
● не способны к самопроизвольному делению
● не имеют ферментов энергетического метаболизма и белоксинтезирующих систем
● наличие одного типа нуклеиновой кислоты (ДНК или РНК)
● отсутствие клеточного строения
● возможность интеграции в клеточный геном и репликации с ним
● разобщенным (дисъюнктивным) способом размножения (репродукции) - только в живой клетке отдельно синтезируются нуклеиновые кислоты вирусов и их белки, затем происходит их сборка в вирусные частицы.
Слайд 6
Простейшая классификация вирусов
Слайд 7
Молекулярно-биологические особенности вирусов:
● Морфология: размеры в широких
пределах: 15 - 400 нм
● Форма: палочковидная (вирус Эбола),
пулевидная (вирус бешенства), нитевидная, сферическая (герпесвирусы), овальные (вирус оспы), шаровидная ( ротавирус)
● Геном вирусов образуют нуклеиновые кислоты, представленные одноцепочечными молекулами РНК (у большинства РНК- вирусов) или двухцепочечными молекулами ДНК (у большинства ДНК- вирусов).
● Капсид - белковая оболочка, в которую упакована геномная нуклеиновая кислота. Капсид состоит из идентичных белковых субъединиц - капсомеров.
● Транскрипция ДНК вирусов в м РНК осуществляется в ядре и регулируется ферментами клетки
Синтезируются: ранние белки
поздние белки
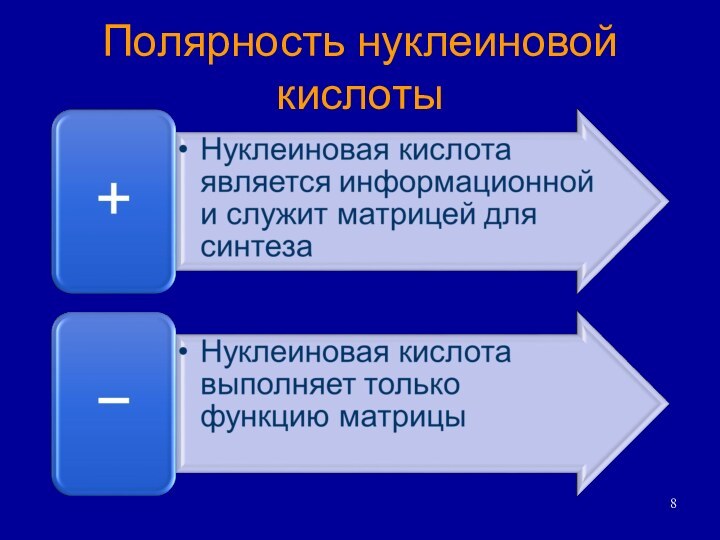
Однонитевую РНК вируса различают по - полярности. (+РНК и –РНК)
Двунитевую ДНК так же отличают по полярности(+ДНК и –ДНК).
Слайд 8
Полярность нуклеиновой кислоты
Слайд 9
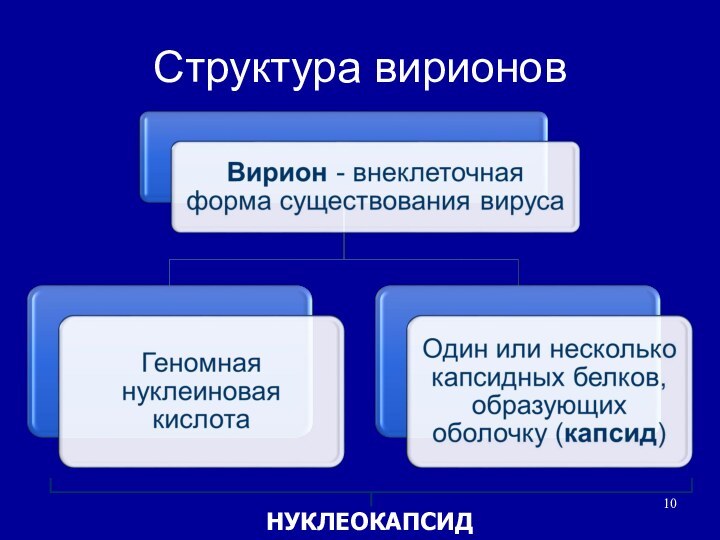
Формы существования вирусов
сохранение вируса во внешней среде и
перенос его в другую клетку
Слайд 11
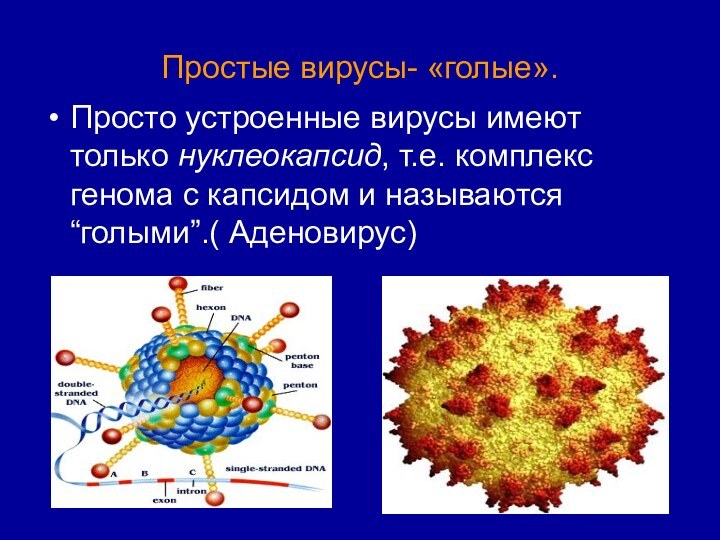
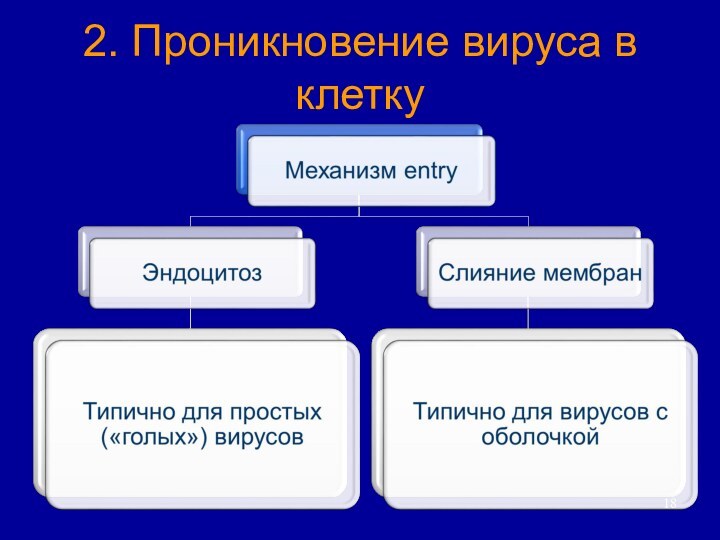
Простые вирусы- «голые».
Просто устроенные вирусы имеют только нуклеокапсид,
т.е. комплекс генома с капсидом и называются “голыми”.( Аденовирус)
Слайд 12
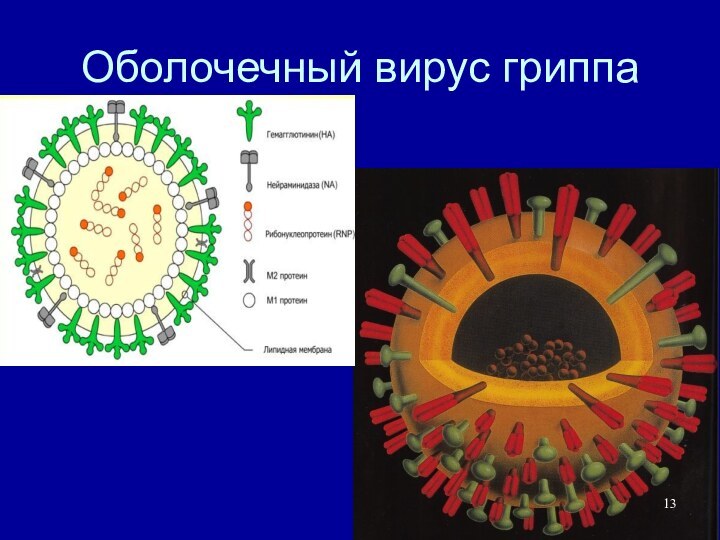
Структура сложных (оболочечных) вирионов
Более сложные вирионы могут иметь
внешнюю оболочку состоящий из двуслойной липидной мембраны (заимствованной из
мембраны клетки-хозяина), в которую встроены поверхностные гликопротеины вируса (вирусы гриппа, ретровирусы) – суперкапсид.
Изнутри к суперкапсиду может прилегать слой матриксного белка (М-слой)
Слайд 14
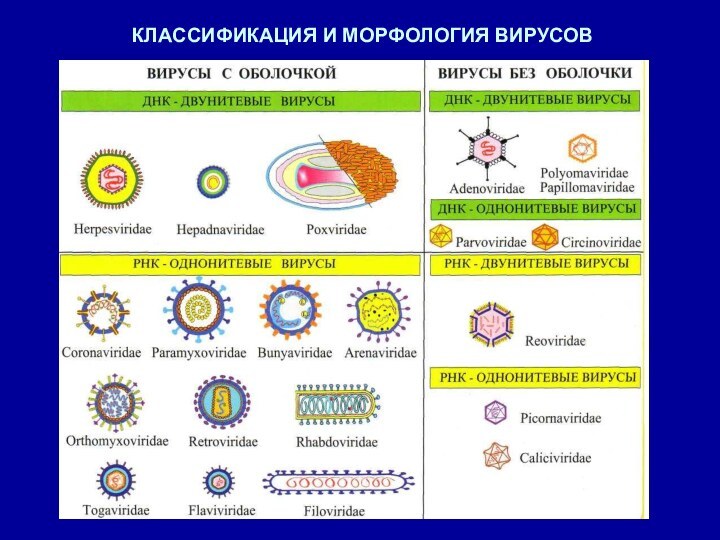
КЛАССИФИКАЦИЯ И МОРФОЛОГИЯ ВИРУСОВ
Слайд 17
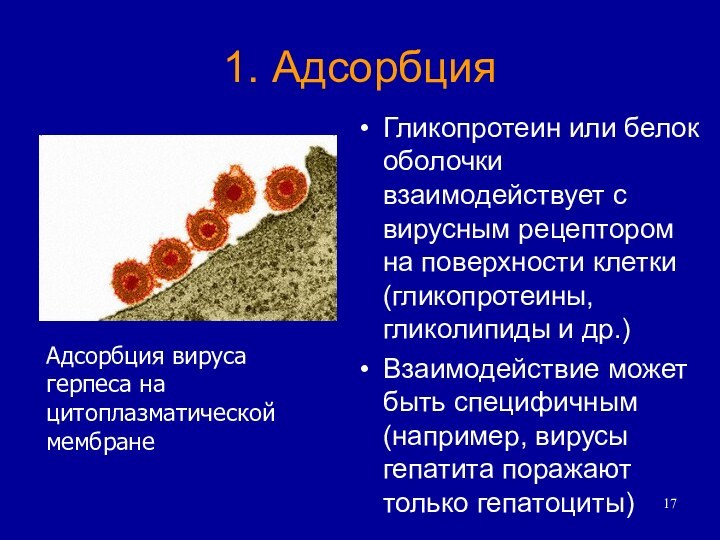
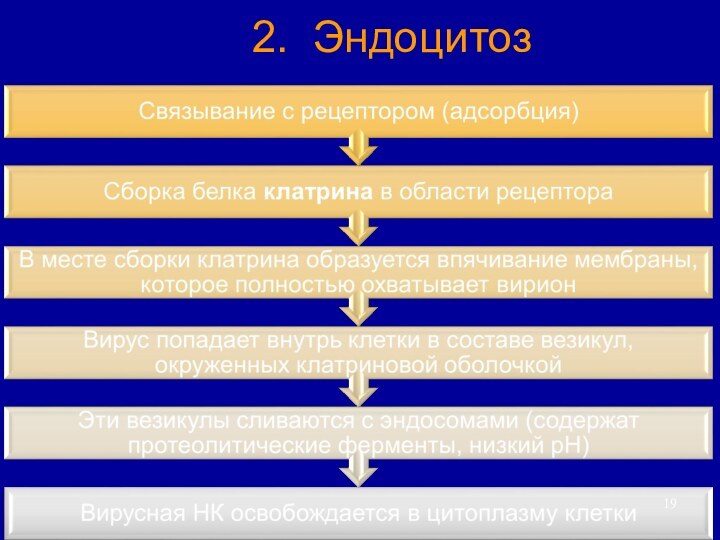
1. Адсорбция
Гликопротеин или белок оболочки взаимодействует с вирусным
рецептором на поверхности клетки (гликопротеины, гликолипиды и др.)
Взаимодействие может
быть специфичным (например, вирусы гепатита поражают только гепатоциты)
Адсорбция вируса герпеса на цитоплазматической мембране
Слайд 18
2. Проникновение вируса в клетку
Слайд 20
Один из поверхностных белков (белок слияния) взаимодействует с
липидным бислоем клетки, в результате липидные бислои вируса и
клетки сливаются в общую мембрану.
Содержимое вириона переходит внутрь клетки, а оболочка вириона остается на поверхности клетки.
Слияние мембран
Слайд 21
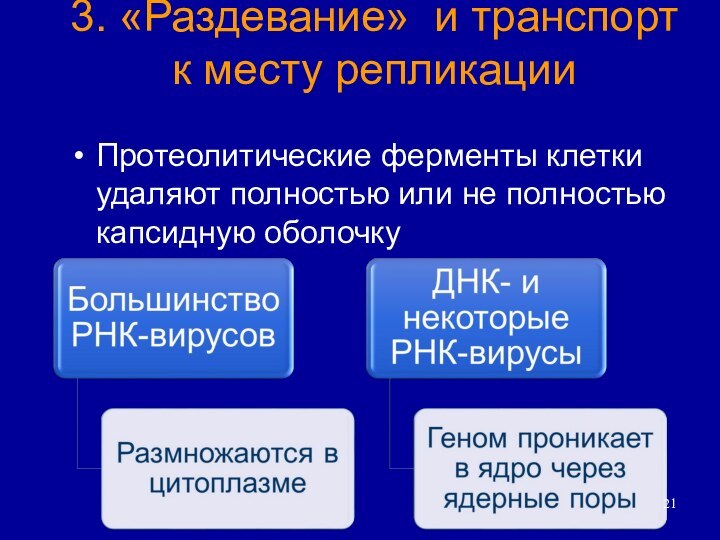
3. «Раздевание» и транспорт к месту репликации
Протеолитические ферменты
клетки удаляют полностью или не полностью капсидную оболочку
Слайд 23
Простые вирусы образуются путем самосборки: нуклеиновая кислота +
капсидные белки;
Сложные вирусы формируются в несколько этапов: образование
нуклеокапсида, «одевание» оболочки из мембраны клетки-хозяина.
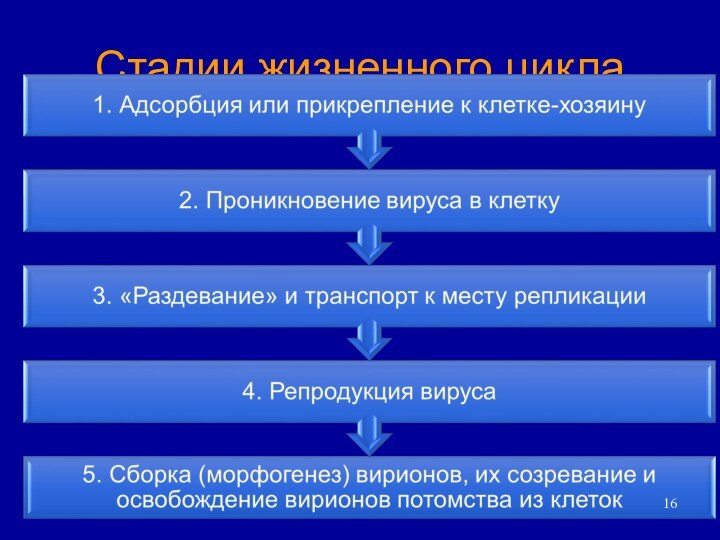
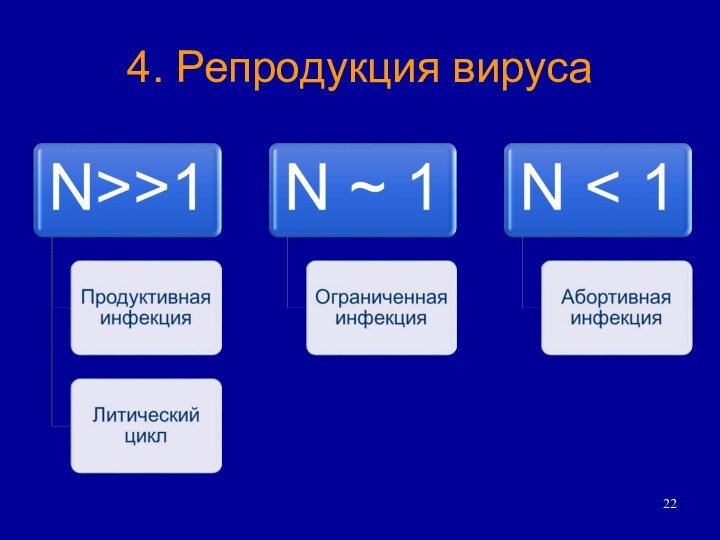
5. Сборка вирионов, созревание и выход из клеток
Слайд 24
Почкование
Нуклеиновая кислота и капсидный белок вируса собираются
в нуклеокапсид;
Белки-предшественники гликопротеинов проходят через ЭР и аппарат Гольджи;
Зрелые
гликопротеины встраиваются в плазматическую мембрану клеток, вытесняя гликопротеины хозяина;
Нуклеокапсид взаимодействует с гликопротеинами и образуется комплекс, подвергающийся экзоцитозу.
Слайд 25
Цитолиз
Сборка завершается в ядре или цитоплазме клетки-хозяина;
Вирус
нарушает жизнедеятельность клетки и приводит к ее гибели (некротическая
гибель);
Клеточные ферменты разрушают цитоплазматическую мембрану;
Вирус выходит во внеклеточную среду.
Слайд 27
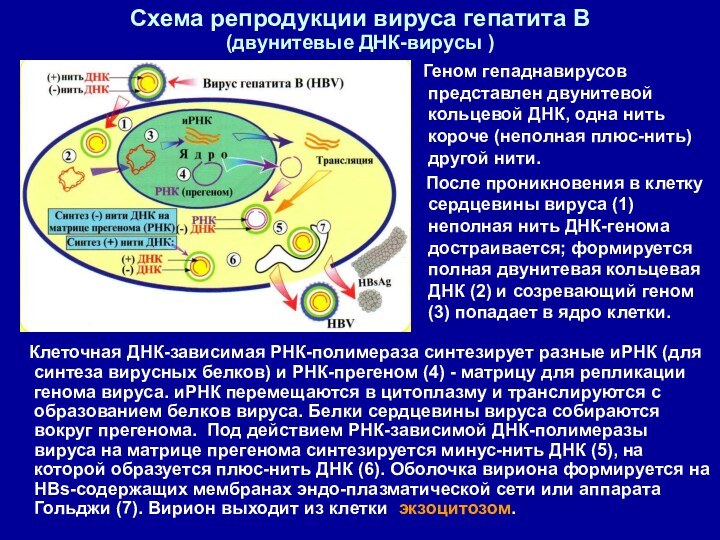
Схема репродукции вируса гепатита В
(двунитевые ДНК-вирусы )
Клеточная ДНК-зависимая РНК-полимераза синтезирует разные иРНК (для синтеза
вирусных белков) и РНК-прегеном (4) - матрицу для репликации генома вируса. иРНК перемещаются в цитоплазму и транслируются с образованием белков вируса. Белки сердцевины вируса собираются вокруг прегенома. Под действием РНК-зависимой ДНК-полимеразы вируса на матрице прегенома синтезируется минус-нить ДНК (5), на которой образуется плюс-нить ДНК (6). Оболочка вириона формируется на HBs-содержащих мембранах эндо-плазматической сети или аппарата Гольджи (7). Вирион выходит из клетки экзоцитозом.
Геном гепаднавирусов представлен двунитевой кольцевой ДНК, одна нить короче (неполная плюс-нить) другой нити.
После проникновения в клетку сердцевины вируса (1) неполная нить ДНК-генома достраивается; формируется полная двунитевая кольцевая ДНК (2) и созревающий геном (3) попадает в ядро клетки.
Слайд 28
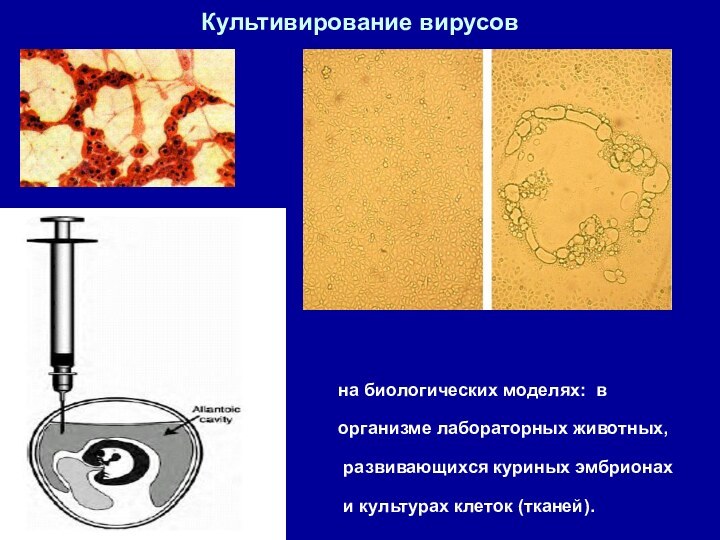
Культивирование вирусов
на биологических моделях: в
организме лабораторных животных,
развивающихся куриных эмбрионах
и культурах клеток (тканей).
Слайд 29
Типы клеточных культур.
1.Первичные (трипсинизированные) культуры - фибробласты эмбриона
курицы (ФЭК), человека (ФЭЧ), клетки почки различных животных и
т.д. Первичные культуры получают из клеток различных тканей чаще путем их размельчения и трипсинизации, используют однократно.
2.Линии диплоидных клеток пригодны к повторному диспергированию и росту, как правило, не более 20 пассажей (теряют исходные свойства).
3.Перевиваемые линии (гетероплоидные культуры), способны к многократному диспергированию и перевиванию, т.е. к многократным пассажам, наиболее удобны в вирусологической работе - например, линии опухолевых клеток Hela, Hep, Vero и др.
Слайд 30
Специальные питательные среды для культур клеток.
Используются разнообразные синтетические
(вирусологические) питательные среды сложного состава, включающие большой набор различных
факторов роста - среда 199, Игла, раствор Хэнкса, гидролизат лактальбумина. В среды добавляют стабилизаторы рН (Hepes), различные в видовом отношении сыворотки крови (наиболее эффективной считают эмбриональную телячью сыворотку), L-цистеин и L-глютамин.
В зависимости от функционального использования среды могут быть ростовые (с большим содержанием сыворотки крови) - их используют для выращивания клеточных культур до внесения вирусных проб, и поддерживающие (с меньшим содержанием сыворотки или ее отсутствием)- для содержания инфицированных вирусом клеточных культур
Слайд 31
Индикация вирусов
Индикацию вирусов проводят на основе следующих
феноменов: цитопатогенного действия (ЦПД) вирусов, образования внутриклеточных включений, образования
бляшек, реакции гемагглютинации, РН или «цветной» реакции.
ЦПД - видимые под микроскопом морфологические изменения клеток (вплоть до их отторжения от стекла), возникающие в результате внутриклеточной репродукции вирусов Включения - скопление вирионов или отдельных их компонентов в цитоплазме или ядре клеток, выявляемые под микроскопом при специальном окрашивании.
Вирус натуральной оспы образует цитоплазмати-ческие включения — тельца Гварниери; вирусы герпеса и аденовирусы - внутриядерные включения
Слайд 32
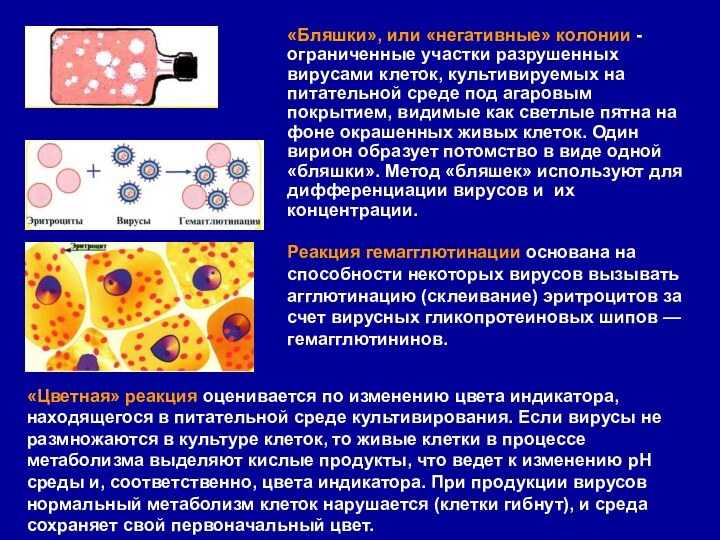
«Бляшки», или «негативные» колонии - ограниченные участки разрушенных
вирусами клеток, культивируемых на питательной среде под агаровым покрытием,
видимые как светлые пятна на фоне окрашенных живых клеток. Один вирион образует потомство в виде одной «бляшки». Метод «бляшек» используют для дифференциации вирусов и их концентрации.
Реакция гемагглютинации основана на способности некоторых вирусов вызывать агглютинацию (склеивание) эритроцитов за счет вирусных гликопротеиновых шипов — гемагглютининов.
«Цветная» реакция оценивается по изменению цвета индикатора, находящегося в питательной среде культивирования. Если вирусы не размножаются в культуре клеток, то живые клетки в процессе метаболизма выделяют кислые продукты, что ведет к изменению рН среды и, соответственно, цвета индикатора. При продукции вирусов нормальный метаболизм клеток нарушается (клетки гибнут), и среда сохраняет свой первоначальный цвет.
Слайд 33
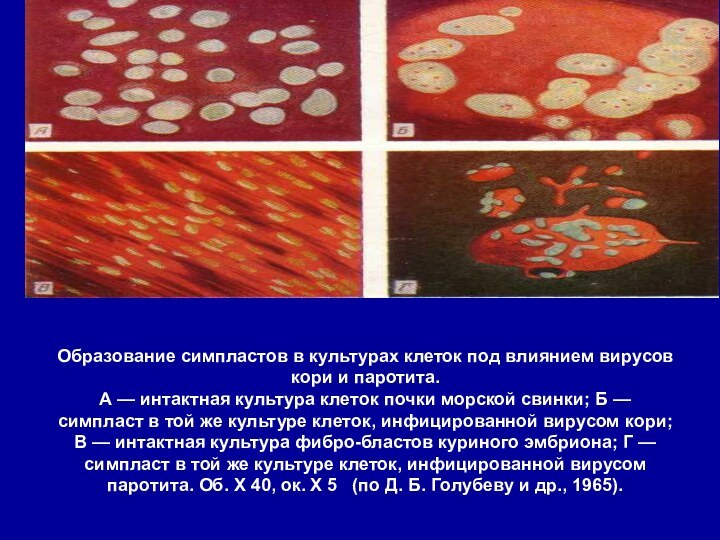
Образование симпластов в культурах клеток под влиянием вирусов
кори и паротита.
А — интактная культура клеток почки морской
свинки; Б — симпласт в той же культуре клеток, инфицированной вирусом кори; В — интактная культура фибро-бластов куриного эмбриона; Г — симпласт в той же культуре клеток, инфицированной вирусом паротита. Об. X 40, ок. X 5 (по Д. Б. Голубеву и др., 1965).
Слайд 34
ВИРУСЫ БАКТЕРИЙ
(БАКТЕРИОФАГИ ИЛИ ФАГИ)
Фаги - вирусы определенных видов
бактерии («пожиратель» бактерий от лат. Phagos - пожирающий).
В
1917 г. французский микробиолог Д'Эррель, наблюдал лизис бактериальной культуры дизентерии.
● Фаги способствуют успешному изучению молекулярной генетики и общей вирусологии: простота культивирования, короткий период генерации, высокий выход фагового потомства, возможность точного его количественного учета
Слайд 35
Номенклатура и биологические особенности
Номенклатура основана на видовом наименовании
хозяина. Например, фаги, лизирующие дизентерийные бактерии, получили название дизентерийных
бактериофагов.
● Структура. Имеют сперматозоидную форму. Состоят из головки, которая содержит нуклеиновую кислоту и отростка.
У некоторых фагов отросток очень короткий или вовсе отсутствует.
Размеры фаговой частицы колеблются от 20 до 200 нм.
Слайд 36
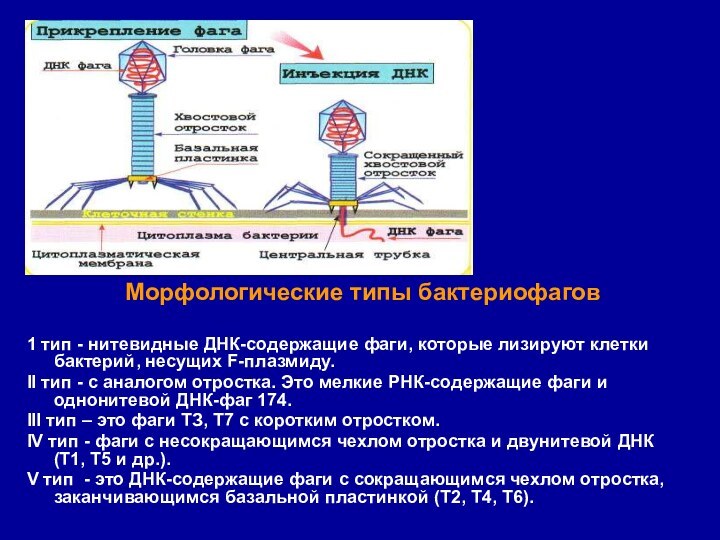
Морфологические типы бактериофагов
1 тип - нитевидные ДНК-содержащие фаги,
которые лизируют клетки бактерий, несущих F-плазмиду.
II тип - с
аналогом отростка. Это мелкие РНК-содержащие фаги и однонитевой ДНК-фаг 174.
III тип – это фаги ТЗ, Т7 с коротким отростком.
IV тип - фаги с несокращающимся чехлом отростка и двунитевой ДНК (Т1, Т5 и др.).
V тип - это ДНК-содержащие фаги с сокращающимся чехлом отростка, заканчивающимся базальной пластинкой (Т2, Т4, Т6).
Слайд 37
● Наиболее изучены Т-фаги (англ. type - типовые).
Они составляют Т-группу коли-дизентерийных фагов: 4 нечетных (Т1, ТЗ,
Т5, Т7) и 3 четных (Т2, Т4, Т6).
● Наиболее сложной структура Т-четных фагов (Т2). Он состоит из головки гексагональной формы и отростка, который образован полым стержнем. Снаружи стержень окружен чехлом, способным к сокращению. На дистальном конце отростка имеется шестиугольная базальная пластинка, в углах которой располагаются короткие зубцы. От каждого зубца отходит по одной нити длиной 150 нм. Базальная пластинка и нити осуществляют процесс адсорбции фага на бактериальной клетке.
Слайд 38
Химический состав
Химический состав. Фаги состоят из нуклеиновой кислоты
(ДНК или РНК) и белка. Большинство их них содержат
двунитевую ДНК в виде кольца. Реже - однонитевые фаги (фаг 174).
Обнаружены ДНК с необычными азотистыми основаниями (у фага Т2 вместо цитозина содержится 5-оксиметилцитозин.
Слайд 39
Капсид головки фага и чехол отростка построены из
полипептидных субъединиц по кубическому (головка) и спиральному (отросток) типу
симметрии.
Под чехлом дистальной части отростка (фаг Т2) содержится фермент лизоцим.
Внутри головки у фага Т2 обнаружен внутренний белок (полиамины -спермин, путресцин) для суперспирализации фаговой ДНК.
●
● Взаимодействие фагов с бактериальной клеткой имеют последовательность как у вирусов животных и человека, но имеются и особенности.
● Адсорбция фага на бактериальной клетке происходит только при соответствии фаговых рецепторов с рецепторами клеточной стенки. Некоторые фаги адсорбируются на половых ворсинках (sex pili), контролируемых F- или R-плазмидами. На протопластах адсорбции фагов не происходит.
Слайд 40
Влияние факторов окружающей среды на фаги.
Фаги более устойчивы
к действию физических и химических факторов, чем многие вирусы
человека. Большинство из них инактивируются при температуре свыше 65°- 70)°С. Переносят замораживание и длительно сохраняются при низких температурах и высушивании.
Ультрафиолетовые лучи и ионизирующая радиация также вызывают инактивирующий эффект, а в низких дозах - мутации.
Слайд 41
На адсорбцию фагов большое влияние оказывают: состав и

рН среды, температура, наличие аминокислот (триптофана для фага Т2)
или других соединений. Некоторые фаги вводят свою ДНК без предварительного повреждения клеточной стенки бактерий, другие - сквозь отверстия, которые они пробуравливают в клеточной стенке с помощью лизоцима, содержащегося в их капсиде.
Репликация фаговой нуклеиновой кислоты и синтез фагоспецифических ферментов транскрипции и репликации происходят примерно так же, как и при репродукции других вирусов. Однако латентный период инфекции, т. е. время для формирования фагового потомства, значительно короче.
Сборка фаговых частиц, или морфогенез, заключается в заполнении фаговой ДНК пустотелых капсид головки.
Выход зрелых фагов из бактериальной клетки происходит путем «взрыва», во время которого зараженные бактерии лизируются. Лизис происходит при участии фагового лизоцима либо без него. Некоторые ДНК-содержащие нитчатые фаги освобождаются из клетки путем «просачивания» ДНК через цитоплазматическую мембрану и клеточную стенку бактерии, во время которого они приобретают капсиды. Бактериальная клетка при этом сохраняет свою жизнеспособность.
Слайд 42
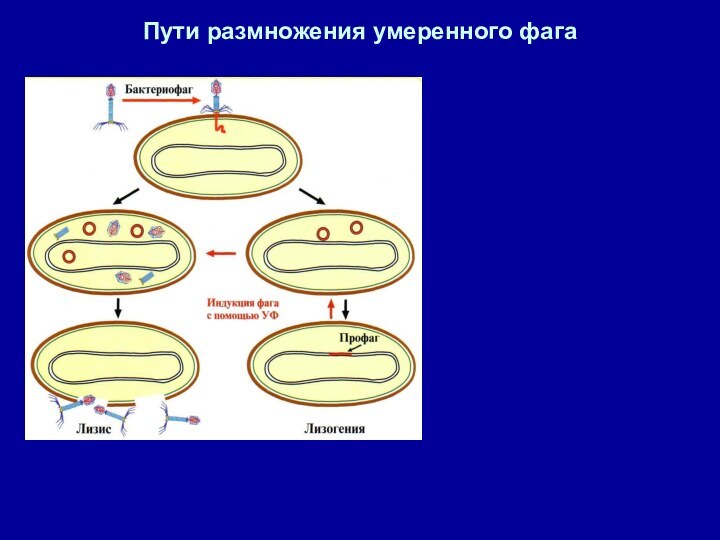
Пути размножения умеренного фага
Слайд 43
Лизогения Фаговая ДНК. ассоциированная с геномом своего хозяина,
носит название профага. Бактериальные клетки, содержащие профаг, называются лизогенными,
а само явление лизогенией. Это название отражает потенциальную способность лизогенных бактерий к лизису при освобождении профага из состава бактериального генома и перехода в вирулентный фаг, способный репродуцироваться.
Фаги, вызывающие данный тип инфекции, получили название умеренных. Они отличаются от вирулентных тем, что встраивают свою ДНК в бактериальный геном, с которым реплицируются.
Спонтанный лизис нередко происходит в отдельных клетках популяции лизогенных бактерий, но не захватывает все клетки. Это связано со способностью лизогенных бактерий приобретать иммунитет к последующему заражению одноименным фагом, вследствие чего остальные лизогенные клетки, содержащиеся в бактериальной популяции, полностью сохраняют свою целостность и жизнеспособность.
Слайд 44
Продукция фагов лизогенными бактериями значительно увеличивается при их

облучении суббактерицидными дозами Уф-лучей или обработке некоторыми химическими соединениями,
взаимодействующими с их ДНК. Данный феномен называется индукцией профага.
Как уже отмечалось, наличие профага в составе бактериального генома не мешает репликации ДНК бактериальной клетки и самого профага. Однако гены профага самостоятельно не транскрибируются, что связано с образованием репрессора - низкомолекулярного белка, блокирующего данный процесс. Синтез репрессора контролируется генами профага. При инактивации репрессора УФ-облучением профаг выходит из состава бактериального генома и превращается в вирулентный фаг, вызывающий продуктивную инфекцию.
Лизогенизация лежит в основе фаговой или лизогенной конверсии. Она заключается в изменении свойств у лизогенных бактерий, например приобретении способности продуцировать токсин, изменять морфологию, антигенные свойства и другие признаки. Механизм этого явления связан с внесением новой информации в бактериальную клетку.
Умеренные фаги могут быть дефектиыми, т.е. неспособными образовывать фаговое потомство, например, трансдуцирующие фаги. Их используют в качестве векторов в генной инженерии.
Слайд 45
Практическое применение бактериофагов.
Строгая специфичность бактериофагов используется

для:
фаготипирования,
дифференцировки бактериальных
культур,
индикации их во внешней среде (например в водоемах).
Метод фаготипирования бактерий применяется в микробиологической практике. Он позволяет не только определить видовую принадлежность исследуемой культуры, но и ее фаготип (фаговар). Это связано с тем, что у бактерий одного и того же вида имеются рецепторы, адсорбирующие строго определенные фаги, которые затем вызывают их лизис. Использование наборов таких типоспецифических фагов позволяет проводить фаготипирование исследуемых культур с целью эпидемиологического анализа инфекционных заболеваний: установления источника инфекции и путей ее передачи.
Кроме того, по наличию фагов во внешней среде (водоемах) можно судить о содержании в них соответствующих бактерий, представляющих опасность для здоровья человека. Данный метод индикации патогенных бактерий также применяется в эпидемиологической практике. Его эффективность повышается при постановке реакции нарастания титра фага, которая основана на способности специфических линий фагов репродуцироваться на строго определенных бактериальных культурах. При внесении такого фага в исследуемый материал, содержащий искомый возбудитель, происходит нарастание его титра. Широкое использование реакции нарастания титра фага осложняется трудностью получения индикаторных наборов фагов.
Слайд 46
Применение фагов с лечебными и профилактическими целями проводится

сравнительно редко. Это связано с большим количеством отрицательных результатов,
которые объясняются следующими причинами:
1) строгой специфичностью фагов, лизирующих только те клетки бактериальной популяции, которые снабжены соответствующими рецепторами, вследствие чего фагорезистентные особи, имеющиеся в каждой популяции, полностью сохраняют свою жизнеспособность;
2) широким применением более эффективных этиотропных средств - антибиотиков, не обладающих специфичностью бактериофагов.
Выпускаются препараты дизентерийного, сальмонеллезных, коли-протейного, стафилококкового и других бактериофагов.
Выпускаются наборы для фаготипирования брюшнотифозных бактерий, стафилококков, которые применяются с эпидемиологическими целями для установления источника инфекции. Например, в случае выделения от разных больных бактериальных культур, принадлежащих не только к одному виду, но и к одному фаготипу, можно считать, что они заразились из одного и того же источника инфекции. В случае выделения разных фаготинов следует искать несколько источников инфекции.
Препараты бактериофагов применяются для лечения дизентерии, сальмонеллеза, гнойной инфекции, вызванных антибиотикорезистентными бактериями. В каждом случае предварительно определяют чувствительность выделенных возбудителей к данному препарату бактериофага.
Сальмонеллезные фаги применяются для профилактики салмонеллезов заболевания в детских коллективах.