Слайд 2
Открытие атома.
Мысль о том, что все разнообразие веществ
в природе состоит из мельчайших и невидимых глазу частиц,
не поддающихся дальнейшему дроблению, приходила ещё в голову мудрецам Древнего Востока, Индии, Китая, Греции.
«Атом»(греч.)- неделимый. ( Демокрит, 4 в. до н. э.)
Слайд 3
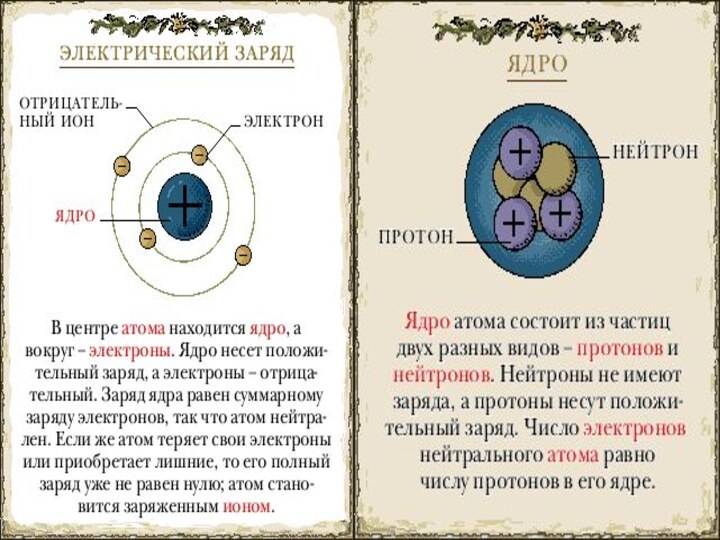
Электрон.
Открывателем электрона считают английского физика Дж. Дж. Томсона
(1897г.; нобелевская премия 1906г).
Точные первые измерения электрического заряда электрона
провел в 1909 г. американский физик Роберт Милликен.
Слайд 4
Первооткрыватель электрона.
- английский физик, основатель
научной школы, член и президент Лондонского Королевского общества, иностранный
член-корреспондент Петербургской АН и иностранный почетный член АН СССР. Директор Кавендишской лаборатории. Исследовал прохождение электрического тока через разреженные газы. Открыл (1897) электрон и определил (1898) его заряд. Предложил (1903) одну из первых моделей атома. Один из создателей электронной теории металлов. Нобелевская премия (1906).
ТОМСОН Джозеф Джон (1856-1940)
Слайд 6
Первыми изучали внутреннюю структуру атома английский физик Э.Резерфорд
и его студенты Э. Марсден и X. Гейгер.
— великий английский физик, уроженец Новой Зеландии. Своими экспериментальными открытиями Резерфорд заложил основы современного учения о строении атома и радиоактивности. Он первым исследовал состав излучения радиоактивных веществ. Резерфорд открыл атомное ядро и впервые осуществил искусственное превращение атомных ядер. Все поставленные им опыты носили фундаментальный характер, отличались исключительной простотой и ясностью.
Резерфорд Эрнест (1871 —1937)
«Теперь я знаю, как выглядит атом!»
Резерфорд, 1911 г.
Слайд 7
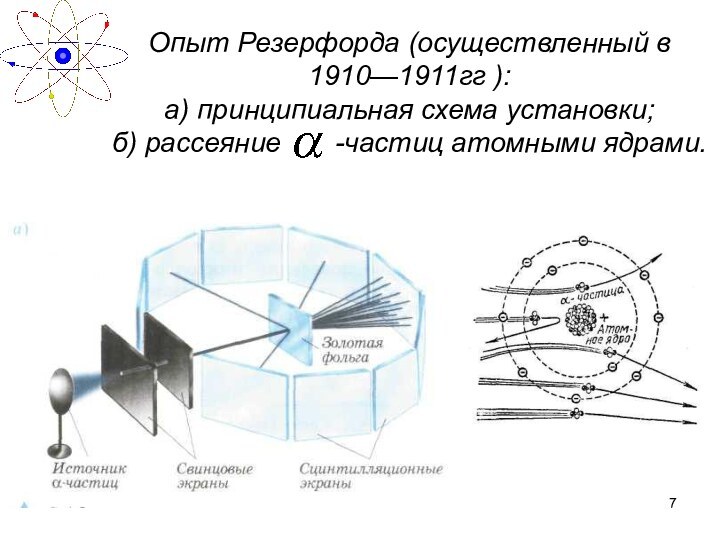
Опыт Резерфорда (осуществленный в 1910—1911гг ):
а) принципиальная схема
установки;
б) рассеяние -частиц атомными ядрами.
Слайд 8
Объяснение результатов опыта:
Т.к. большинство - частиц
не изменяли траекторию своего движения, то это говорит о
том, что атомы не сплошные, большой объём атомов представляет собой пустоту.
Т.к. часть - частиц меняли траекторию своего движения, то это говорит о том, что в центре атома находится «нечто», имеющее массу, сравнимую с массой - частиц, и положительно заряженное – только при этих условиях это «нечто» могло изменить траекторию движения - частиц. Это «нечто» было названо ядром атома.
Слайд 9
Квантовые постулаты Бора.
— великий датский
физик. Создал первую квантовую теорию атома и затем принял
самое активное участие в разработке основ квантовой механики. Наряду с этим Бор внес большой вклад в теорию атомного ядра и ядерных реакций. Он, в частности, развил теорию деления атомных ядер, в процессе которого выделяется огромная энергия. В Копенгагене Бор создал большую интернациональную школу физиков и много сделал для развития сотрудничества между физиками всего мира. Бор активно участвовал в борьбе против атомной угрозы человечеству.
Бор Нильс (1885—1962)
Слайд 10
Постулаты:
Первый постулат Бора гласит: атомная система может находиться
только в особых стационарных, или квантовых, состояниях, каждому из
которых соответствует определенная энергия Еn; в стационарном состоянии атом не излучает.
Согласно второму постулату Бора (правило частот) излучение света происходит при переходе атома из стационарного состояния с большей энергией Ek в стационарное состояние с меньшей энергией Еn. Энергия излученного фотона равна разности энергий стационарных состояний:
Третий постулат Бора (правило квантования орбит) гласит: электроны могут двигаться вокруг ядра только по строго определенным орбитам, радиус которых определяется по формуле:
Слайд 11
Обозначение ядер химического элемента.
Х – символ химического элемента
в таблице Д.И.Менделеева.
А – массовое число (равно относительной атомной
массе элемента в таблице Д.И.Менделеева).
Z – число протонов (равно порядковому номеру элемента в таблице Д.И.Менделеева).
Ядро кремния, в состав которого входят 14 протонов и 14 нейтронов (28-14).
ПРИМЕР:
N – число нейтронов.
Слайд 12
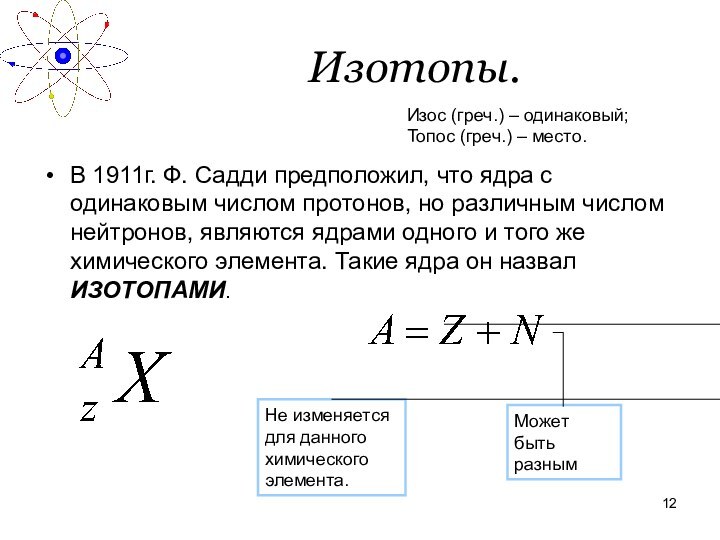
Изотопы.
В 1911г. Ф. Садди предположил, что ядра с
одинаковым числом протонов, но различным числом нейтронов, являются ядрами
одного и того же химического элемента. Такие ядра он назвал ИЗОТОПАМИ.
Изос (греч.) – одинаковый;
Топос (греч.) – место.
Слайд 13
Изотопы водорода.
Легкий водород (в ядре 1
протон). При соединении с кислородом образуют обыкновенную воду, которая
при нормальном атмосферном давлении кипит при 1000С и замерзает при 00С.
Тяжелый водород (в ядре 1 протон и 1 нейтрон). При соединении с кислородом образуют тяжелую воду, которая при нормальном атмосферном давлении кипит при 101,20С и замерзает при 3,80С.
Сверхтяжелый водород (в ядре 1 протон и 2 нейтрона). Радиоактивен, излучает быстродвижущиеся - частицы. Период полураспада 12 лет.
Слайд 14
Дефект масс.
Дефектом масс называют разность между
суммарной массой всех нуклонов в свободном состоянии и массой
ядра.
Слайд 15
Радиоактивность.
Явление радиоактивности было случайно открыто в 1896г. французским
ученым Беккрелем, обнаружившим самопроизвольное излучение ураном невидимых глазу лучей,
действующие на фотопленку.
Этим явлением заинтересовались французские ученые Пьер и Мария Кюри. Они обнаружили самопроизвольное излучение Тория, Полония и Радия.
Радий давал очень сильное излучение, поэтому в честь него явление самопроизвольного излучения было названо супругами Кюри РАДИОАКТИВНОСТЬЮ или РАДИАЦИОННЫМ ИЗЛУЧЕНИЕМ.
Слайд 16
Мария Кюри была первой женщиной, удостоенной в 1903
г. Нобелевской премии в области физики. По окончании Парижского
университета Мария получила сразу два диплома: в 1893 г. она стала специалистом по естественным наукам, в 1894 г. — по химии. Кроме того, она, первая из женщин-исследователей, стала профессором Сорбонны, самого известного университета Франции. В 1911 г. она стала первым ученым, который получил вторую Нобелевскую премию (на этот раз в области химии). Работая в лаборатории вместе с мужем, она не получала жалованья. Ее имя поначалу исключили из списка кандидатур на первую Нобелевскую премию. Когда Марию Кюри представили ко второму награждению, аргументы ее противников, оспаривавших значительность ее вклада в науку, были исчерпаны.
Слайд 17
Лауреатами Нобелевской премии
в 1903 г. стали три человека.
Вместе
с супругами Кюри премией был награжден француз, который открыл
явление радиоактивности, обнаружив излучение солей урана.
Слайд 18
На многих фотографиях Мария Кюри
запечатлена со своей старшей дочерью Ирен. Их объединял интерес
к науке, и особенно к явлению радиоактивности. Мать и дочь и внешне были похожи: скромное платье, утомленное лицо и непослушные волосы. Эти женщины, подчинившие свою жизнь служению науке, были почти уничтожены ею — они обе умерли от тяжелой формы лейкемии, вызванной частым облучением.
В Первую мировую войну Мария и Ирен вместе работали над реализацией проекта — создания мобильной рентгенологической службы — бригады машин, которые перевозили по фронтам рентгеновские установки. В 1935 г. Ирен вместе с мужем Фредериком Жолио была удостоена Нобелевской премии в области физики, так же как когда-то ее родители.
Слайд 19
Виды радиоактивного излучения.
- лучи – поток
положительно заряженных ядер гелия движущихся со скоростью
.
- лучи – поток быстродвижущихся электронов со скоростью .
- лучи – электромагнитные волны с очень маленькой длиной волны
Слайд 20
Виды радиоактивности.
Устойчивыми, стабильными являются лишь атомные ядра с
энергией связи нуклонов, большей суммарной энергии связи нуклонов в
продуктах распада.
Различают естественную и искусственную радиоактивность.
Естественная радиоактивность — радиоактивность, наблюдаемая у неустойчивых изотопов, существующих в природе.
Искусственная радиоактивность — радиоактивность изотопов, полученных искусственно при ядерных реакциях.
Нестабильными радиоактивными являются тяжелые ядра с зарядовым числом Z > 83 или массовым числом А > 209, которые могут спонтанно распадаться.
Слайд 21
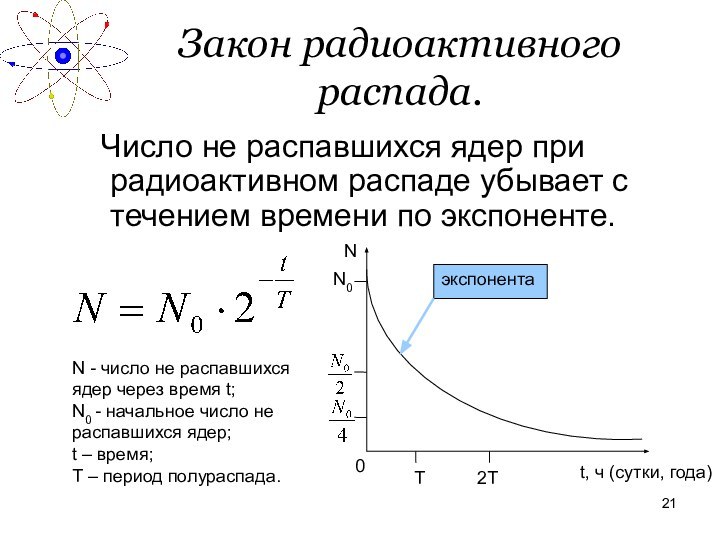
Закон радиоактивного распада.
Число не распавшихся ядер при
радиоактивном распаде убывает с течением времени по экспоненте.
N
N0
0
Т
2Т
t, ч
(сутки, года)
экспонента
N - число не распавшихся ядер через время t;
N0 - начальное число не распавшихся ядер;
t – время;
Т – период полураспада.
Слайд 22
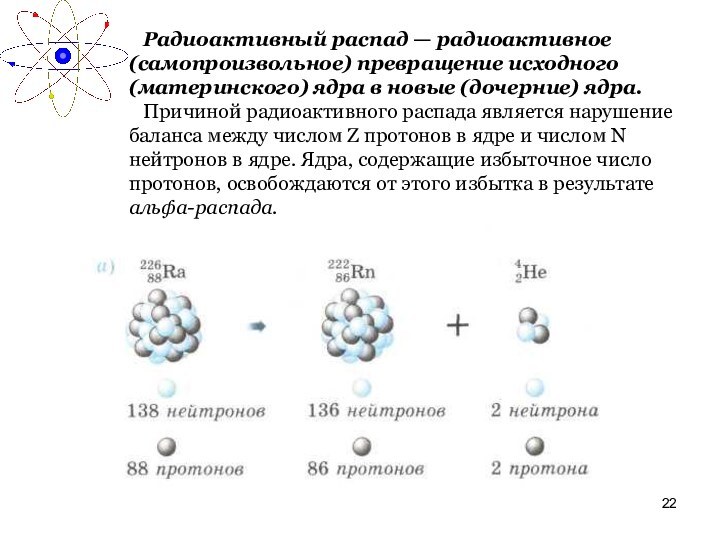
Радиоактивный распад — радиоактивное (самопроизвольное) превращение исходного (материнского)
ядра в новые (дочерние) ядра.
Причиной радиоактивного распада является нарушение
баланса между числом Z протонов в ядре и числом N нейтронов в ядре. Ядра, содержащие избыточное число протонов, освобождаются от этого избытка в результате альфа-распада.
Слайд 23
Процесс деления ядра:
а)взаимодействие нейтрона с ядром; б)захват нейтрона
ядром; в)колебание возбужденного ядра; г)образование осколков деления
Слайд 24
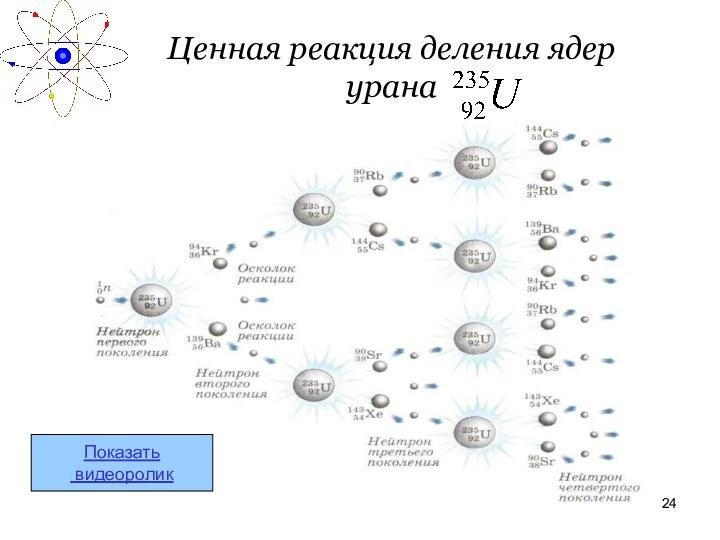
Ценная реакция деления ядер
урана
Показать
видеоролик
Слайд 25
Ядерный реактор.
Для стабильной цепной ядерной
реакции, необходимо создать условия, в которых при делении ядра,
поглотившего один нейтрон, будет выделяться частица, необходимая для деления следующего ядра. Устройство, в котором осуществляется управляемая цепная реакция деления тяжелых ядер, называется ядерным реактором.
Слайд 26
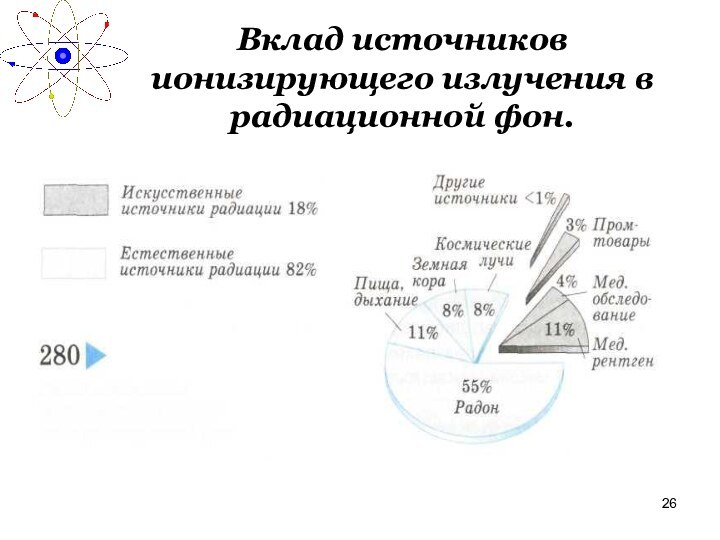
Вклад источников ионизирующего излучения в радиационной фон.
Слайд 27
Ядерной бомбой
Современный вид оружия, обладающий огромной разрушительной силой,
в котором взрыв происходит под действием энергии, выделяющейся при
делении ядер атома. Помимо действия сильнейшей ударной волны, которая образуется при взрыве, поражающим действием является радиоактивное заражение местности в районе взрыва, которое сохраняется в течение нескольких лет.