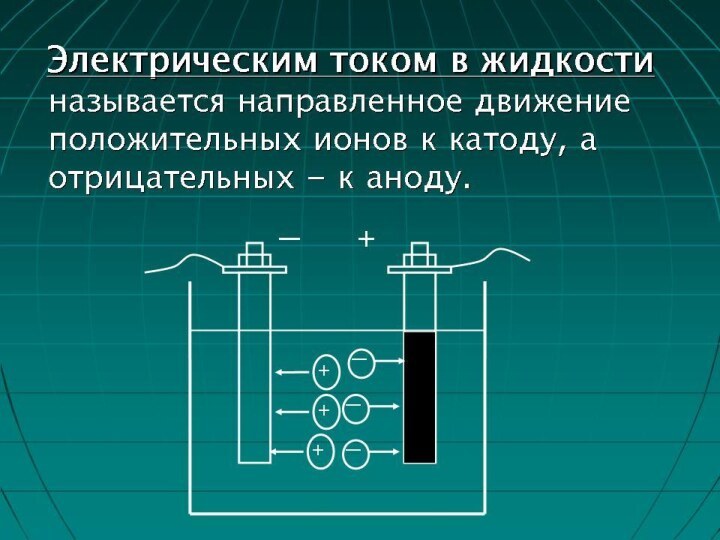
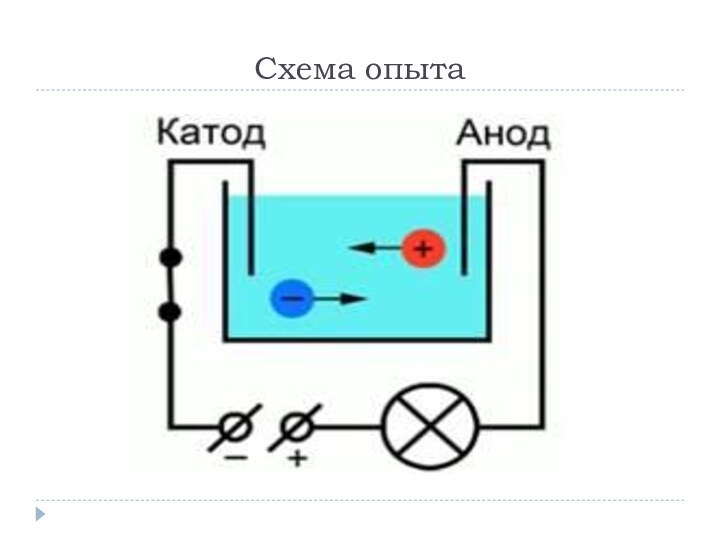
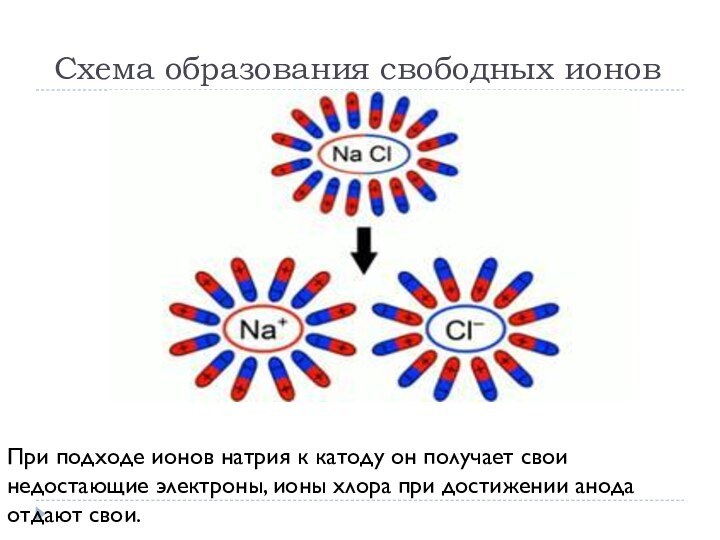
полупроводниками и диэлектриками. Речь пойдет о жидкостях-проводниках. Причем не о
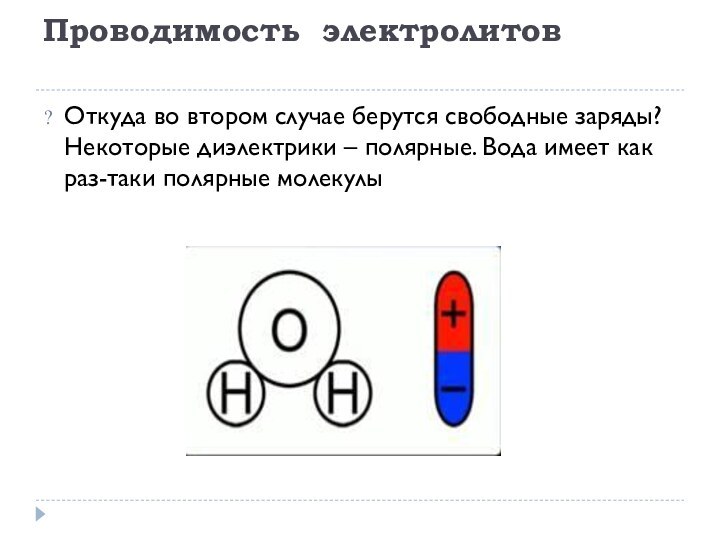
жидкостях с электронной проводимостью (расплавленные металлы), а о жидкостях-проводниках второго рода (растворы и расплавы солей, кислот, оснований). Тип проводимости таких проводников – ионный.Проводники второго рода – такие проводники, в которых при протекании тока происходят химические процессы.