- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Электролиз
Содержание
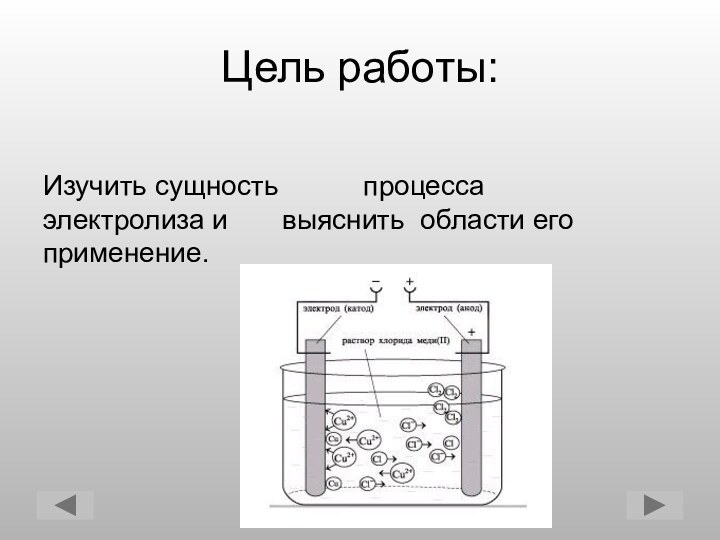
- 2. Цель работы: Изучить сущность
- 3. Содержание:Электролиз расплаваЭлектролиз раствораСхема электролизаСущность электролизаПрименение электролизаВыводыИсточники информации
- 4. Электролиз расплава Если расплавить поваренную
- 5. Примеры электролиза расплавов:Электролиз- окислительно-восстановительный процесс, который возникает
- 6. Электролиз раствора В водных растворах
- 7. Электролиз раствора
- 8. Электролиз воды проводится всегда в присутствии инертного
- 10. Сущность электролиза В результате электролиза
- 11. Восстановительный процесс на катоде в водных растворах:Катионы
- 12. Электрическая энергияХимическая энергияЭлектролиз
- 13. Преимущества электролиза
- 14. Электрохимическое процессы широко применяют в различных областях
- 15. Выводы
- 16. Скачать презентацию
- 17. Похожие презентации













Слайд 3
Содержание:
Электролиз расплава
Электролиз раствора
Схема электролиза
Сущность электролиза
Применение электролиза
Выводы
Источники информации
Слайд 4
Электролиз расплава
Если расплавить поваренную соль,
то произойдет расщепление кристаллической решетки на ионы. При этом
образуются катионы натрия и анионы хлора:NaCI -> Na+ + CI-
Опустим в расплав электроды постоянного электрического тока.
Направляясь к катоду, катион натрия получает с него один электрон, т.е. происходит восстановление:
Na+ + ē -> Na0
Катод, на котором имеется постоянный избыток электронов, является восстановителем.
К аноду направляется анион хлора. Поскольку на аноде постоянный недостаток электронов, ион хлора отдает электрон, превращаясь в нейтральный атом, т.е. окисляется:
Cl- - ē -> Cl0
Анод, на котором постоянный недостаток электронов, является окислителем.
2NaCl -> 2 Na + Cl2
ЭЛЕКТРОЛИЗ – окислительно-восстановительный процесс, протекающий под действием электрического тока.
Слайд 5
Примеры электролиза расплавов:
Электролиз- окислительно-восстановительный процесс, который возникает на
электродах при прохождении электрического тока через раствор или расплав
электролита.На катоде(-) -восстановление
На аноде(+) -окисление
Li+, K+, Ca2+, Na+, Mg2+, Al3+, Zn2+, Cr3+, Fe2+, Ni2+, Sn2+, Pb2+, H+, Cu2+, Hg2+, Ag+, Pt4+, Au3+.
Для солей неактивных металлов и бескислородных кислот(CuCl2) электролиз раствора и расплава соли одинаков.
Увеличение окислительной активности ионов
F-, NO3-, SO42-, OH-, Cl-, Br-, I-, S2-
Увеличение восстановительной активности ионов
Слайд 6
Электролиз раствора
В водных растворах процесс
приобретает ряд особенностей, так как в нем принимает участие
вода.В растворе, помимо диссоциации соли, происходит весьма слабая диссоциация воды.
NaCI -> Na+ + CI-
H2O -> H+ + OH-
Таким образом, в растворе образуется два вида катионов (Na+ и H+) и два вида анионов (CI- и OH-).
В ряду напряжений металлов натрий стоит намного левее водорода. Следовательно, восстановительные свойства атома натрия сильнее, чем атома водорода. Зато окислительные свойства иона Na+ выражены слабее, чем иона H+ , следовательно, на катоде будет восстанавливаться не металлический натрий, а водород:
2H2O + 2ē -> H2 + 2OH-
Ионы натрия будут находиться в растворе до тех пор, пока полностью не разрядятся ионы водорода.
К аноду направятся анионы CI- и OH-, восстановительные свойства которых также неодинаковы (см. ряд анионов, расположенных в порядке увеличения способности к окислению). Анионы CI- окисляются легче, чем OH-, поэтому на аноде будет происходить процесс:
CI- - ē → CI0
Слайд 7
Электролиз раствора
К
аноду направятся анионы CI- и OH-, восстановительные свойства которых
также неодинаковы (см. ряд анионов, расположенных в порядке увеличения способности к окислению). Анионы CI- окисляются легче, чем OH-, поэтому на аноде будет происходить процесс:CI- - ē CI0, 2CI0 CI2
В большинстве случаев анионы, состоящие из атомов одного элемента, такие, как CI-, Br-, I-, S2-, окисляются на аноде быстрее, чем гидроксид-ион.
При электролизе раствора поваренной соли на электродах получаются водород и хлор, а в растворе остаются ионы Na+ и OH-. Эти ионы представляют собой в диссоциированном виде едкий натр NaOH.Таким способом в промышленности получают едкие щелочи.
2NaCl + 2H2O H2 + Cl2 + 2NaOH
Слайд 8 Электролиз воды проводится всегда в присутствии инертного электролита
(для увеличения электропроводности очень слабого электролита - воды):
В зависимости
от инертного электролита электролиз проводится в нейтральной, кислотной или щелочной среде. При выборе инертного электролита необходимо учесть, что никогда не восстанавливаются на катоде в водном растворе катионы металлов, являющихся типичными восстановителями (например Li+, Cs+, K+, Ca2+, Na+, Mg2+, Al3+) и никогда не окисляется на аноде кислород O−II анионов оксокислот с элементом в высшей степени окисления (например ClO4−, SO42−, NO3−, PO43−, CO32−, SiO44−, MnO4−), вместо них окисляется водаСлайд 9
Примеры электролиза растворов солей:
на аноде
окисляются анионы Сl, а не кислород O молекул воды, так как электроотрицательность хлора меньше, чем кислорода, и следовательно, хлор отдает электроны легче, чем кислородна катоде восстанавливаются катионы Cu, а не водород H молекул воды, так как медь стоит правее водорода в ряду напряжений, то есть легче принимает электроны, чем H в воде
Слайд 10
Сущность электролиза
В результате электролиза на
электродах (катоде и аноде) выделяются соответствующие продукты восстановления и
окисления, которые в зависимости от условий могут вступать в реакции с растворителем, материалом электрода и т.п., так называемые вторичные процессы Для осуществления электролиза к отрицательному полюсу внешнего источника постоянного тока присоединяют катод, а к положительному полюсу - анод, после чего погружают их в электролизер с раствором или расплавом электролита
Слайд 11
Восстановительный процесс на катоде в водных растворах:
Катионы металлов
со стандартным электродным потенциалом, больше, чем у водорода, расположены
в ряду стандартных электродных потенциалов после него: Cu2+;Zn2+;Cr3+;Fe2+;…; до Pt4+. При электролизе они почти полностью восстанавливаются на катоде и выделяются в виде металла.Катионы металлов с малой величиной стандартного электродного потенциала (металлы начала ряда Li+;Na+;K+;Rb+;…; до Al3+ включительно). При электролизе на катоде они не восстанавливаются, вместо них восстанавливаются молекулы воды.
Катионы металлов со стандартным электродным потенциалом меньшим, чем у водорода, но большим, чем у алюминия (Mn2+;Zn2+;Cr3+;Fe2+;…; до H). При электролизе эти катионы, характеризующиеся средними значениями электроноакцепторной способности, на катоде восстанавливаются одновременно с молекулами воды.
При электролизе кислородосодержащих кислот и их солей (SO4 2- ; NO3-;PO43- и т.п.) с максимальной степенью окисления неметалла на аноде окисляются не анионы, а молекулы воды с выделением кислорода.
Сущность электролиза
Слайд 12
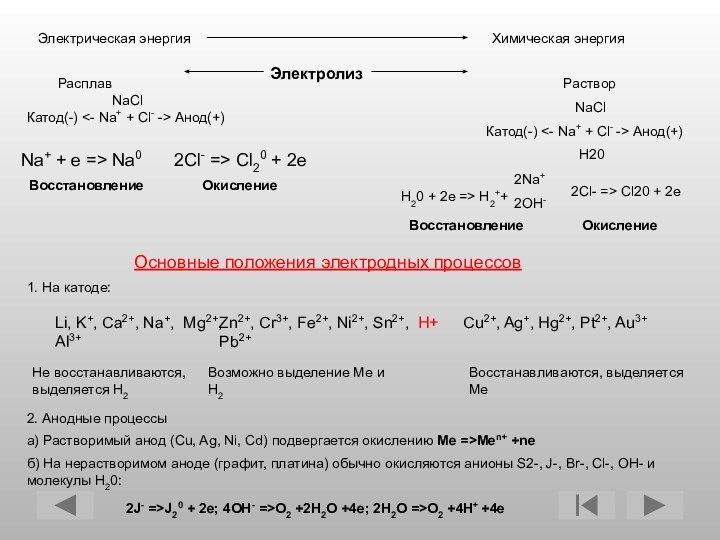
Электрическая энергия
Химическая энергия
Электролиз
Раствор
NaClКатод(-) <- Na+ + Cl- -> Анод(+)
H20
Расплав
NaCl
Катод(-) <- Na+ + Cl- -> Анод(+)
Na+ + e => Na0
2Cl- => Cl20 + 2e
Восстановление Окисление
H20 + 2e => H2++
2Na+
2OH-
2Cl- => Cl20 + 2e
Восстановление Окисление
Основные положения электродных процессов
1. На катоде:
Li, K+, Ca2+, Na+, Mg2+, Al3+
Zn2+, Cr3+, Fe2+, Ni2+, Sn2+, Pb2+
Cu2+, Ag+, Hg2+, Pt2+, Au3+
H+
Не восстанавливаются, выделяется H2
Возможно выделение Me и H2
Восстанавливаются, выделяется Me
2. Анодные процессы
а) Растворимый анод (Cu, Ag, Ni, Cd) подвергается окислению Me =>Men+ +ne
б) На нерастворимом аноде (графит, платина) обычно окисляются анионы S2-, J-, Br-, Cl-, OH- и молекулы H20:
2J- =>J20 + 2e; 4OH- =>O2 +2H2O +4e; 2H2O =>O2 +4H+ +4e
Слайд 13 Преимущества электролиза перед
химическим методами получения целевых продуктов
заключаются в возможности сравнительно
просто (регулируя ток) управлять скоростью и селективной направленностью реакций. Условия электролиза легко контролировать, благодаря чему можно осуществлять процессы как в самых "мягких", так и в наиболее "жёстких" условиях окисления или восстановления, получать сильнейшие окислители и восстановители, используемые в науке и технике. Электролиз - основной метод промышленного производства алюминия, хлора и едкого натра, важнейший способ получения фтора, щелочных и щелочноземельных металлов, эффективный метод рафинирования металлов.
Применение электролиза
Путём электролиза воды производят водород и кислород. Электрохимический метод используется для синтеза органических соединений различных классов и многих окислителей (персульфатов, перманганатов, перхлоратов, перфторорганических соединений и др.).
Применение электролиза для обработки поверхностей включает как катодные процессы гальванотехники (в машиностроении, приборостроении, авиационной, электротехнической, электронной промышленности), так и анодные процессы полировки, травления, размерной анодно-механической обработки, оксидирования (анодирования) металлических изделий (см. также Электрофизические и электрохимические методы обработки).
Путём электролиза в контролируемых условиях осуществляют защиту от коррозии металлических сооружений и конструкций (анодная и катодная защита).
Слайд 14 Электрохимическое процессы широко применяют в различных областях современной
техники, в аналитической химии, биохимии и т.д.
В химической промышленности электролизом получают хлор и фтор, щелочи, хлораты и перхлораты, надсерную кислоту и персульфаты, химически чистые водород и кислород и т.д. При этом одни вещества получают восстановлением на катоде (альдегиды, парааминофенол и др.), другие электроокислением на аноде (хлораты, перхлораты, перманганат калия и др.) Гальванотехника - область прикладной электрохимии, занимающаяся процессами нанесения металлических покрытий на поверхность как металлических, так и неметаллических изделий при прохождении постоянного электрического тока через растворы их солей. Гальванотехника подразделяется на гальваностегию и гальванопластику.
Гальваностегия- электроосаждение на поверхность металла другого металла, который прочно связывается(сцепляется) с покрываемым металлом(предметом), служащим катодом электролизера.
Гальванопластика- получение путем электролиза точных, легко отделяемых металлических копий относительно значительной толщины с различных как неметаллических, так и металлических предметов, называемых матрицами. Гальванопластику используют для нанесения сравнительно толстых металлических покрытий на другие металлы (например, образование «накладного слоя никеля, серебра, золота и т.д.).
Слайд 15
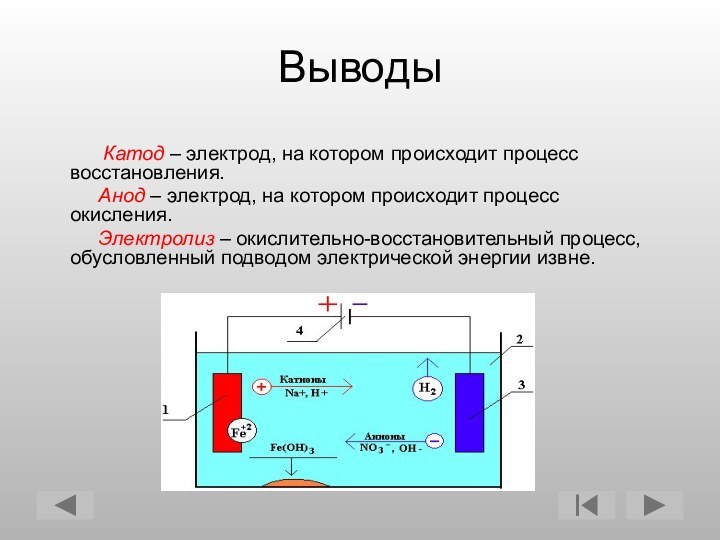
Выводы
Катод – электрод, на котором происходит процесс восстановления.
Анод – электрод, на котором происходит процесс окисления. Электролиз – окислительно-восстановительный процесс, обусловленный подводом электрической энергии извне.