Слайд 2
МОЛЕКУЛЯРНАЯ
ФИЗИКА
ТЕРМОДИНАМИКА
Т П У
Доцент кафедры
Общей физики
Кузнецов Сергей Иванович
Сегодня
Слайд 3
Тема 4
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Слайд 4
4.1. Внутренняя энергия.
Работа и теплота
Наряду с механической энергией любое тело (или система) обладает
внутренней энергией. Внутренняя энергия – энергия покоя.
Она складывается из
- теплового хаотического движения молекул,
- потенциальной энергии их взаимного расположения,
- кинетической и потенциальной энергии электронов в атомах, нуклонов в ядрах и так далее.
Слайд 5
В термодинамических процессах изменяется только кинетическая энергия движущихся
молекул (тепловой энергии недостаточно, чтобы изменить строение атома, а
тем более ядра).
Следовательно, фактически под внутренней энергией в термодинамике подразумевают энергию теплового хаотического движения молекул.
В термодинамике важно знать не абсолютное значение внутренней энергии,
а её изменение.
Слайд 6
Внутренняя энергия U одного моля идеального газа равна:
или
Таким образом, внутренняя энергия зависит только от температуры.
Внутренняя энергия U является функцией состояния системы независимо от предыстории
Слайд 7
Понятно, что в общем случае термодинамическая система может
обладать как внутренней, так и механической энергией и разные
системы могут обмениваться этими видами энергии. Обмен механической энергией характеризуется совершённой работой А, а обмен внутренней энергией – количеством переданного тепла Q.
Слайд 8
Например, зимой вы бросили в снег горячий камень.
За счёт запаса потенциальной энергии совершена механическая работа по
смятию снега, а за счёт запаса внутренней энергии снег был растоплен.
Если же камень был холодный, т.е. температура камня равна температуре среды, то будет совершена только работа, но не будет обмена внутренней энергией.
Слайд 9
Итак, работа и теплота не есть особые формы
энергии.
Нельзя говорить о запасе теплоты или работы. Это
мера переданной другой системе механической или внутренней энергии. О запасе этих энергий можно говорить.
Механическая энергия может переходить в тепловую энергию и обратно. Например, если стучать молотком по наковальне, то через некоторое время молоток и наковальня нагреются (пример диссипации энергии)
Слайд 10
Можно найти ещё массу примеров диссипации или превращения
одной формы энергии в другую.
Опыт показывает, что во всех
случаях, превращение механической энергии в тепловую и обратно совершается всегда в строго эквивалентных количествах.
В этом и состоит суть первого начала термодинамики, следующая из закона сохранения энергии.
Слайд 11
Количество теплоты, сообщаемой телу, идёт на
увеличение внутренней энергии и на совершение телом работы:
(4.1.1)
– это и есть первое начало термодинамики или закон сохранения энергии в термодинамике.
если тепло передаётся от окружающей среды данной
системе, и если система производит работу над окружающими телами, при этом . Учитывая правило знаков, первое начало термодинамики можно записать в виде:
– изменение внутренней энергии тела равно разности сообщаемой телу теплоты и произведённой телом работы.
Слайд 14
Закон сохранения энергии для малого изменения состояния системы
будет иметь вид:
(4.1.2)
U – функция состояния системы;
dU – её полный дифференциал, а
δQ и δА таковыми не являются.
Слайд 15
В каждом состоянии система обладает
определенным и только таким значением внутренней энергии, поэтому можно
записать
Так как U – функция состояния, то
Этот справедливо для любой функции состояния.
Слайд 16
Теплота Q и работа А зависят от того,
каким образом совершен переход из состояния 1 в состояние
2 (изохорически, адиабатически), а внутренняя энергия U не зависит.
При этом нельзя сказать, что система, обладает определенным для данного состояния значением теплоты и работы.
Количество теплоты Q выражается в тех же единицах, что работа и энергия, т.е. в джоулях [Q] = Дж.
Слайд 17
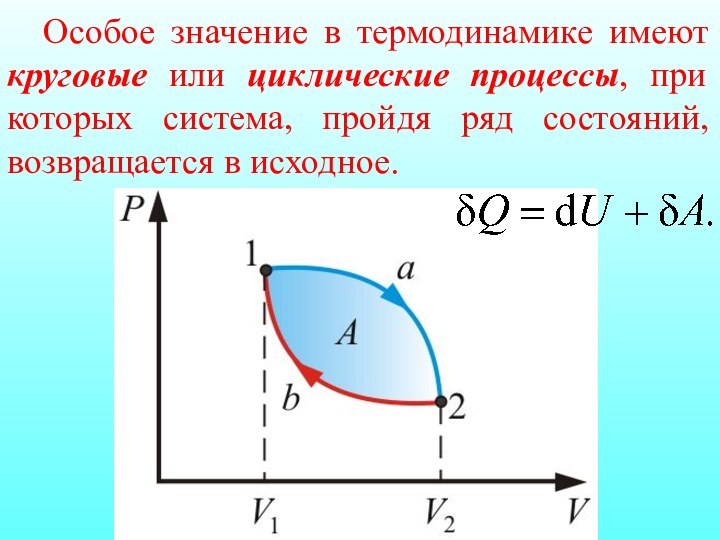
Особое значение в термодинамике имеют круговые или циклические
процессы, при которых система, пройдя ряд состояний, возвращается в
исходное.
то согласно первому началу термодинамики
т.е. нельзя построить периодически действующий двигатель, который совершал бы бóльшую работу, чем количество сообщенной ему извне энергии. Иными словами, вечный двигатель первого рода невозможен.
Это одна из формулировок первого начала термодинамики.
Слайд 19
К недостаткам первого начала следует отнести
то, что: первое начало термодинамики не указывает, в каком
направлении идут процессы изменения состояния.
Слайд 20
4.2. Теплоёмкость идеального газа.
Теплоёмкость тела
характеризуется количеством теплоты, необходимой для нагревания этого тела на
один градус
(4.2.1)
Размерность теплоемкости: [C] = Дж/К.
Теплоёмкость – величина неопределённая, поэтому пользуются понятиями удельной и молярной теплоёмкости.
Слайд 21
Удельная теплоёмкость Суд – есть количество теплоты,
необходимое для нагревания единицы массы вещества на
1 градус
[Cуд] = Дж/К.
Для газов удобно пользоваться молярной теплоемкостью Сμ количество теплоты, необходимое для нагревания
1 кмоля газа на 1 градус
(4.2.2)
[Cμ] = Дж/(мольК).
Слайд 22
Молярная масса – масса одного
моля:
где А – атомная масса; mед атомная
единица массы; NА число Авогадро Моль μ – количество вещества, в котором содержится число молекул, равное числу атомов в 12 г изотопа углерода 12С.
Слайд 23
Теплоёмкость термодинамической системы зависит от того, как изменяется
состояние системы при нагревании.
Если газ нагревать при постоянном объёме,
то всё подводимое тепло идёт на нагревание газа, то есть изменение его внутренней энергии.
Теплоёмкость при постоянном объёме СV
Слайд 24
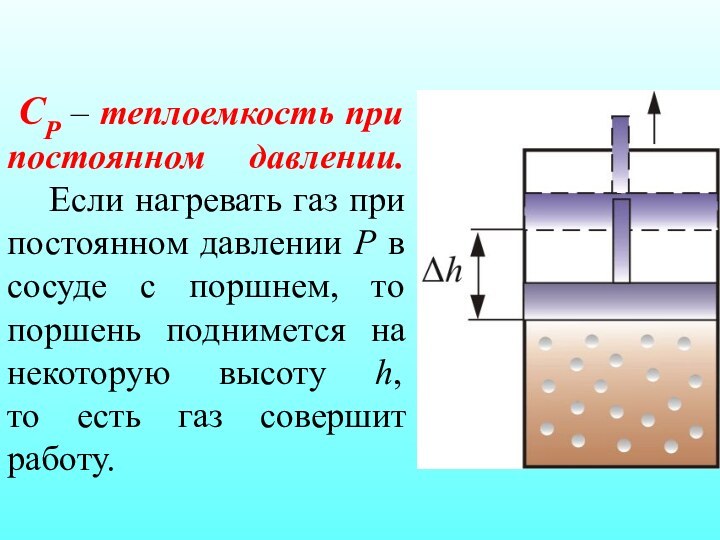
СР – теплоемкость при постоянном давлении.
Если нагревать газ при постоянном давлении Р в сосуде
с поршнем, то поршень поднимется на некоторую высоту h,
то есть газ совершит работу.
Слайд 26
Следовательно, проводимое тепло затрачивается и на нагревание и
на совершение работы. Отсюда ясно, что
Итак, проводимое тепло и теплоёмкость зависят от того, каким путём осуществляется передача тепла. Следовательно Q и С не являются функциями состояния. Величины СР и СV оказываются связанными простыми соотношениями. Найдём их.
Слайд 27
Пусть мы нагреваем один моль идеального
газа при постоянном объёме. Тогда, первое начало термодинамики, запишем
в виде:
(4.2.3)
т.е. бесконечно малое приращение количества теплоты , равно приращению внутренней энергии dU.
Теплоемкость при постоянном объёме будет равна:
(4.2.4)
так как U может зависеть не только от температуры.
В случае идеального газа справедлива формула
Из этого следует, что
Слайд 29
Внутренняя энергия идеального газа является только функцией температуры
(и не зависит от V, Р и тому подобным),
поэтому формула справедлива для любого процесса.
Для произвольной массы идеального газа:
(4.2.6)
Слайд 30
При изобарическом процессе кроме увеличения внутренней энергии происходит
совершение работы газом:
(4.2.7)
Из основного уравнения молекулярно-кинетической теории
При изобарическом процессе Р = const.
Тогда получим:
(4.2.8)
Слайд 31
Это уравнение Майера для одного моля газа. Из
него следует, что физический смысл универсальной газовой постоянной в
том, что R – численно равна работе, совершаемой одним молем газа при нагревании на один градус при изобарическом процессе.
Используя это соотношение, Роберт Майер в 1842 г. вычислил механический эквивалент теплоты: 1 кал = 4,19 Дж.
Слайд 32
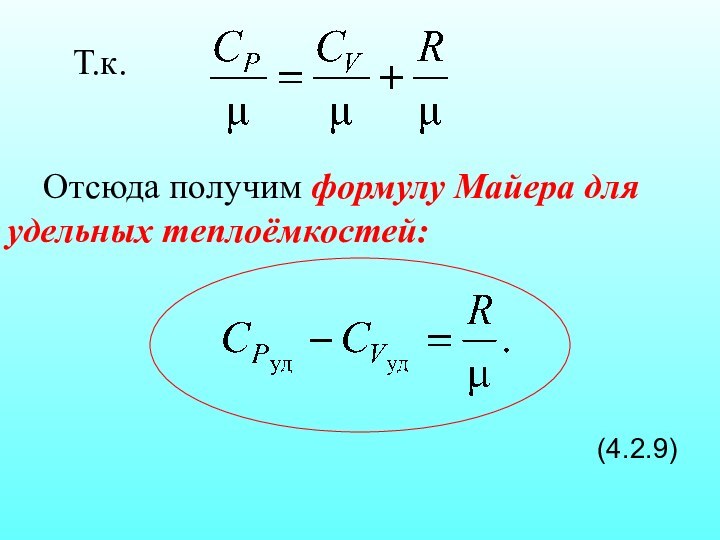
Отсюда получим формулу Майера для удельных теплоёмкостей:
Слайд 33
4.3. Теплоёмкости одноатомных и многоатомных газов
Внутренняя энергия одного
моля идеального газа равна
(4.3.1)
Слайд 34
Теплоёмкости одноатомных газов
теплоемкость при постоянном объеме СV –
величина постоянная, от температуры не зависит.
Слайд 35
Учитывая физический смысл R для
изобарических процессов можно записать:
(4.3.3)
(для одного моля). Отсюда
Тогда,
теплоемкость при постоянном давлении для одноатомных газов:
Слайд 36
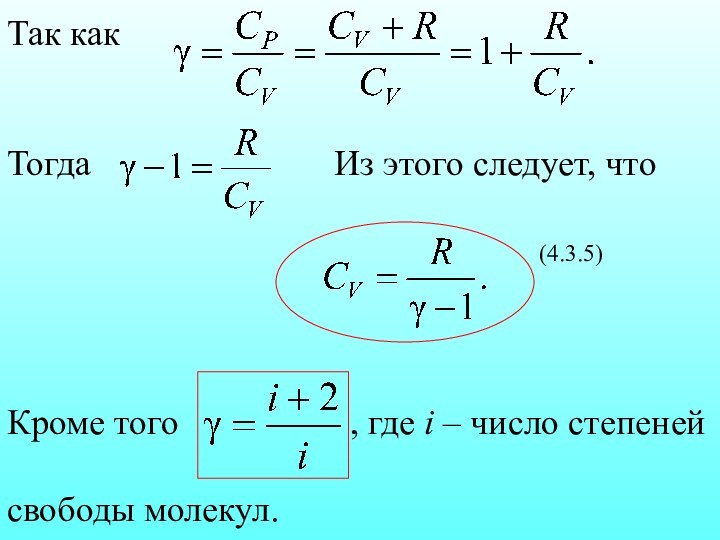
- постоянная адиабаты (коэффициент Пуассона)
Из
этого следует, что
(4.3.5)
Кроме того , где i – число степеней
свободы молекул.
Слайд 38
Подставив в выражение для внутренней энергии, получим:
а так
как
, то
внутреннюю энергию можно найти по формуле:
(4.3.6)
,
хорошо подтверждается на опыте с Ne, He, Ar, Kr, парами одноатомных металлов.
Слайд 40
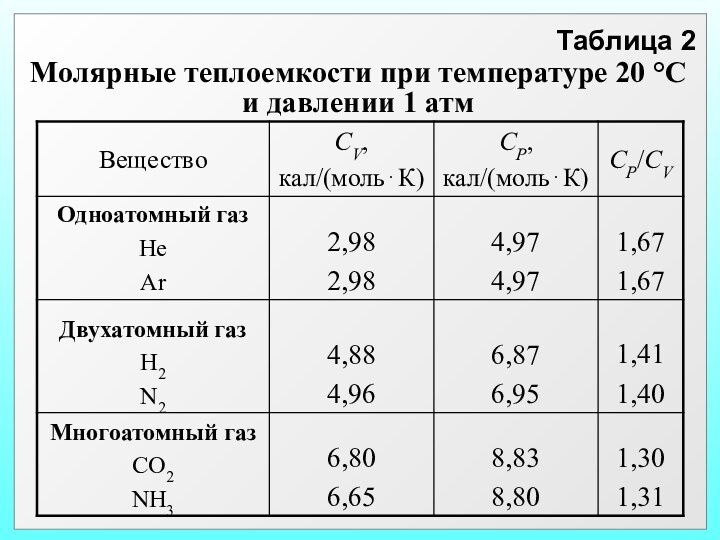
Теплоемкости многоатомных газов
Опыты с двухатомными газами
такими как азот, кислород и др. показали, что
Для водяного пара и других многоатомных газов (СН3, СН4, и так далее)
То есть молекулы многоатомных газов нельзя рассматривать как материальные точки.
Слайд 41
Необходимо учитывать вращательное движение молекул и
число степеней свободы этих молекул.
Молекулы многоатомных газов
нельзя рассматривать как материальные точки.
Слайд 42
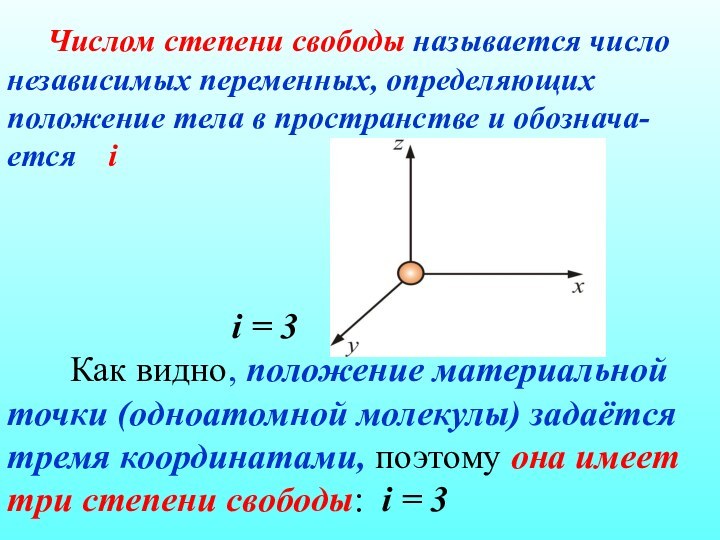
Числом степени свободы называется число
независимых переменных, определяющих положение тела в пространстве и обознача-ется
i
i = 3
Как видно, положение материальной точки (одноатомной молекулы) задаётся тремя координатами, поэтому она имеет три степени свободы: i = 3
Слайд 43
Многоатомная молекула может ещё и вращаться.
Например, у двухатомных молекул вращательное движение можно разложить на
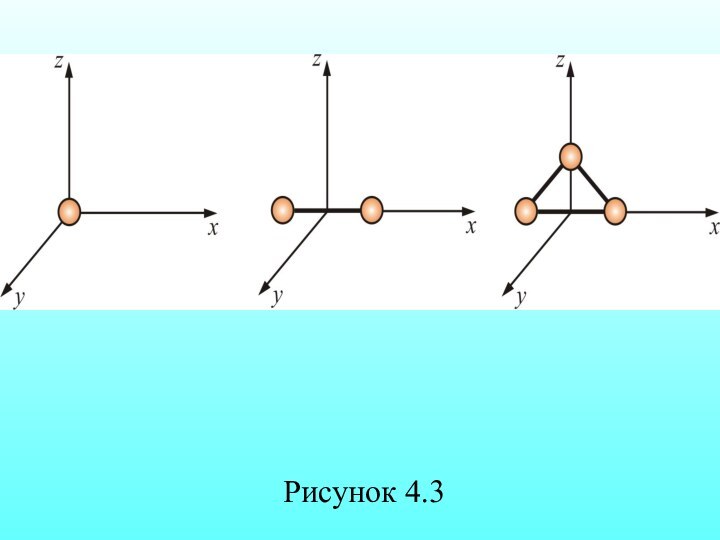
два независимых вращения, а любое вращение можно разложить на три вращательных движения вокруг взаимно перпендикулярных осей. Но для двухатомных молекул вращение вокруг оси z не изменит её положение в пространстве, а момент инерции относительно этой оси равен нулю (рисунок 4.3).
Слайд 47
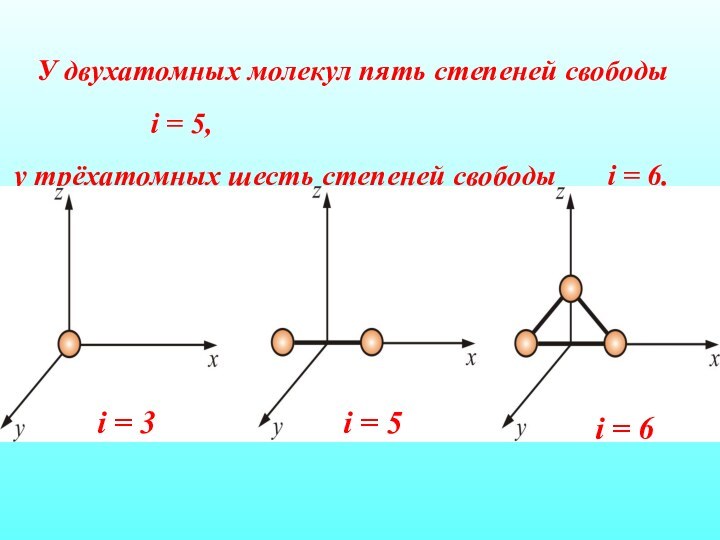
У двухатомных молекул пять степеней свободы
i
= 5,
у трёхатомных шесть степеней свободы
i = 6.
i = 6
i = 5
i = 3
Слайд 48
При взаимных столкновениях молекул возможен обмен их энергиями
и превращение энергии вращательного движения в энергию поступательного движения
и обратно. Таким путём установили равновесие между значениями средних энергий поступательного и вращательного движения молекул.
Слайд 49
Больцман доказал, что, средняя энергия
приходящаяся на одну степень
свободы
равна
4.4. Закон о равномерном распределении энергии по
степеням свободы
Слайд 50
Итак, средняя энергия приходящаяся на
одну степень свободы:
(4.4.1)
Слайд 51
У одноатомной молекулы i = 3, тогда
(4.4.2)
для двухатомных молекул i = 5
(4.4.3)
для трёхатомных молекул i = 6
(4.4.4)
Слайд 52
На среднюю кинетическую энергию молекулы, имеющей i-степеней свободы
приходится
(4.4.5)
Это и есть закон Больцмана о равномерном распределении средней кинетической энергии по степеням свободы.
Здесь i = iп + iвр + iкол (4.4.6)
Слайд 54
для трехатомных молекул:
.
При этом: для двухатомных молекул:
Слайд 55
В общем случае, для молярной массы газа
(4.4.6)
(4.4.7)
Слайд 56
Для произвольного количества газов:
, (4.4.9)
(4.4.10)
Из теории также следует, что СV не зависит от температуры (рисунок 4.4).
Слайд 58
Для одноатомных газов это выполняется
в очень широких пределах, а для двухатомных газов только
в интервале от 100 1000 К. Отличие связано с проявлением квантовых законов. При низких температурах вращательное движение как бы «вымерзает» и двухатомные молекулы движутся поступательно, как одноатомные;
равны их теплоёмкости.
При увеличении температуры, когда Т > 1000 К, начинают сказываться колебания атомов молекулы вдоль оси z (атомы в молекуле связаны не жёстко, а как бы на пружине).
Слайд 59
Одна колебательная степень свободы несет
энергии, так как при этом есть и кинетическая
и потенциальная энергия, то есть появляется шестая степень свободы – колебательная. При температуре равной 2500 К, молекулы диссоциируют. На диссоциацию молекул тратится энергия раз в десять превышающая среднюю энергию поступательного движения. Это объясняет сравнительно низкую температуру пламени. Кроме того, атом – сложная система, и при высоких температурах начинает сказываться движение электронов внутри него.
Слайд 60
4.5. Применение первого начала термодинамики к
изопроцессам идеальных газов
В таблице (4.1) приводятся сводные данные о характеристиках
изопроцессов в газах. Здесь используются известные нам формулы:
– I начало термодинамики или закон сохранения энергии в термодинамике;
Слайд 61
Таблица 4.1
δQ = 0
Закон
Шарля
Закон
Гей-Люссака
Закон
Бойля –
Мариотта
Слайд 65
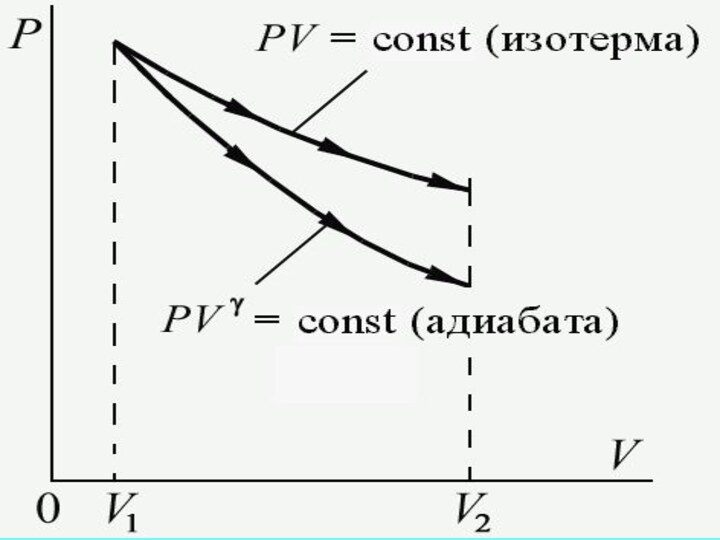
Здесь уместно рассмотреть еще и политропный процесс –
такой процесс, при котором изменяются все основные параметры системы,
кроме теплоемкости, т.е. С = const.
Уравнение политропы
(4.5.1)
или
. (4.5.2)
Здесь n – показатель политропы.
Слайд 66
С помощью показателя n можно легко
описать любой изопроцесс:
1. Изобарный процесс Р = const, n
= 0
(4.5.3)
2. Изотермический процесс Т = const, n = 1,
3. Изохорный процесс V = const,
(4.5.4)
Слайд 67
4. Адиабатический процесс Q = 0, n =
γ,
Сад = 0.
Во всех этих процессах работу можно
вычислить по одной формуле:
(4.5.5)