Слайд 2
Оптический количественный анализ
Основан на регистрации изменений, происходящих
с лучом света при прохождении его через исследуемый раствор.
Методы
количественного анализа:
Фотометрия
Рефрактометрия
Поляриметрия
Слайд 3
Фотометрические методы анализа
Абсорбционная фотометрия:
спектрофотометрия
нефелометрия (собственно нефелометрия и
турбидиметрия)
атомно-адсорбционная фотометрия
2. Эмиссионная фотометрия:
флуориметрия
пламенная фотометрия
атомно-эмиссионный спектральный анализ
Слайд 4
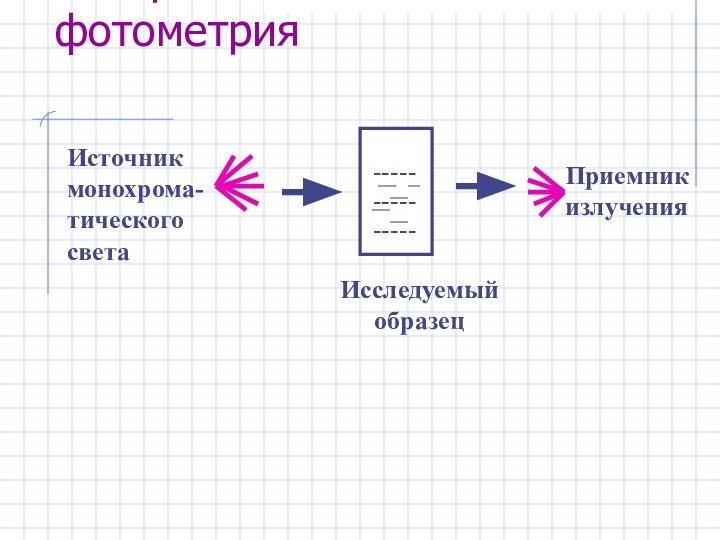
Адсорбционная фотометрия
Источник монохрома-тического света
---------------
Приемник излучения
Исследуемый образец
Слайд 5
Закон Бугера-Ламберта-Беера
где It – интенсивность света, прошедшего
через раствор, Io – интенсивность падающего на раствор света,
L – толщина слоя раствора в см, с – концентрация поглощающего свет раствора вещества; ε – коэффициент погашения (абсорбции, экстинции). Если концентрация раствора составляет моль/л и L = 1см, то ε = А
Слайд 6
Оптическая плотность раствора
Оптическая плотность раствора = экстинция
= адсорбция раствора (Е, D, А) – логарифм
отношения интенсивности падающего на раствор света (Io) к интенсивности света, прошедшего через раствор (It).
Оптическая плотность растворов при прочих равных условиях прямо пропорциональна концентрации вещества!
Слайд 7
Светопроницаемость раствора
Светопроницаемость (прозрачность) раствора (Т) – отношение интенсивности
монохроматического потока излучения, прошедшего через исследуемый объект, к интенсивности
первоначального светового потока. Выражается в %.
Т(%) = It/Io х 100
Слайд 8
Спектрофотометрия
Измерение интенсивности окраски раствора анализируемого вещества относительно интенсивности
окраски эталонового раствора.
Приборы для выполнения - фотометры и спектро
-фотометры.
В фотометрах нужные спектральные диапазоны выделяются при помощи светофильтров. Число рабочих участков спектра = числу светофильтров.
В спектрофотометрах участки света выделяются с помощью призм или дифракционных решеток, поэтому можно установить любую длину волны в заданном диапазоне и выделить более узкий (монохроматический) участок спектра.
Спектрофотометры –приборы более высокого класса.
Слайд 9
Нефелометрия
Нефелометрия – метод анализа, связанный с оценкой
степени мутности исследуемого раствора. Мутность возникает в результате взвешивания
в растворителе мельчайших твердых частиц вещества, которые рассеивают лучи света, проходящие через раствор. Интенсивность рассеивания света возрастает с увеличением размера и числа рассеивающих частиц.
Эта закономерность соблюдается в сильно разбавленных растворах, что позволяет определять концентрацию вещества по степени мутности образуемых им растворов.
Слайд 10
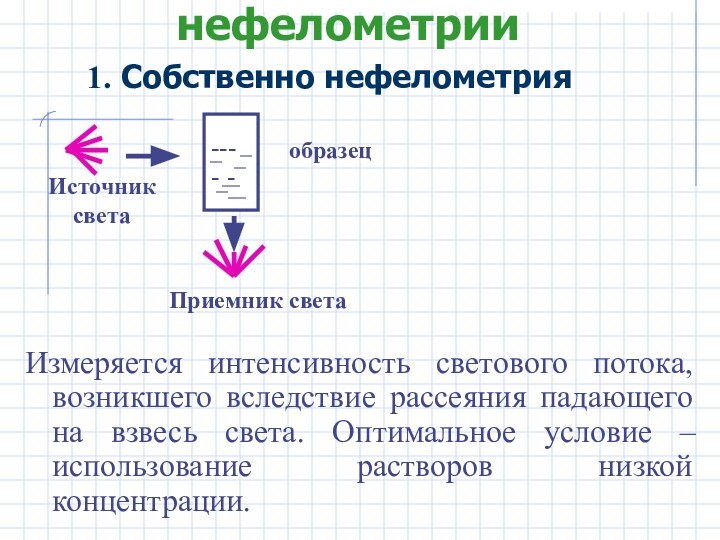
Основные методы нефелометрии
Измеряется интенсивность светового потока, возникшего
вследствие рассеяния падающего на взвесь света. Оптимальное условие –
использование растворов низкой концентрации.
1. Собственно нефелометрия
Источник света
--- - -
образец
Приемник света
Слайд 11
Основные методы нефелометрии (продолжение)
2. Турбидиметрия
-- -- -
-
образец
Приемник света
Источник света
Измеряется ослабление светового потока, прошедшего через
мутный раствор. Все нефелометрические методы в клинике относятся к турбидиметрии – тимоловая проба, определение серомукоидов, беталипопротеидов, тесты агрегации тромбоцитов и др
Слайд 12
Наиболее частые длины волн, используемые для фотометрии
Видимая
область спектра – 400-700 нм.
(самый частый используемый диапазон.)
Более
700 нм – инфакрасная (используется очень редко)
Менее 400 – УФ длинноволновая (300-400)
УФ коротковолновая (220-300)
Слайд 13
Эмиссионная фотометрия
Это метод анализа, основанный на
измерении энергии, излучаемой веществом в результате энергетически возбужденного состояния.
Основные методы эмиссионной фотометрии:
а) Флуориметрия
б) Пламенная фотометрия
Слайд 14
Флуориметрия
Флуориметрия – основана на измерении флуоресценции, которая возникает
в результате энергетического возбуждения исследуемого вещества под влиянием жесткого
коротковолнового облучения (обычно ультрафиолетовые лучи).
Выполняется на аппаратах – флуориметрах.
По чувствительности намного выше колориметрических методов (в 100-1000 раз).
Недостаток – связан именно с высокой чувствительностью, т.к. требуются громоздкие способы предварительной очистки вещества от примесей, которые вносят фоновые искажения.
В клинических лабораториях используется нешироко. Определяют катехоламины.
Слайд 15
Пламенная фотометрия
В качестве энергетического агента, вызывающего
состояние возбуждения исследуемого вещества используется пламя газовой горелки. Ионы
металлов окрашивают пламя в различный цвет, в соответствии с характерными для них спектрами испускания. Для выделения излучения отдельных ионов применяют специальные светофильтры.
В КДЛ применяют в основном для определения концентрации ионов калия и натрия, т.к. эти элементы возбуждаются легче остальных - достаточна энергия низкотемпературного пламени сгорания метана в воздухе. Недостаток метода – необходимость газового оборудования. Эти методы заменяют на ионоселективные, потенциометрические.
Слайд 16
Атомно-эмиссионный
спектральный анализ
Электрич. разряд
-- --
Испарение,
возбуждение
атомов
Полихро-матор
Разложение на спектры
Обработка спектров
Слайд 17
Основные условия измерения при работе с фотометрической аппаратурой
1.
Толщина рабочего слоя фотометрической кюветы. Чем толще рабочий слой
кюветы, тем выше будет оптическая плотность измеряемых в ней растворов вещества. Обязательно учитывается и вносится поправка. В ФЭК (измерение в видимой части спектра) применяют оптические кюветы из обычного стекла, с толщиной 5, 10, редко 3 мм. Для измерений в ультрафиолетовой области спектра (СФ, флуориметр) используется материал, не поглощающий УФ лучи - увиолевое, реже кварцевое стекло, толщиной 10 мм.
Слайд 18
Основные условия измерения при работе с фотометрической аппаратурой
(продолжение)
2. Длина световой волны. Определяется физико-химическими свойствами исследуемых растворов.
Визуально они могут быть: а) прозрачные неокрашенные; б)мутные неокрашенные; в)прозрачные окрашенные, г) мутные окрашенные (исследованию не подлежат).
используются в иммунологии при определении ЦИК, в биохимии для определения НАД. Замер в УФ области при соответственно 280 и 340 нм.
относится к нефелометрии, длина волны 540 нм (зеленый светофильтр) или 640 нм (красный светофильтр).
длина световой волны обусловлена принципом дополнительности цветов исследуемого раствора и светофильтра. Например, для растворов, окрашенных в желтый цвет используется синий светофильтр (440нм), для растворов синего цвета желтый (590) иногда красный - 640 нм.
Слайд 19
Способы расчета результатов фотометрии
условные единицы
по стандартным (эталонным)
растворам
по калибровочному графику
с помощью коэффициента пересчета
Слайд 20
Способ расчета результатов фотометрии по условным единицам
Это
фактически непосредственное выражение единиц оптической плотности исследуемого раствора. Для
удобства единицы оптической плотности умножают на коэффициент 100 или 1000 для выражения у.е. в больших целых числах. Например, сиаловые кислоты 130-200 у.е. соответствуют коэффициенту экстинции 0,13-0,20, умноженному на 1000 .
Слайд 21
Способ расчета результатов фотометрии
по стандартным растворам
Эталонные
растворы обрабатываются параллельно с серией исследуемого биоматериала и находятся
в тех же условиях, что исследуемый материал.
Недостаток - повышенный расход реактивов и рабочего времени.
Подготовка эталонного раствора: из реактива хч, взвешивание на аналитических весах с высокой точностью (для флуориметрии, а для ФЭК можно на торсионных), растворение в мерной колбе, концентрация вещества в стандарте должна быть близка к норме. Расчет исследований по стандартным растворам производится по способу простой арифметической пропорции: стандарт умножить на пробу разделить на стандарт.
Слайд 22
Способ расчета результатов фотометрии
по калибровочному графику
Недостаток -
ограниченное количество методик со стабильными условиями проведения и с
хорошим подчинением результатов основному закону фотометрии. Калибровочные графики строятся для каждого фотометра отдельно, перенос на другой аппарат недопустим даже в случае использования однотипных фотометров, т.к. у каждого аппарата свои технические особенности. Калибровочные графики проверяются не реже 1 раза в год.
Слайд 23
Правила построения калибровочного графика
Проводят исследование серии стандартных
растворов, различающихся между собой концентрацией. Диапазон концентраций должен охватывать
как значения физиологической нормы, так и наиболее вероятные пределы патологии для данного исследуемого компонента. Для приготовления стандартных растворов навеска берется только на аналитических весах, обязательно в параллелях (для снижения вероятности ошибок, связанных с погрешностями взвешивания), растворение в мерной колбе.
Калибровочный график должен содержать:
название метода исследования,
заводской номер фотометра, к которому построен график,
указать длину световой волны, толщину слоя кюветы,
исходные данные для построения,
дата построения
Слайд 24
Способ расчета результатов фотометрии
по коэффициентам пересчета
Является
наиболее простым и быстрым. Формула: С=F x E, где
С - концентрация исследуемого компонента,
F - коэффициент пересчета, Е - экстинция.
Коэффициент пересчета является величиной специфической для каждого отдельного теста. Обычно указывается в описании метода исследования. Можно рассчитывать самому на основании исследования стандартных растворов. За основу можно взять ранее построенный калибровочный график. Коэффициенты требуют проверки не реже 1 раза в год.
Коэффициенты используются в анализаторах. Они вводятся в память компьютера и выдаются автоматически.
Слайд 25
Методы оценки результатов фотометрии
по конечной точке (измерение
в конечной точке) - учет образования продукта за некоторое
время инкубации. Расчет результатов по стандарту.
по фиксированному времени - требуется применение фотометров с термостатируемыми кюветами. Устанавливается количество нарабатываемого (расходуемого) продукта за определенный промежуток времени, расчет концентрации по стандарту.
кинетически (кинетическое измерение) - производят измерение оптической плотности через определенные интервалы времени. Используется для ферментативных методов
Слайд 26
Особенности эксплуатации фотометрической аппаратуры
Показания фотометров можно снимать
в единицах оптической плотности или в процентах поглощенного или
прошедшего света относительно фоновых величин (шкалы разных цветов). Во всех, предназначенных для измерений оптической плотности приборах, наибольшая точность достигается при значениях экстинции около 0,3, т.е. когда проходит примерно половина падающего света. По мере удаления в ту или другую сторону точность измерения уменьшается!
Экстинция раствора есть произведение его концентрации на толщину слоя раствора. Оптимальны в смысле чувствительности, точности и удобства кюветы с длине оптического пути 1 см.
Точность фотометрии значительно возрастает при использовании проточных кювет.
Слайд 27
Основные источники ошибок
при фотометрии
1).Работа с растворами,
имеющими слишком высокую
(более 1) или слишком низкую (менее
0,3) оптическую плотность резко увеличивает погрешность измерения.
2). Для фотометрии пригодны лишь прозрачные растворы. Мутные растворы рассеивают свет и снижают достоверность измерений. Мутные окрашенные растворы использоваться не должны.
Слайд 28
Рефрактометрия
Метод основан на измерении показателя преломления света
при прохождении его через оптически неоднородные среды.
Пример – определение
общего белка в сыворотке. В лаборатории используется мало.
Слайд 29
Обыкновенное и плоскополяризованное электромагнитное поле излучения
О
С
А
В
О
С1
В1
А1
В
В1
О
Слайд 30
Поляриметрия
Основан на способности веществ в растворе изменять плоскость
поляризованного луча света.
Пример – лазерный поляриметр для определения глюкозы
в моче. В КЛД применяется мало.