- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Основы термодинамики необратимых процессов
Содержание
- 2. Основные понятия термодинамикиТермодинамическая система – совокупность тел,
- 3. Основные понятия термодинамикиИзолированные системы – системы, которые
- 4. Основные понятия термодинамикиЭкстенсивные параметры – характеризуют систему
- 5. Основные понятия термодинамикиРавновесный процесс – процесс, рассматриваемый
- 6. Равновесное состояние системы – состояние, в которое
- 7. термодинамика неравновесных процессов Описание эволюции системы во времени и свойств таких систем
- 8. Литература:Н. М. Бажин, В. А. Иванченко, В.
- 9. Современная термодинамика / Пригожин И., Кондепуди Д. – М.: Мир, 2002. – 462 с.Литература:
- 10. Пригожин И. Введение в термодинамику необратимых процессов.
- 11. Агеев Е.П. Неравновесная термодинамика в вопросах и ответах. М.: Эдиториал УРСС, 2001. – 136 с.Литература:
- 12. Научная периодика Journal of Non-Equilibrium Thermodynamicshttp://www.degruyter.com/view/j/jnet4 Issues per yearIMPACT FACTOR 2010: 1.152
- 13. Научная периодикаThe Journal of Chemical ThermodynamicsImpact Factor: 2.794 http://www.journals.elsevier.com
- 14. Системы в термодинамике неравновесных процессовТипы неравновесных системПостулаты
- 15. Системы в термодинамике неравновесных процессовТермодинамическая система –
- 16. Для неравновесных систем (открытых и закрытых) характерны
- 17. Однородное состояниеСтационарное состояниеНеоднородное и нестационарное состояниеРавновесное состояниеfi - cвойство системы
- 18. Системы в термодинамике неравновесных процессоводнородные, непрерывные и прерывные Zi(r, t) – интенсивное свойство
- 19. Постулаты термодинамики необратимых процессов dS 0diS
- 20. Постулаты термодинамики необратимых процессов энтропия вне равновесия
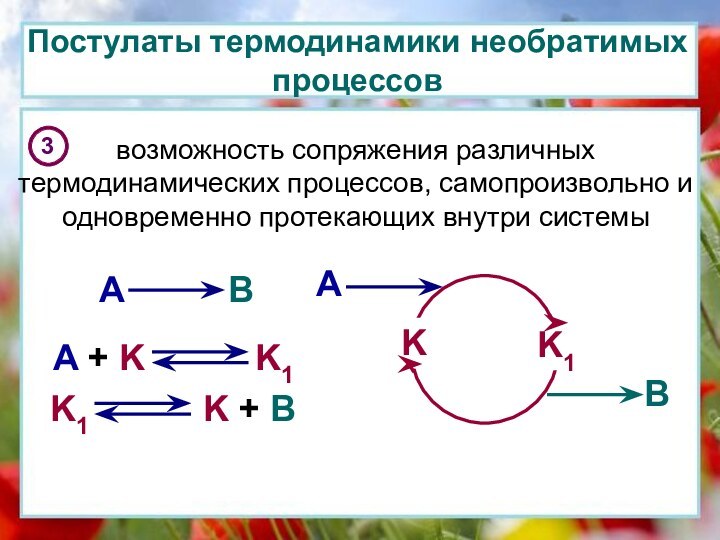
- 21. Постулаты термодинамики необратимых процессов возможность сопряжения различных термодинамических процессов, самопроизвольно и одновременно протекающих внутри системы
- 22. принципиальная важность понятия устойчивости неравновесной системы Постулаты термодинамики необратимых процессов
- 23. Локальные величины в неравновесной термодинамике Локальные макроскопические
- 24. Локальные величины в неравновесной термодинамике Локальное термодинамическое
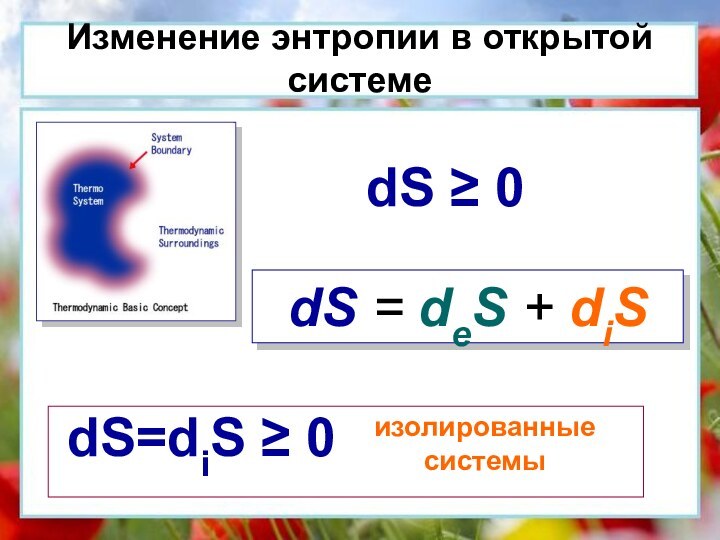
- 25. Изменение энтропии в открытой системе dS = deS + diSdS 0dS=diS 0изолированные системы
- 26. Изменение энтропии в открытой системе dS =
- 27. Изменение энтропии в открытой системе dS/dt =
- 28. Изменение энтропии в открытой системе dS/dt =
- 29. diS для однородной гомогенной системы при наличии
- 30. diS для однородной гомогенной системы при наличии
- 31. Скачать презентацию
- 32. Похожие презентации























Слайд 3
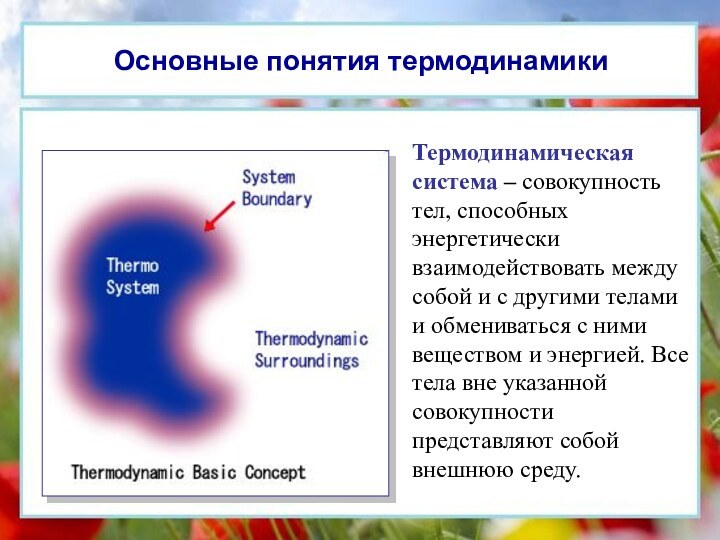
Основные понятия термодинамики
Изолированные системы – системы, которые не
обмениваются с окружающей средой ни энергией, ни массой.
Закрытые
системы - системы, которые обмениваются с окружающей средой энергией, но не обмениваются массой. Открытые системы – системы, которые обмениваются с внешней средой и энергией, и массой.
Адиабатные (адиабатические) системы - системы, которые не обмениваются с окружающей средой энергией.
Термодинамические системы
Слайд 4
Основные понятия термодинамики
Экстенсивные параметры – характеризуют систему как
целое. Это масса и пропорциональные ей величины, например –
объем. Эти величины имеют аддитивный характер – общая масса системы равна сумме масс ее отдельных частей и т.п.Интенсивные параметры – не зависят от массы и могут принимать вполне определенные значения в каждой точке системы.
Термодинамические параметры
величины, характеризующие состояние термодинамической системы.
Слайд 5
Основные понятия термодинамики
Равновесный процесс – процесс, рассматриваемый как
непрерывный ряд равновесных состояний системы.
Обратимый термодинамический процесс –
процесс, после которого система и взаимодействующие с ней системы могут возвратиться в начальное состояние. Термодинамический процесс
изменение состояния системы, которое характеризуется изменением ее термодинамических параметров
Равновесный процесс всегда обратим, а обратимый процесс всегда протекает равновесным путем.
Слайд 6 Равновесное состояние системы – состояние, в которое со
временем приходит система при постоянных внешних условиях, и которое
характеризуется неизменностью во времени термодинамических параметров и отсутствием в системе потоков вещества и теплоты. Постоянство параметров не должно быть связано с протеканием какого-либо процесса, внешнего по отношению к системе.Основные понятия термодинамики
Слайд 7
термодинамика неравновесных процессов
Описание эволюции системы во времени
и свойств таких систем
Слайд 8
Литература:
Н. М. Бажин, В. А. Иванченко, В. Н.
Пармон. Термодинамика для химиков. М.: Химия, КолосС, 2004 –
416 с.Слайд 10 Пригожин И. Введение в термодинамику необратимых процессов. –
Ижевск: НИЦ «Регулярная и хаотическая динамика», 2001. – 160с.
Литература:
Слайд 11 Агеев Е.П. Неравновесная термодинамика в вопросах и ответах.
М.: Эдиториал УРСС, 2001. – 136 с.
Литература:
Слайд 12
Научная периодика
Journal of Non-Equilibrium Thermodynamics
http://www.degruyter.com/view/j/jnet
4 Issues per
year
IMPACT FACTOR 2010: 1.152
Слайд 13
Научная периодика
The Journal of Chemical Thermodynamics
Impact Factor: 2.794
http://www.journals.elsevier.com
Слайд 14
Системы в термодинамике неравновесных процессов
Типы неравновесных систем
Постулаты термодинамики
необратимых процессов
Локальные величины в неравновесной термодинамике
Изменение энтропии в открытой
системеПроизводство энтропии для однородной гомогенной системы при наличии химических превращений
Слайд 15
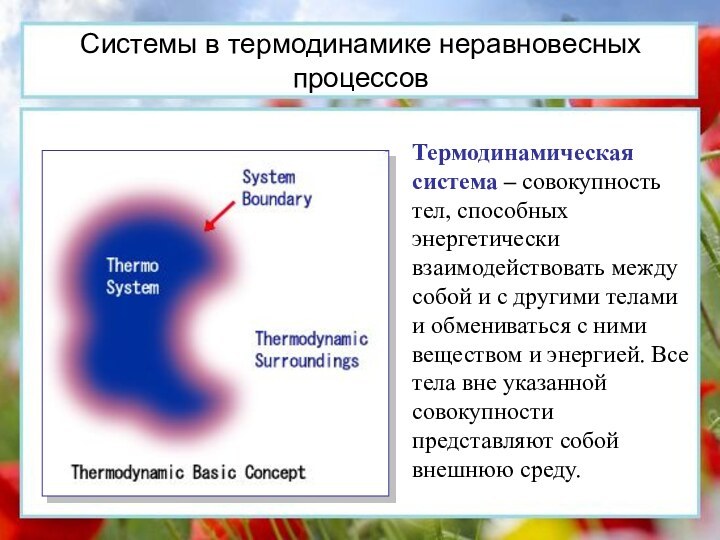
Системы в термодинамике неравновесных процессов
Термодинамическая система – совокупность
тел, способных энергетически взаимодействовать между собой и с другими
телами и обмениваться с ними веществом и энергией. Все тела вне указанной совокупности представляют собой внешнюю среду.Слайд 16 Для неравновесных систем (открытых и закрытых) характерны неравновесные
состояния, параметры и свойства которых являются функциями времени и/или
пространства. В общем случае неравновесную систему нельзя охарактеризовать едиными значениями Т и р.Системы в термодинамике неравновесных процессов
Слайд 17
Однородное состояние
Стационарное состояние
Неоднородное и нестационарное состояние
Равновесное состояние
fi -
cвойство системы
Слайд 18
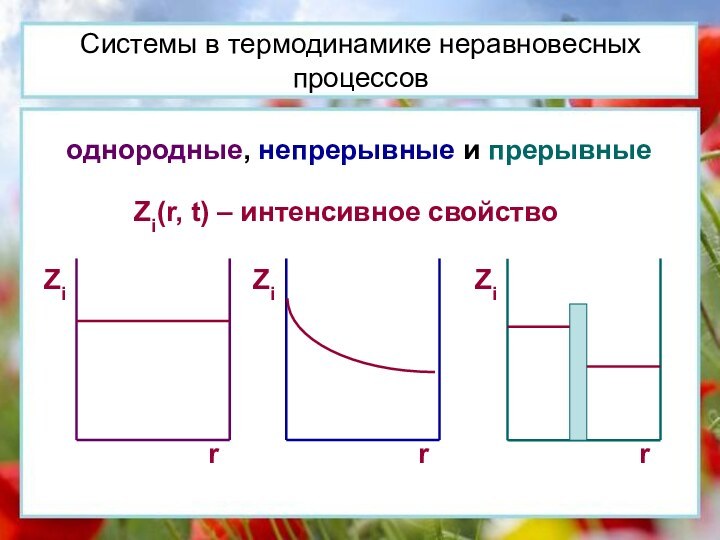
Системы в термодинамике неравновесных процессов
однородные, непрерывные и прерывные
Zi(r, t) – интенсивное свойство
Слайд 19
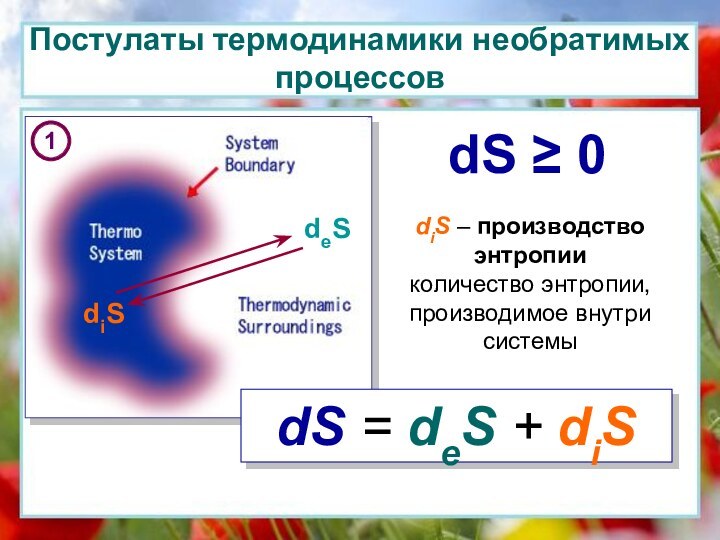
Постулаты термодинамики необратимых процессов
dS 0
diS –
производство энтропии
количество энтропии, производимое внутри системы
dS =
deS + diS
Слайд 20
Постулаты термодинамики необратимых процессов
энтропия вне равновесия зависит
от тех же величин и переменных, что и в
состоянии равновесия (допущение существования локального равновесия)diS 0
Слайд 21
Постулаты термодинамики необратимых процессов
возможность сопряжения различных термодинамических
процессов, самопроизвольно и одновременно протекающих внутри системы
Слайд 22
принципиальная важность понятия устойчивости неравновесной системы
Постулаты термодинамики
необратимых процессов
Слайд 23
Локальные величины в неравновесной термодинамике
Локальные макроскопические величины
– величины, отнесенные к физически бесконечно малым частям системы
Физически
бесконечно малая величина – конечная, но относительно малая часть целого. Применимо только для экстенсивных величин. Физически бесконечно малый объем должен быть велик по сравнению с расстоянием между молекулами и очень мал по сравнению с макроскопическими неоднородностями среды.
Слайд 24
Локальные величины в неравновесной термодинамике
Локальное термодинамическое равновесие
- термодинамическое равновесие, которое реализуется только в физически бесконечно
малых частях системы. При этом макроскопические величины, характеризующие систему в целом, становятся функциями координат и времени.Время установления локального равновесия составляет порядка 1,6*10-10 с для газов и 1*10-13 с для жидкостей
Слайд 26
Изменение энтропии в открытой системе
dS = deS
+ diS
dS/dt = deS/dt + diS/dt
Скорость общего изменения энтропии
dS/dt системы равна сумме скорости возникновения (производства) энтропии внутри самой системы diS/dt и скорости обмена энтропией между системой и окружающей средой deS/dt
Слайд 27
Изменение энтропии в открытой системе
dS/dt = deS/dt
+ diS/dt
1. dS/dt > 0
deS/dt > 0 или
deS/dt < 0, но |deS/dt| < diS/dt2. dS/dt < 0
deS/dt < 0 и |deS/dt| > diS/dt
3. dS/dt = 0
deS/dt < 0 и |deS/dt| = diS/dt
Слайд 28
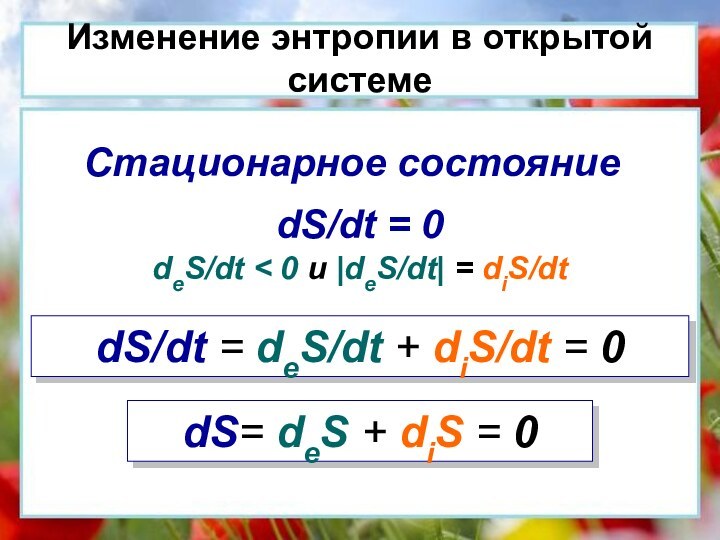
Изменение энтропии в открытой системе
dS/dt = deS/dt
+ diS/dt = 0
dS/dt = 0
deS/dt < 0 и
|deS/dt| = diS/dtСтационарное состояние
dS= deS + diS = 0
Слайд 29 diS для однородной гомогенной системы при наличии химических
превращений
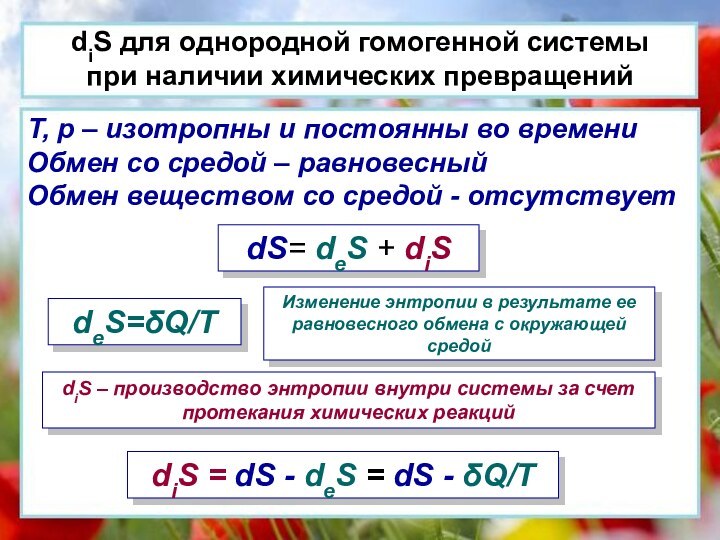
T, p – изотропны и постоянны во времени
Обмен со
средой – равновесныйОбмен веществом со средой - отсутствует
dS= deS + diS
deS=Q/T
Изменение энтропии в результате ее равновесного обмена с окружающей средой
diS – производство энтропии внутри системы за счет протекания химических реакций
diS = dS - deS = dS - Q/T
Слайд 30 diS для однородной гомогенной системы при наличии химических
превращений
Система совершает только механическую работу расширения
Q = dU +
PdVdiS = dS – (dU + PdV)/T
diS = (1/T)(TdS – dU - PdV)
dG = -TdS + dU + PdV
diS = -dG/T > 0





























