- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Тепловое движение
Содержание
- 2. Первоначальные сведения о строении веществаВсе вещества (тела)
- 3. Атомы и молекулы
- 4. Изотопы водорода
- 5. СПЕКТРЫ
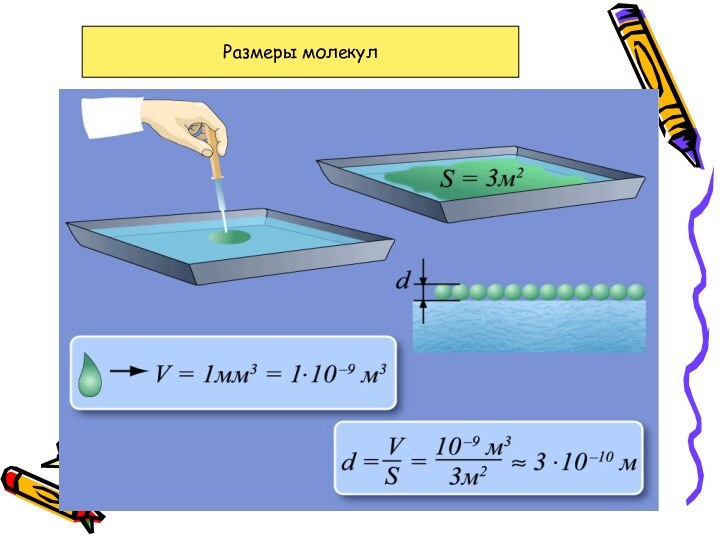
- 6. Размеры молекул
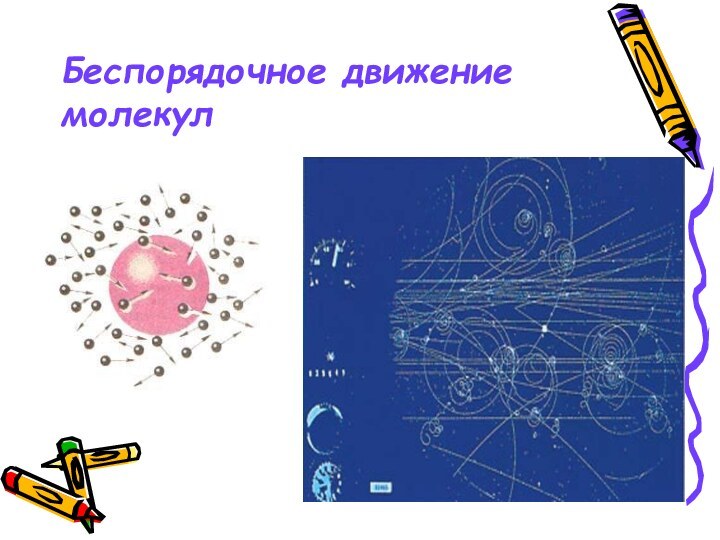
- 7. Беспорядочное движение молекул
- 8. Диффузия – это явление самопроизвольного проникновения частиц одного вещества в межмолекулярное пространство другого веществаначало процессаустановившееся положение
- 9. Температура.
- 10. Термометры
- 11. Опыт Штерна
- 12. Броуновское движение - это тепловое движение мельчайших
- 15. Агрегатные состояния вещества
- 16. Тепловое движение атомов в твердых телах
- 18. Плавление и отвердевание льда
- 19. Тепловое движение молекул в жидкости Молекулы жидкости
- 20. Кипение интенсивное (бурное) парообразование, происходящее
- 21. Конденсация – это превращение вещества из
- 22. Тепловое движение молекул в газеМолекулы в газе
- 25. Тепловой двигатель
- 26. Скачать презентацию
- 27. Похожие презентации
Первоначальные сведения о строении веществаВсе вещества (тела) состоят из мельчайших частицЧастицы беспорядочно движутсяЧастицы взаимодействуют друг с другом





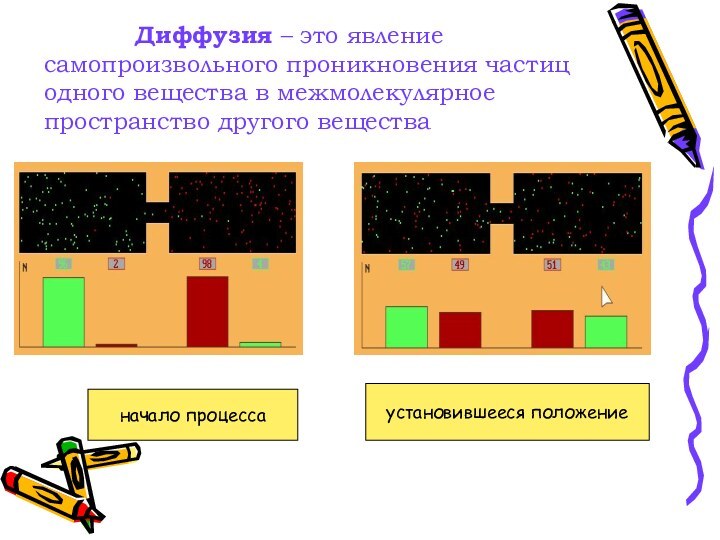
















Слайд 8 Диффузия – это явление самопроизвольного проникновения частиц одного
вещества в межмолекулярное пространство другого вещества
начало процесса
установившееся положение
Слайд 12 Броуновское движение - это тепловое движение мельчайших частиц,
взвешенных в жидкости или газе
открыто английским ботаником Броуном (1827
г.)явилось наглядным доказательством хаотичного молекулярного движения.
Броуновская частица
среди молекул.
Траектория
движения
трех броуновских
частиц
Слайд 16
Тепловое движение атомов в твердых телах
Атомы
и молекулы твердых тел колеблются около определенных положений равновесия.
Твердые тела сохраняют и объем, и форму.
Если мысленно соединить центры положений равновесия атомов или ионов твердого тела, то получится кристаллическая решетка.
Слайд 19
Тепловое движение молекул в жидкости
Молекулы жидкости расположены
почти вплотную друг к другу.
Молекулы жидкости совершают колебания
около положения равновесия. Время от времени молекула совершает переходы из одного оседлого состояния в другое, как правило, в направлении действия внешней силы.
Жидкости текучи, не сохраняют своей формы и принимают форму сосуда, в который налиты.
Слайд 20
Кипение
интенсивное (бурное) парообразование, происходящее по
всему объему жидкости за счет возникновения и всплытия на
поверхность многочисленных пузырей пара.Слайд 21 Конденсация – это превращение вещества из газообразного состояния
в жидкое
пар, вырывающийся из чайника невидимой струей, вскоре
конденсируется – превращается в туман (скопление мельчайших капелек воды).
Слайд 22
Тепловое движение молекул в газе
Молекулы в газе движутся
хаотично (беспорядочно).
В газах расстояние между атомами или молекулами
в среднем во много раз больше размеров самих молекул. Молекулы в газе движутся с большими скоростями (сотни м/с).
Газы легко сжимаются, среднее расстояние между молекулами при этом уменьшается, но все равно остается большим их размеров.
Газы не сохраняют ни формы, ни объема, их объем и форма совпадают с объемом и формой сосуда, который они заполняют.
Многочисленные удары молекул о стенки сосуда создают давление газа.