двух или нескольких простых веществ.
Компонентами называют
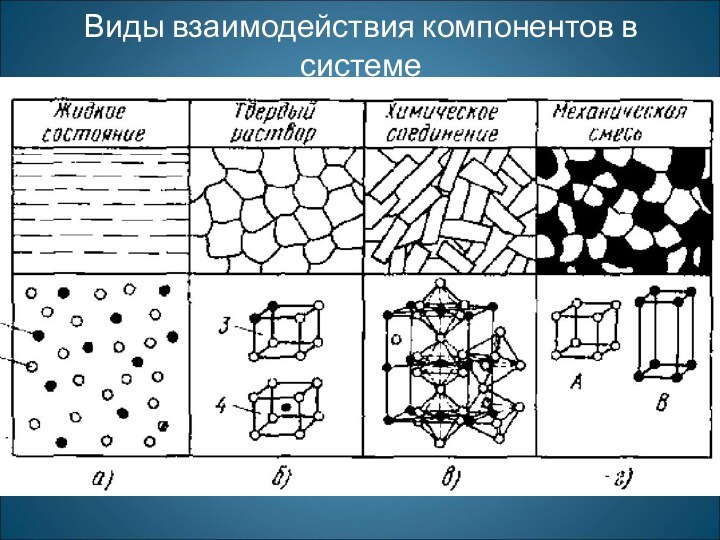
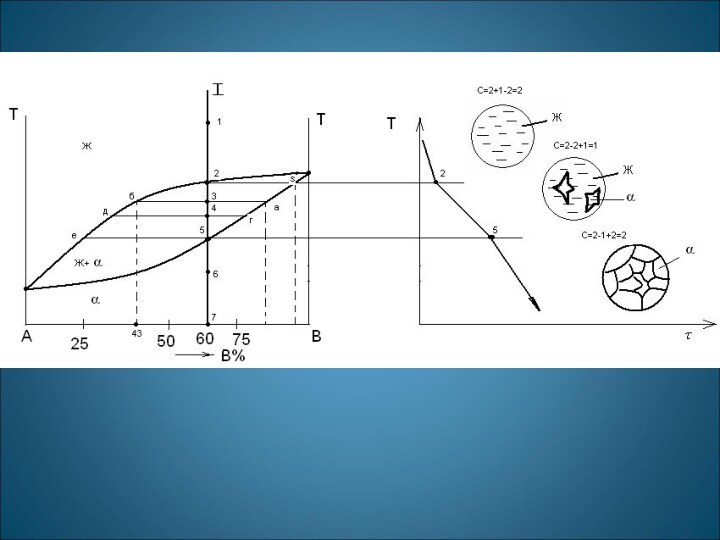
вещества, образующие систему. В зависимости от физико-химического взаимодействия компонентов в сплавах образуются фазы, число и тип которых характеризует состояние сплава. Чистый металл представляет собой однокомпонентную систему, сплав двух металлов - двухкомпонентную систему и т. д. Компонентами могут быть металлы и неметаллы, а также химические соединения.
Фазой называют однородную часть сплава, имеющую одинаковый состав одно и то же агрегатное состояние и отделенную от остальных частей сплава поверхностью раздела, при переходе через которую химический состав или структура вещества изменяются скачкообразно.
Совокупность фаз, находящихся в равновесии при определенных внешних условиях (давлении, температуре), называют системой.