- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химические свойства алкенов
Содержание
- 2. Основное содержание Химические свойства.Применение алкенов на примере непредельного углеводорода - этилена.
- 3. Реакции присоединения Химические свойства Гидрирование (присоединение молекулы
- 4. 2) Галогенирование (присоединения молекулы галогена) Реакции присоединения
- 5. 3) Гидрогалогенирование (присоединения галогеноводорода)Реакции присоединения CH3 –
- 6. 4) Гидратация (присоединения молекулы воды)Реакции присоединения CH2
- 7. 4) Гидратация (присоединения молекулы воды)Реакции присоединения CH3
- 8. реакция полимеризации n CH2═CH2
- 9. Твердостьплотностьплавкостьэлектропроводностьтеплопроводностьметаллический блескпластичностьЛегкие (ρ ≤ 5 г/см3)Li,
- 11. §4 упр.8Домашнее задание
- 12. Скачать презентацию
- 13. Похожие презентации
Основное содержание Химические свойства.Применение алкенов на примере непредельного углеводорода - этилена.






Слайд 2
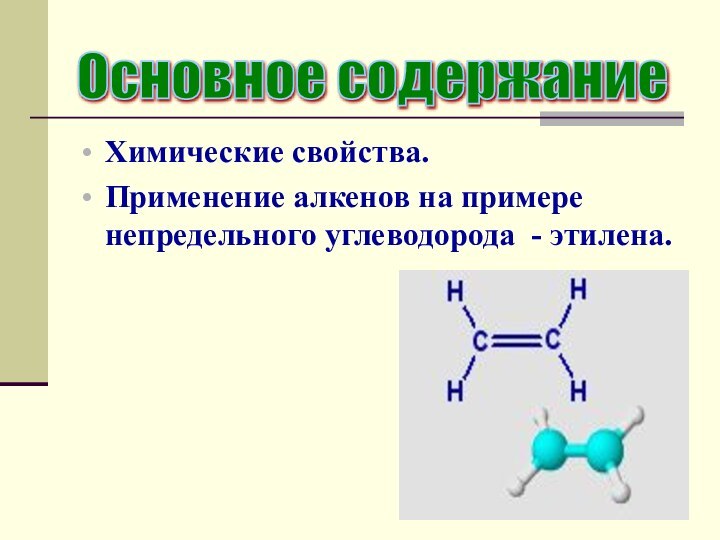
Основное содержание
Химические свойства.
Применение алкенов на примере непредельного
углеводорода - этилена.
Слайд 3
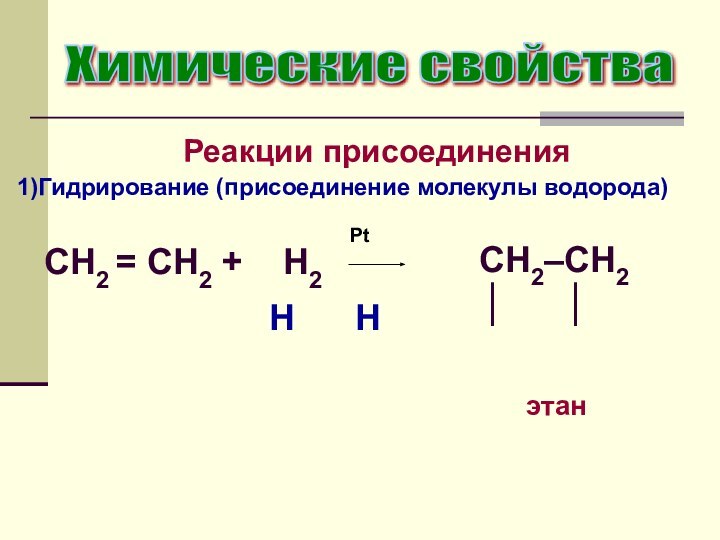
Реакции присоединения
Химические свойства
Гидрирование (присоединение молекулы водорода)
CH2
= CH2 + H2
Pt
CH2–CH2
│
│ этан
H H
Слайд 4
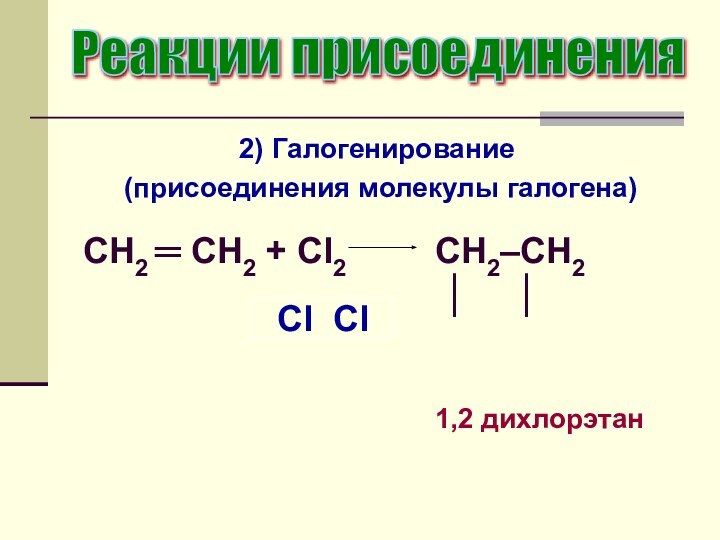
2) Галогенирование
(присоединения молекулы галогена)
Реакции присоединения
CH2
═ CH2 + Cl2
CH2–CH2
│ │
1,2
дихлорэтанCl Cl
Слайд 5
3) Гидрогалогенирование
(присоединения галогеноводорода)
Реакции присоединения
CH3 – CH
= СН2 + HBr
пропен
CH3 – CH – CH2
│ │ 2 – бромпропан
H
Правила Марковникова: при присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, т.е. атому, при котором больше атомов водорода, а галоген – к менее гидрированному.
Br
Слайд 6
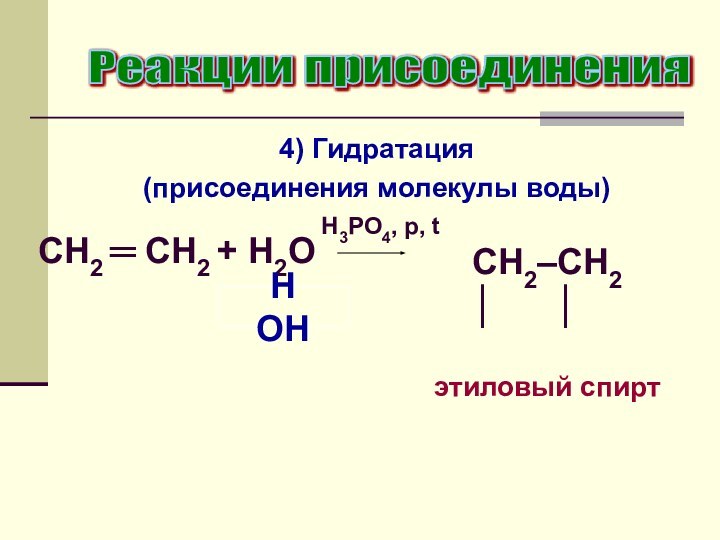
4) Гидратация
(присоединения молекулы воды)
Реакции присоединения
CH2 ═
CH2 + H2O
H3PO4, p, t
H OH
CH2–CH2
│ │этиловый спирт
Реакции присоединения
Реакции присоединения
Реакции присоединения
Слайд 7
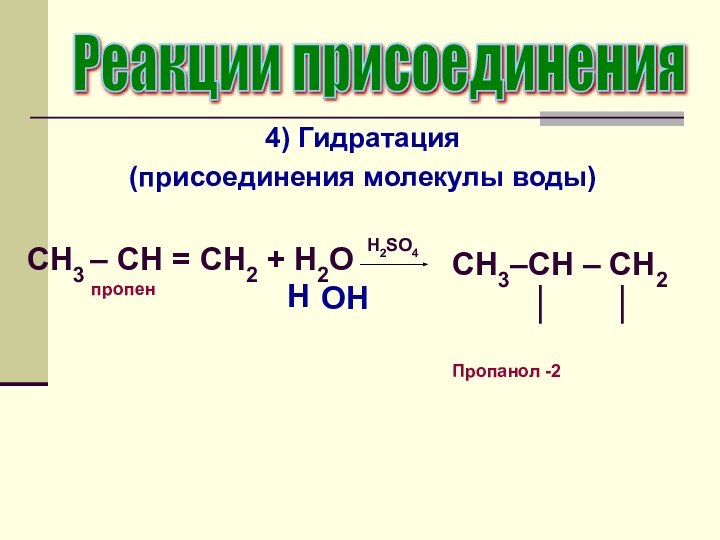
4) Гидратация
(присоединения молекулы воды)
Реакции присоединения
CH3 –
CH = CH2 + H2O
пропенH2SO4
H
CH3–CH – СН2
│ │
Пропанол -2
OH
Слайд 8
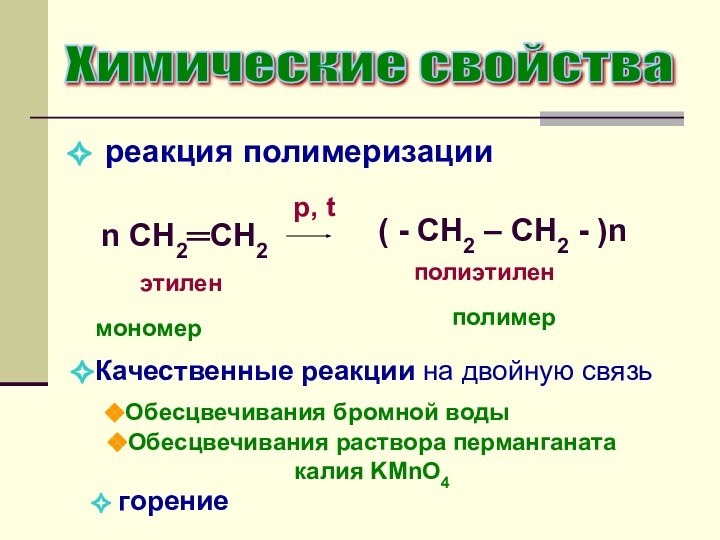
реакция полимеризации
n CH2═CH2
этилен
мономер
Химические свойства
p, t
( -
CH2 – CH2 - )nполиэтилен
полимер
Качественные реакции на двойную связь
Обесцвечивания бромной воды
Обесцвечивания раствора перманганата калия KMnO4
горение
Слайд 9
Твердость
плотность
плавкость
электропроводность
теплопроводность
металлический
блеск
пластичность
Легкие (ρ ≤ 5 г/см3)
Li, Na, K,
Mg, Al.
Тяжелые (ρ > 5 г/см3)
Zn, Cu, Sn, Pb,
Ag, AuPt