- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Основания, их классификация
Содержание
- 2. Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-ионов.
- 3. гироксид кальция Ca(OH)2гидроксид меди (II) Cu(OH)2 гидроксид
- 4. Единственное жидкое основание – гидроксид аммония NH4OH или водный раствор аммиака. гидроксид аммония NH4OH
- 5. Щёлочи(по растворимости в воде)
- 7. Вода H2O
- 8. Основаниягидроксид лития LiOHгидроксид калия KOHгидроксид натрия NaOHгидроксид
- 9. Щёлочи(по степени электролитической диссоциации основания )в водных
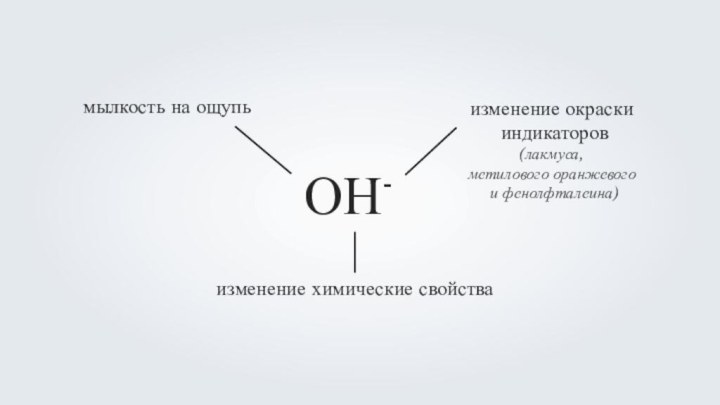
- 10. ОН-
- 11. Щёлочи(по степени электролитической диссоциации основания )в водных
- 12. Основаниягидроксид лития LiOHгидроксид калия KOHгидроксид натрия NaOHгидроксид аммония NH4OH
- 13. Щёлочи(по числу гидроксогрупп)содержат в составе своей молекулы
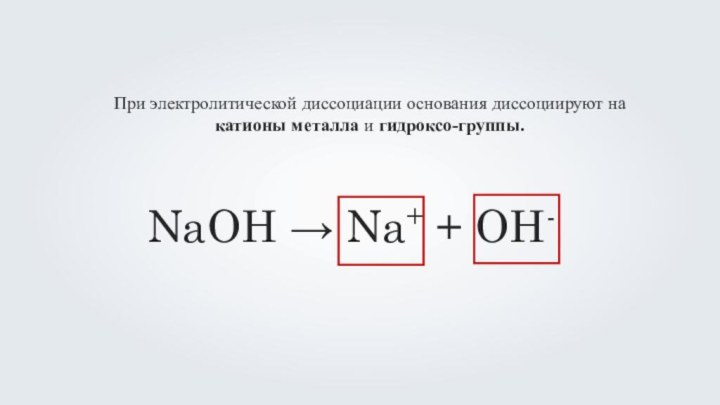
- 14. При электролитической диссоциации основания диссоциируют на катионы металла и гидроксо-группы.NaOH → Na+ + OH-
- 15. Диссоциация однокислотных основанийLiOH = Li+ + OH- При диссоциации молекулы однокислотного основания образуется один гидроксид-анион.
- 16. При диссоциации молекулы двухкислотного основания образуется два гидроксид-аниона.Диссоциация двухкислотных основанийBa(OH)2 = Ba2+ + 2OH-
- 17. При диссоциации молекулы трехкислотного основания образуется три гидроксид-аниона. Диссоциация трёхкислотных основанийAl(OH)3 = Al3+ + 3OH-
- 18. Скачать презентацию
- 19. Похожие презентации
Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-ионов.














Слайд 2
Основания – это сложные вещества, состоящие из ионов
металлов и связанных с ними гидроксид-ионов.
Слайд 3
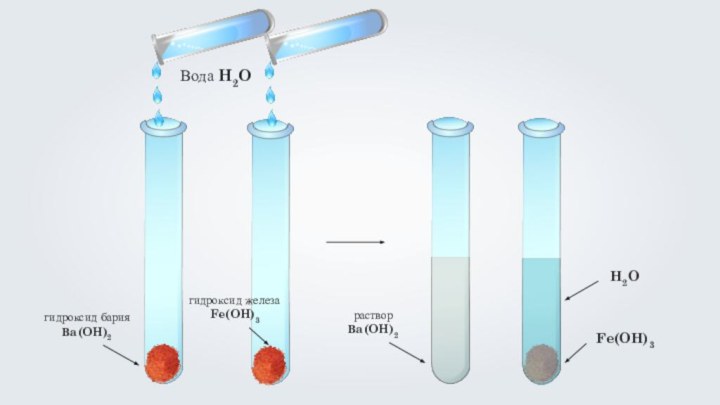
гироксид кальция Ca(OH)2
гидроксид меди (II) Cu(OH)2
гидроксид никеля
(II) Ni(OH)2
гидроксид железа (III) Fe(OH)3
Все основания – это
твердые вещества различные по окраске.
Слайд 4
Единственное жидкое основание – гидроксид аммония NH4OH или
водный раствор аммиака.
гидроксид аммония NH4OH
Слайд 8
Основания
гидроксид лития LiOH
гидроксид калия KOH
гидроксид натрия NaOH
гидроксид аммония
NH4OH
гидроксид бария Ba(OH)2
гидроксид алюминия Al(OH)3
гидроксид магния Mg(OH)2
гидроксид железа (II) Fe(OH)2
гидроксид цинка (II) Zn(OH)2
гидроксид меди (II) Сu(OH)2
Слайд 9
Щёлочи
(по степени электролитической диссоциации основания )
в водных растворах
полностью диссоциируют
на отдельные ионы
NaOH → Na+ + OH-
при
растворении в воде в растворе одновременно
присутствуют и ионы
и молекулы вещества
Слайд 11
Щёлочи
(по степени электролитической диссоциации основания )
в водных растворах
полностью диссоциируют
на отдельные ионы
NaOH → Na+ + OH-
при
растворении в воде в растворе одновременно
присутствуют и ионы
и молекулы вещества
Слайд 12
Основания
гидроксид лития LiOH
гидроксид калия KOH
гидроксид натрия NaOH
гидроксид аммония
NH4OH
Слайд 13
Щёлочи
(по числу гидроксогрупп)
содержат в составе своей молекулы одну
гидроксид группу ОН
гидроксид лития LiOH
гидроксид калия KOH
гидроксид натрия NaOH
содержат
в составе своей молекулы две гидроксид группы ОНгидроксид бария Ba(OH)2
гидроксид магния Mg(OH)2
гидроксид железа Fe(OH)2
содержат в составе своей молекулы три гидроксид группы ОН
гидроксид алюминия Al(OH)3
гидроксид железа Fe(OH)3