- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Соляная кислота и её соли
Содержание
- 2. « Просто знать - ещё не всё, знания нужно уметь использовать».Гёте
- 3. видео
- 4. Получение соляной кислоты: 1.В промышленности получают сжиганием
- 5. Химические свойства: 1. Изменение окраски индикатора (лакмус-
- 6. Вывод:Если металл находится в ряду, составленном Н.Н.Бекетовым,
- 7. 3. Взаимодействует с основными и амфотерными оксидами: MgO
- 8. 4. Взаимодействует с основаниями:HCl + KOH →
- 9. 5. Взаимодействует с солямиРяд кислот
- 10. Вывод:В соответствии с рядом кислот, каждая предыдущая
- 11. 6. Взаимодействует с нитратом серебра HCl + AgNO3
- 12. Вывод:Нитрат серебра является реактивом на соляную кислоту
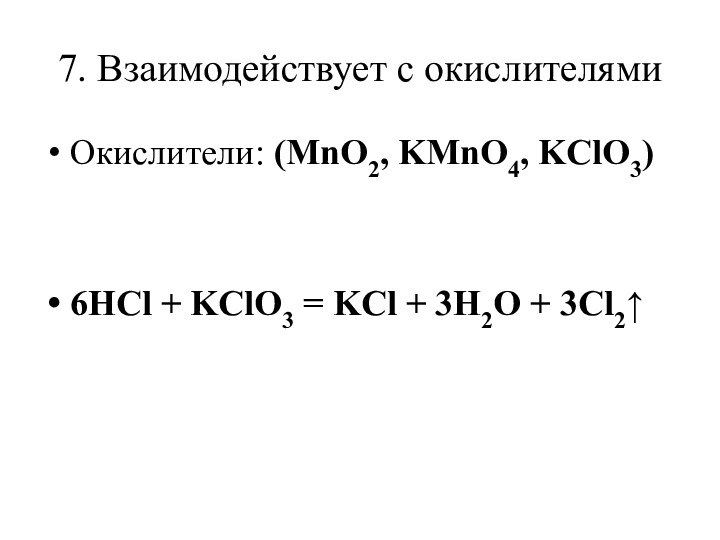
- 13. 7. Взаимодействует с окислителямиОкислители: (MnO2, KMnO4, KClO3) 6HCl + KClO3 = KCl + 3H2O + 3Cl2↑
- 14. Вывод:Во всех нами изученных реакциях получились хлориды- соли соляной кислоты.
- 15. Применение соляной кислотыВходит в состав желудочного сока
- 16. Применение солей - хлоридов KCl - удобрение,
- 17. Задания для закрепления №1. Осуществите превращения по
- 18. №3. Решите задачу: Какое количество алюминия прореагирует
- 19. Скачать презентацию
- 20. Похожие презентации
« Просто знать - ещё не всё, знания нужно уметь использовать».Гёте


















Слайд 4
Получение соляной кислоты:
1.В промышленности получают сжиганием водорода в
хлоре и растворением продукта реакции в воде.
2.В лаборатории
H2SO4
+2NaCl →2HCl ↑ + Na2SO4Этот газ легко растворяется в воде: до 450 объемов хлороводорода - в одном объеме воды.
Слайд 5
Химические свойства:
1. Изменение окраски индикатора (лакмус- красный)
2. Взаимодействует
с металлами
Mg + 2HCl → MgCl2 + H2
2Al +
6HCl → 2AlCl3 + 3H2Cu + HCl →
Слайд 6
Вывод:
Если металл находится в ряду, составленном Н.Н.Бекетовым, до
водорода, то выделяется водород и образуется соль.
Исключение HNO3
(выделяются другие газы)
Слайд 7
3. Взаимодействует с основными и амфотерными оксидами:
MgO +
2HCl → MgCl2 + H2O
ZnO + 2 HCl→ ZnCl2
+ H2OОбразуются соль и вода
Слайд 8
4. Взаимодействует с основаниями:
HCl + KOH → KCl
+ H2O
3HCl + Al(OH)3 → AlCl3 + 3H2O
Образуются соль
и вода
Слайд 9
5. Взаимодействует с солями
Ряд кислот
HNO3
H2SO4, HCl,
H2SO3, H2CO3, H2S, H2SiO3────────────────────────►
H3PO4
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
Слайд 10
Вывод:
В соответствии с рядом кислот, каждая предыдущая кислота
может вытеснить из соли последующую, образуется другая кислота и
другая соль.
Слайд 11
6. Взаимодействует с нитратом серебра
HCl + AgNO3 →
AgCl↓ + HNO3
выпадает осадок белого цвета, который не растворяется
ни в воде, ни в кислотах.
Слайд 12
Вывод:
Нитрат серебра является реактивом
на соляную кислоту и
её соли т.е.
используется в качестве качественной реакции, для
распознавания хлорид-ионов.
Слайд 13
7. Взаимодействует с окислителями
Окислители: (MnO2, KMnO4, KClO3)
6HCl +
KClO3 = KCl + 3H2O + 3Cl2↑
Слайд 15
Применение соляной кислоты
Входит в состав желудочного сока и
способствует перевариванию белковой пищи
Для производства лекарств, красителей, растворителей, пластмасс.
Слайд 16
Применение солей - хлоридов
KCl - удобрение, используется также
в стекольной и химической промышленности.
HgCl2 - сулема - яд,
для дезинфекции в медицине, для протравливания семян в сельском хозяйстве.ZnCl2 - для пропитки древесины против гниения, в медицине, при паянии.
Слайд 17
Задания для закрепления
№1. Осуществите превращения по схеме:
HCl →
Cl2 → AlCl3 →Al(OH)3 → Al2O3 →AlCl3 → Cl2
№2.
Даны вещества:Zn, Cu, Al, MgO, SiO2, Fe2O3, NaOH, Al(OH)3, Fe2(SO4)3, CaCO3, Fe(NO3)3
Какие из указанных веществ будут реагировать с соляной кислотой. Составьте уравнения химических реакций