Слайд 2
Основная причина злокачественных новообразований – генетические факторы.
Рак
– заболевание генома.
1) наличие в опухолевых тканях большого числа
хромосомных перестроек, как численных изменений числа хромосом, так и их структурных повреждений.
2) наличие в опухолевых тканях большого числа мутаций в генах.
3) существование наследственных форм рака
4) онкогенное действие ряда вирусов, способных взаимодействовать с геномом хозяина и встраиваться в молекулы ДНК.
5) химические вещества и физические воздействия, обладающие мутагенным эффектом, имеют также и канцерогенный эффект.
Слайд 4
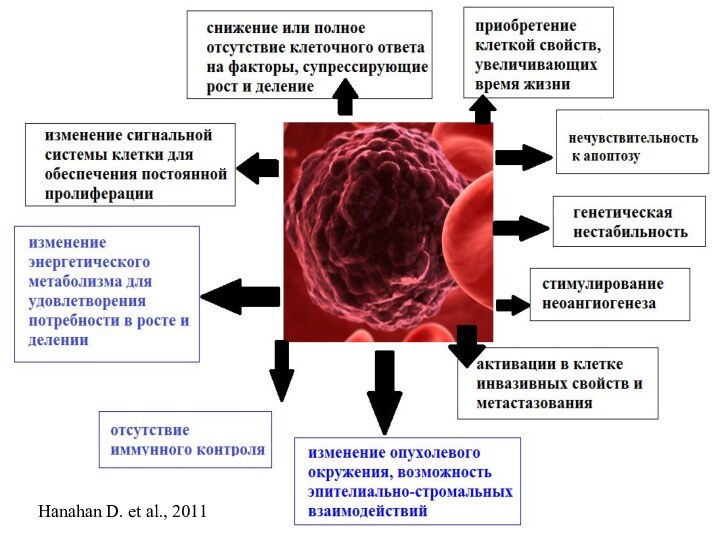
Нестабильность генома - отличительная характеристика опухолевой клетки
Генетическая
нестабильность
Наличие изменений в хромосомах, как числа хромосом (анеуплоидия и
полиплоидия), так и внутренних хромосомных перестроек (делеций, инсерций, транслокаций)
Наличие точковых мутаций в генах , приводящих к активации или инактивации генной функции
Существование нестабильности микросателлитных повторов
Эпигенетическая нестабильность
Нарушение баланса метилирования/деметилирования
Деметилирование транспозонов и вирусных частиц, инактивированных в нормальной клетке
Деметилирование гетерохроматина, в том числе и центромерного, что приводит к нарушению распределения хромосом при делении клетки
Гиперметилирование регуляторных районов генов-супрессоров, приводящее к отсутствию их экспрессии
Образование опухоли
Слайд 5
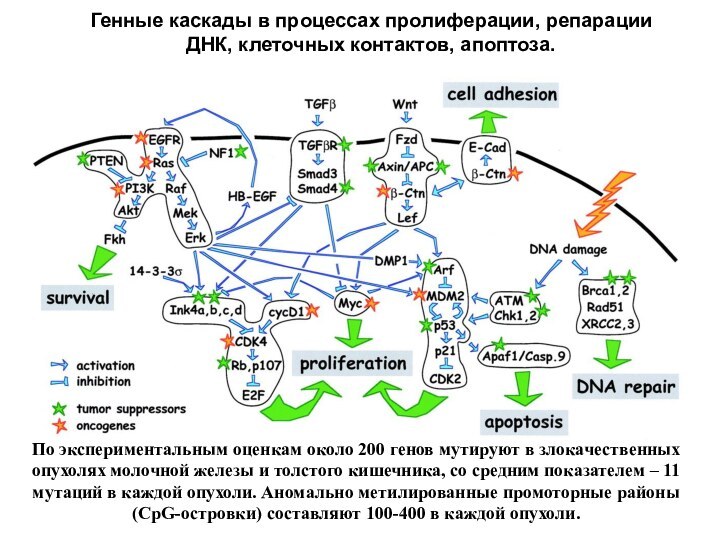
Генные каскады в процессах пролиферации, репарации ДНК, клеточных
контактов, апоптоза.
По экспериментальным оценкам около 200 генов мутируют в
злокачественных опухолях молочной железы и толстого кишечника, со средним показателем – 11 мутаций в каждой опухоли. Аномально метилированные промоторные районы (CpG-островки) составляют 100-400 в каждой опухоли.
Слайд 7
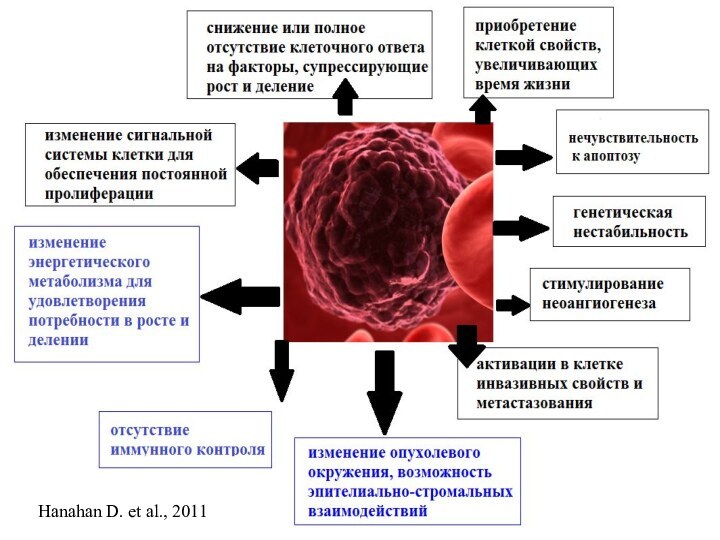
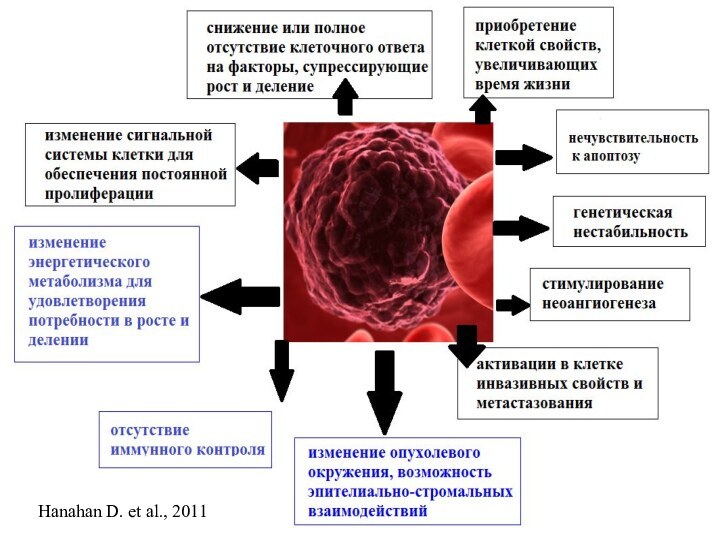
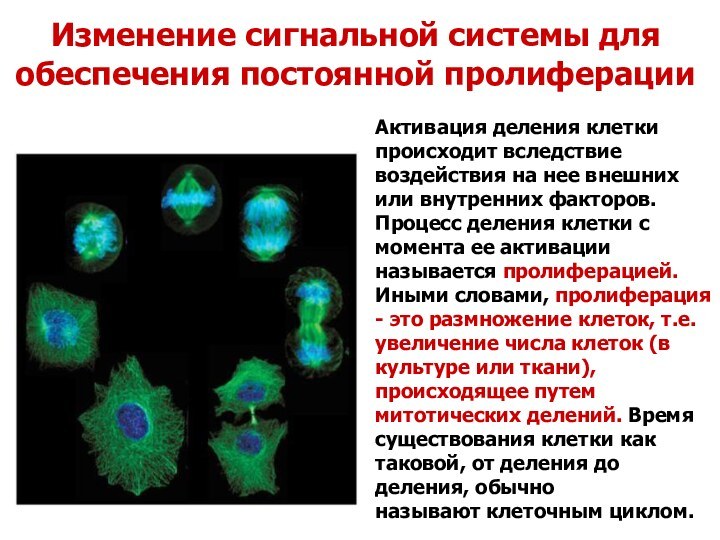
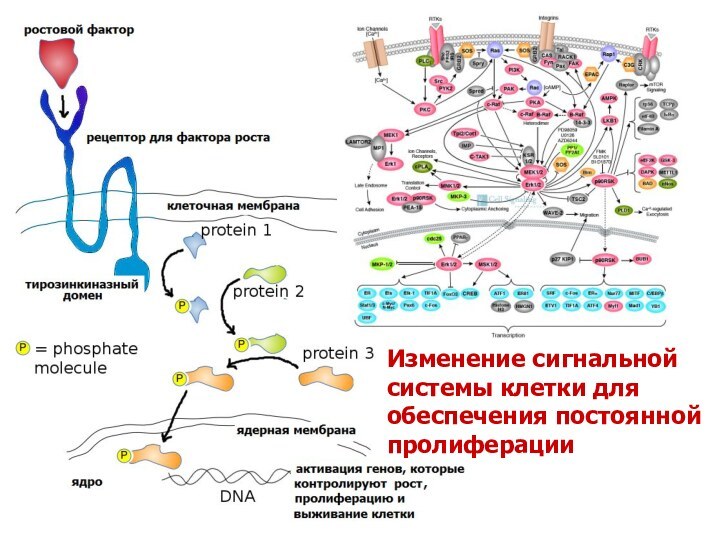
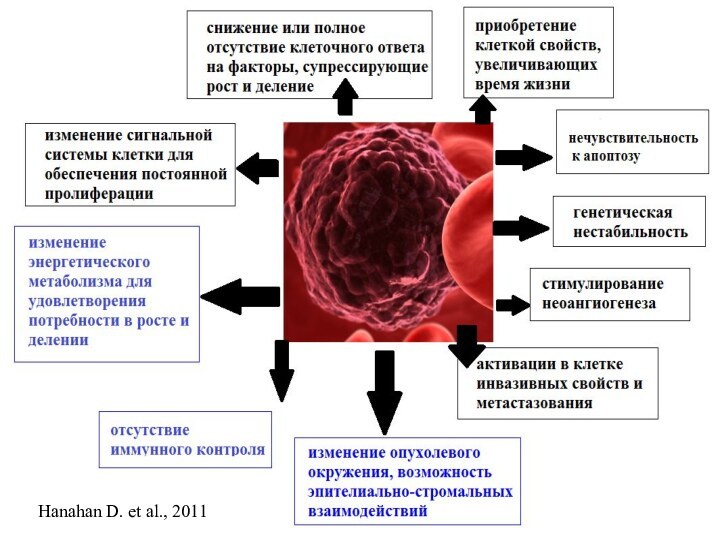
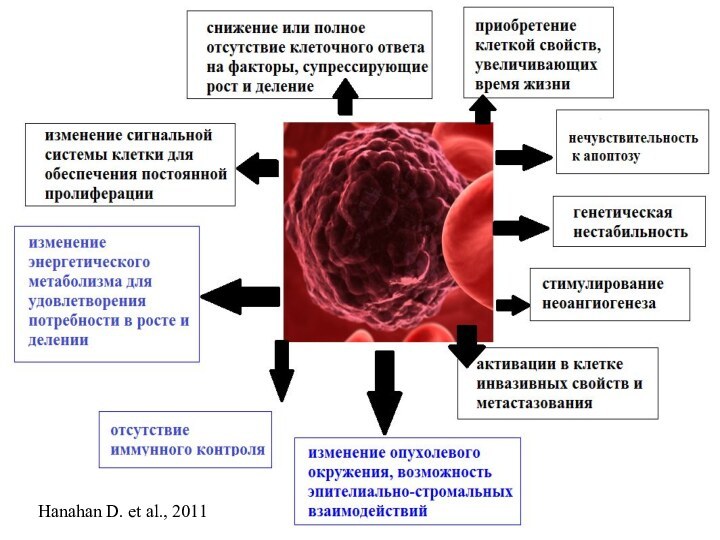
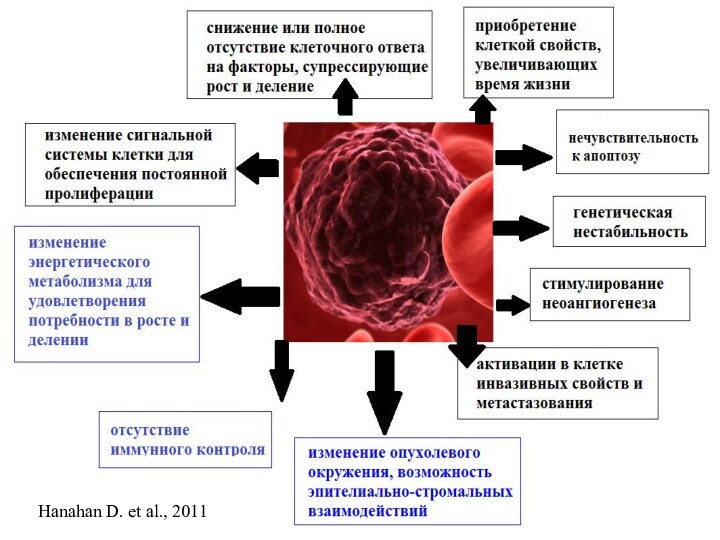
Изменение сигнальной системы для обеспечения постоянной пролиферации
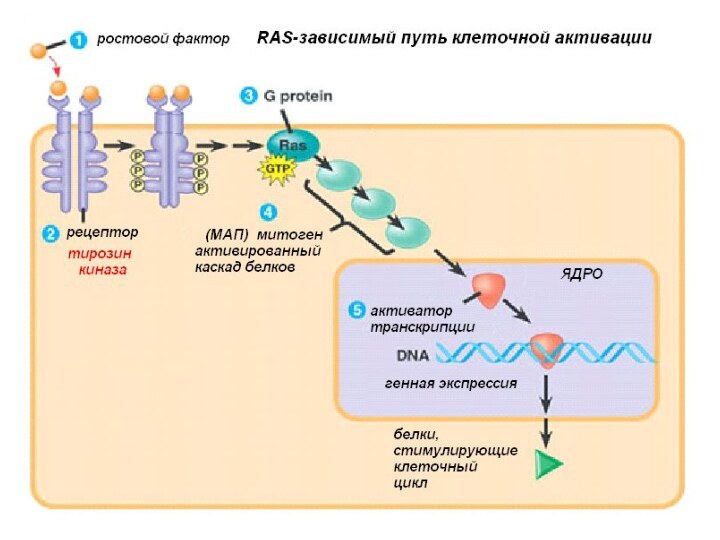
Активация деления
клетки происходит вследствие воздействия на нее внешних или внутренних
факторов.
Процесс деления клетки с момента ее активации называется пролиферацией. Иными словами, пролиферация - это размножение клеток, т.е. увеличение числа клеток (в культуре или ткани), происходящее путем митотических делений. Время существования клетки как таковой, от деления до деления, обычно называют клеточным циклом.
Слайд 8
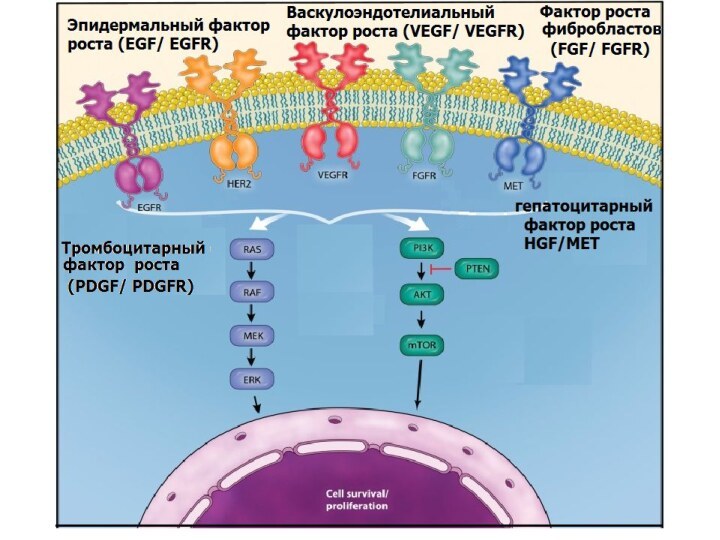
Изменение сигнальной системы клетки для обеспечения постоянной пролиферации
Слайд 11
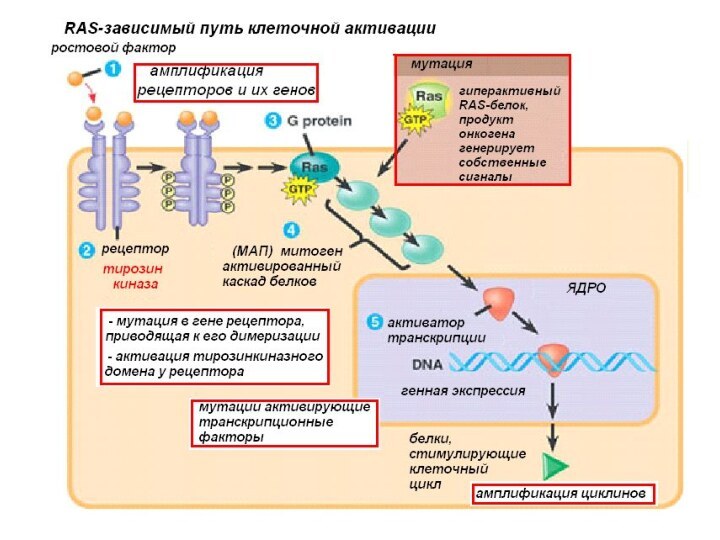
Активация сигнальной системы клетки в опухоли
Во-первых, опухолевые
клетки могут сами вырабатывать факторы роста, в результате амплификации
или мутации в генах, кодирующих ростовые факторы. Клетки опухоли могут сами посылать сигнал, стимулируя нормальные клетки опухоль-ассоциированной стромы к выработке различных, необходимых для них факторов роста. Увеличение концентрации факторов роста приводит к стимуляции пролиферации.
Во-вторых, к изменению сигнальной системы в опухолевых клетках может привести увеличение уровня рецепторов, расположенных на их поверхности, что приводит такие клетки в гиперчувствительное состояние по отношению фактору роста.
Слайд 12
В-третьих, аналогичные последствия могут быть вызваны мутациями или
перестройками в генах, кодирующих рецепторы факторов роста, что приведет
к изменениям в молекуле рецептора. Мутантный рецептор может иметь постоянно активированный тирозинкиназный домен, или находиться в комплексе с другими молекулами, что приведет либо к запуску системы, независимо от наличия ростового фактора, либо к ее запуску при взаимодействии с неспецифическим лигандом.
В-четвертых, активация сигнальной системы опухолевой клетки может возникать независимо от факторов роста и их рецепторов - на нижестоящих уровнях регуляции, независимо от образования комплекса лиганд-рецептор.
Слайд 14
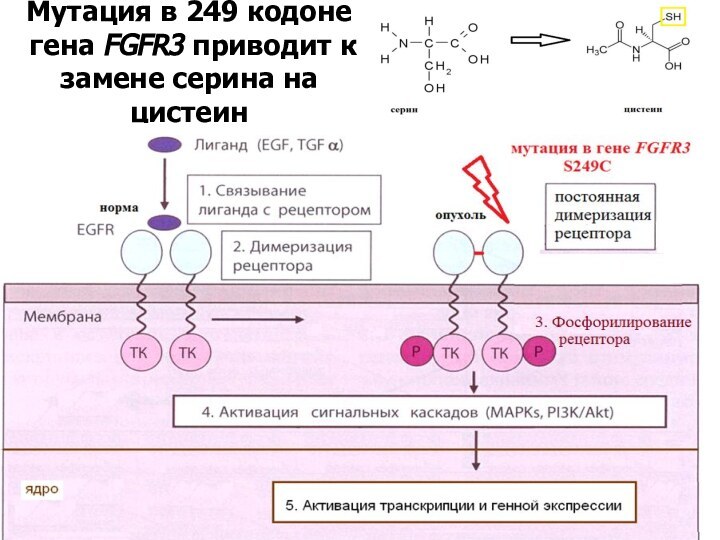
Мутация в 249 кодоне
гена FGFR3 приводит к
замене серина на цистеин
Слайд 15
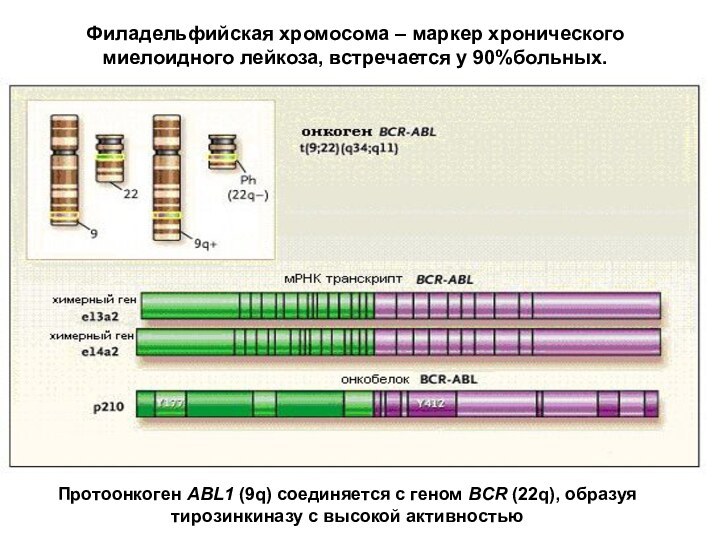
Филадельфийская хромосома – маркер хронического миелоидного лейкоза, встречается
у 90%больных.
Протоонкоген ABL1 (9q) соединяется с геном BCR (22q),
образуя тирозинкиназу с высокой активностью
Слайд 17
Во взрослом организме человека клетки различных тканей и
органов имеют неодинаковую способность к делению. При старении интенсивность
пролиферации клеток снижается, увеличивается интервал между митозами.
Еще в 60-ых годах прошлого века Леонард Хейфлик установил, что в клеточных культурах соматические клетки человека способны делиться ограниченное число раз. При этом предельное число делений (названное лимитом Хейфлика) сильно зависит от возраста индивидуума, которому эти клетки принадлежат: так клетки
новорожденных делились 80-90 раз, а 70-летние 20-30 раз.
Достигнув лимита клетки, переходили в состояние сенесенса – одряхления, которое характеризовалось резким изменением метаболизм, и в первую очередь нарушением репликации ДНК, а затем наступала гибель клеток.
Приобретение клеткой свойств, увеличивающих время жизни
Слайд 18
1. Теломераза синтезирует теломерные ДНК- последовательности, идущие от
5’ к 3’концу по направлению к окончаниям хромосом. Восстановление
хромосомной ДНК необходимо для компенсации укорочения, которое возникает в результате активности нуклеазы и неполной концевой ДНК-репликации.
2. Критически короткие теломеры (3000-5000 пар нуклеотидов или менее 2 кb) неспособны защитить хромосомы от повреждения при деление клетки. Их появление является сигналом для выхода клеток из митотического цикла. Если этой величины достигает хотя бы одна теломера, то в клетке происходит резкое изменение метаболизма, и в первую очередь нарушение репликации ДНК, которые запускают механизмы клеточного сенесенса (репликативное старение) и апоптоза (гибель, разрушение клетки).
Слайд 19
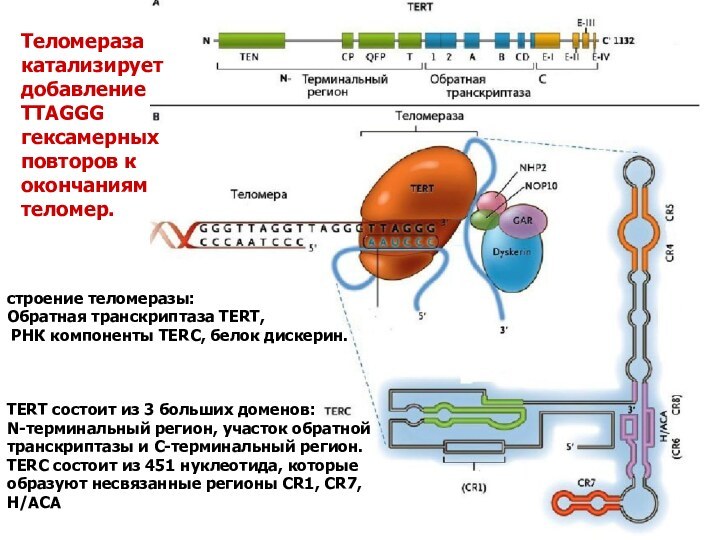
строение теломеразы:
Обратная транскриптаза TERT,
РНК компоненты TERC, белок
дискерин.
TERT состоит из 3 больших доменов:
N-терминальный регион,
участок обратной
транскриптазы и С-терминальный регион.
TERC состоит из 451 нуклеотида, которые
образуют несвязанные регионы CR1, CR7,
H/ACA
Теломераза катализирует добавление
TTAGGG гексамерных повторов к
окончаниям теломер.
Слайд 21
Термин"апоптоз", предложенный в 1972 г. английскими учеными J.F.R.
Кеrr, А.Н. Wyllie и A.R. Currie, состоит из двух
греческих слов и означает в буквальном смысле "отделение лепестков от цветов", а применимо к клетке - особый тип смерти путем разделения ее на части (" апоптозные тельца "), которые впоследствии фагоцитируются соседними клетками разного типа.
Термин "программированная клеточная смерть" отражает функциональное назначение этого процесса, представляюет естественную часть жизни многоклеточного организма, связанного с метаморфозом и развитием.
Слайд 22
У млекопитающих апоптоз часто начинается с активации так

называемых "индуцирующих смерть сигнальных комплексов" на плазматической мембране. Эти
комплексы образуются при взаимодействии определенных внеклеточных лигандов - например, Fas или TNF (tumor necrosis factor) с белками семейства рецепторов фактора некроза опухолей ( TNFR ) на клеточной мембране, называемых "рецепторами смерти".
Рецепторы смерти имеют прямую связь с механизмом апоптоза. Сигналы выживания от окружения клетки и от внутренних сенсоров контролирующих целостность клетки нормально поддерживают механизм апоптоза в состоянии готовности. В случае, если клетка теряет контакт с окружением или в ней поисходит невосстановимое внутреннее повреждение, клетка входит в апоптоз. Клетки, которые одновременно получают конфликтующие сигналы о продолжении или прекращении цикла деления также переходят в апоптоз.
Рецепторы смерти - поверхностные рецепторы клетки, которые передают апоптические сигналы инициируемые специфическими " лигандами смерти " - играют главную роль в апоптозе. Эти рецепторы могут активировать стимулирующие смерть каспазы за время порядка секунд с момента связывания лигандов, вызывая апоптическое разрушение клетки в течение часов.
Рецепторы смерти принадлежат к суперсемейству фактора некроза опухолей (TNF) , и все они имеют сходные внеклеточные домены богатые цистеином. Рецепторы смерти содержат вдобавок гомологичную последовательность, называемую домен смерти.
Слайд 24
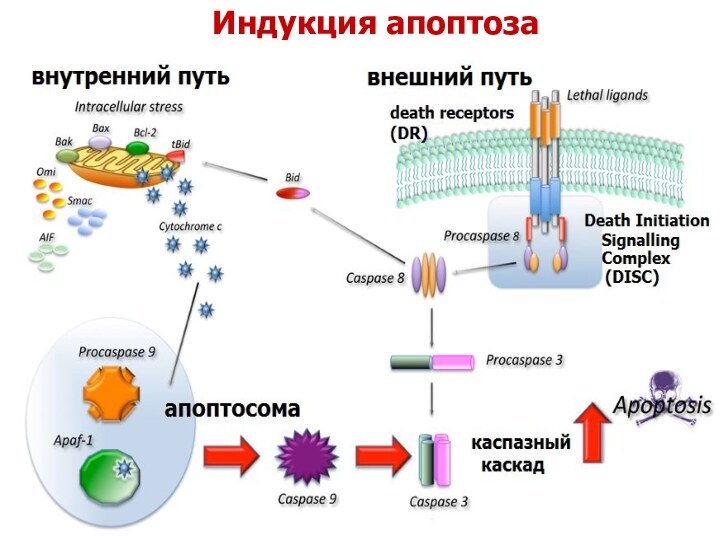
Внешний путь активации апоптоза
Внешний путь начинается со
связывания CD95 со своим лигандом, CD95L. В результате этого
происходит димеризация рецептора и, соответственно, его цитоплазматических доменов смерти, которые активируют внутриклеточный адаптерный белок FADD. Этот белок активирует прокаспазу 8, которая формирует смерть-индуцирующий сигнальный комплекс (DISK). Прокаспаза 8 активируется путем расщепления на более мелкие субъединицы, высвобождая каспазу 8. Каспаза 8 затем активирует другие каспазы, такие как каспаза 3 (исполняющая каспаза), которая расщепляет ДНК и другие субстраты, вызывая гибель клетки.
Слайд 25
Внутренний путь апоптоза запускается различными воздействиями (отсутствие ростовых

факторов, стресс и повреждение). Активация этого пути ведет к
повышению проницаемости наружной мембраны митохондрий с последующим выходом цитохрома C, который инициирует апоптоз.
Целостность митохондриальной мембраны регулируется про- и антиапоптотическими белками семейства BCL2. Активность проапоптотических белков, BAX и BAK ингибируется антиапоптотическими белками семейства BCL2 и BCL-XL. Третья группа белков (т.н. BH3-only белки: BAD, BID и PUMA) регулируют баланс между про- и антиапоптотическими членами семейства BCL2. BH3-only белки стимулируют апоптоз, нейтрализуя действие антиапоптотических белков (BCL2, BCL-XL). Когда суммарный эффект всех экспрессируемых белков BH3 «перекрывает» антиапоптотическое действие белков BCL2/BCL-XL, белки BAX и BAK активируются и формируют поры в митохондриальной мембране. Цитохром с выходит в цитозоль, где связывается с APAF-1, активируя каспазу 9.
Внутренний путь активации апоптоза
Слайд 27
Опухолевые клетки используют разные возможности для ограничения или
обхода апоптоза.
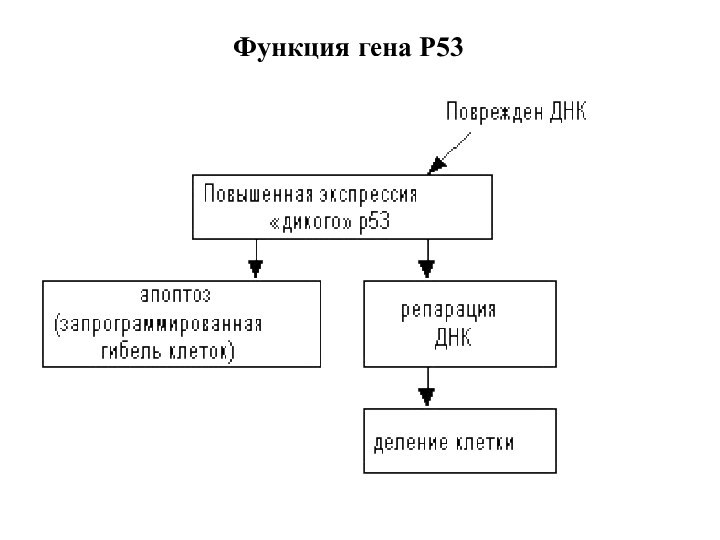
Опухоли часто ингибируют функцию ТР53, что устраняет
этот критический фактор из схемы индуцированного апоптоза.
Опухоли могут увеличивать экспрессию антиапоптотических регуляторов (Bcl-2, Bcl-xL) и сигналов выживания (ИФР-1, ИФР-2) или снижают уровень проапоптотических факторов (Bax, Bim, Puma)
Опухоли могут ингибировать апоптоз, который стимулируется внешним лигандом.
Слайд 29
Активация в клетке свойств инвазии и метастазирования
Опухолевая
инвазия — процесс, при котором опухолевые клетки или группы
клеток распространяются из первичного очага опухоли в соседние ткани. В случае карцином этот процесс включает проникновение опухолевых клеток через разрушаемую ими базальную мембрану.
Слайд 30
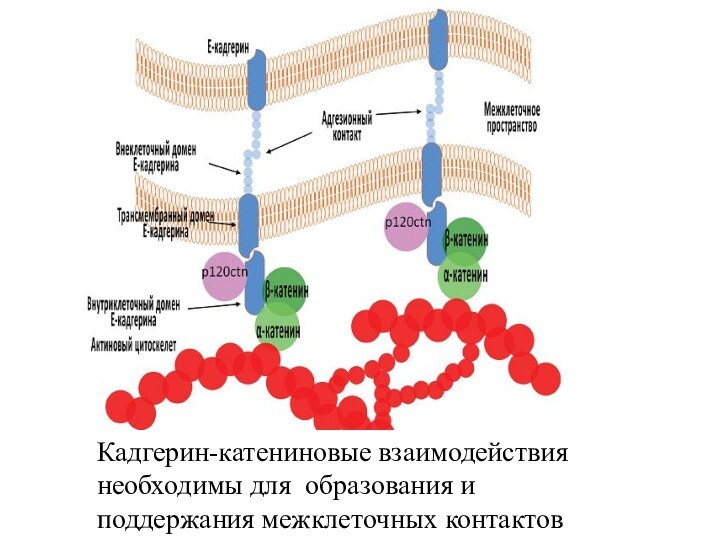
Кадгерин-катениновые взаимодействия необходимы для образования и поддержания межклеточных
контактов
Слайд 31
Ген CDH1 локализуется на хромосоме 16q22.1, занимая объем
около 100 кб. CDH1 содержит 16 экзонов и 15
интронов. Наследственные мутации гена CDH1 обнаружены только в семьях с диффузным РЖ и никогда в семьях с интестинальным РЖ. Наследственные мутации CDH1 распределены относительно равномерно по всему гену, 70% нонсенс и 30% миссенс мутации.
Слайд 32
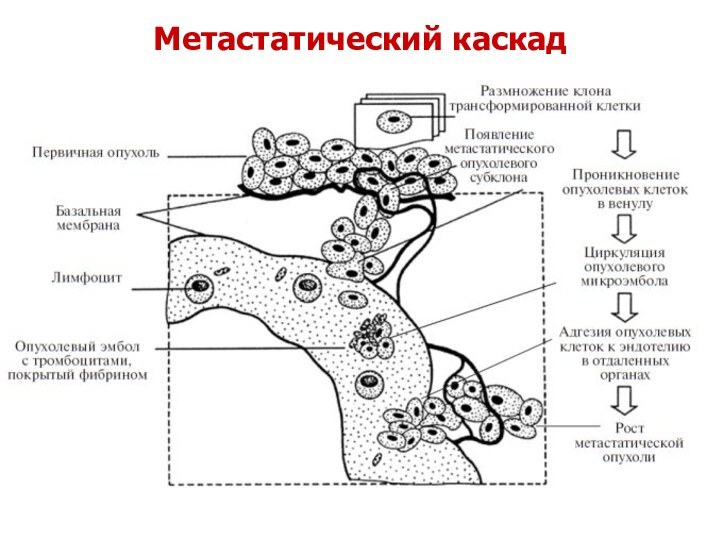
Инвазия является первым этапом сложного инвазивно-метастатического каскада, приводящего
в дальнейшем к метастазированию.
Основным признаком инвазии служит прорыв
базальной мембраны и выход опухолевых клеток за её пределы, позволяющий им приобретать дополнительные преимущества (улучшенное обеспечение кислородом и питательными веществами).
Слайд 33
Коллективная миграция
Коллективная миграция, представляя собой
один из вариантов инвазивного
роста,
характеризуется миграцией целых групп
клеток, соединенных между собой посредством
молекул
адгезии и коммуникационных контактов.
Коллективную клеточную миграцию наблюдали
при развитии и прогрессировании рака молочной
железы и эндометрия, рака предстательной
железы, колоректального рака, крупноклеточного
рака легкого, рабдомиосаркомы, меланомы, а также
большинства плоскоклеточных карцином.
Слайд 34
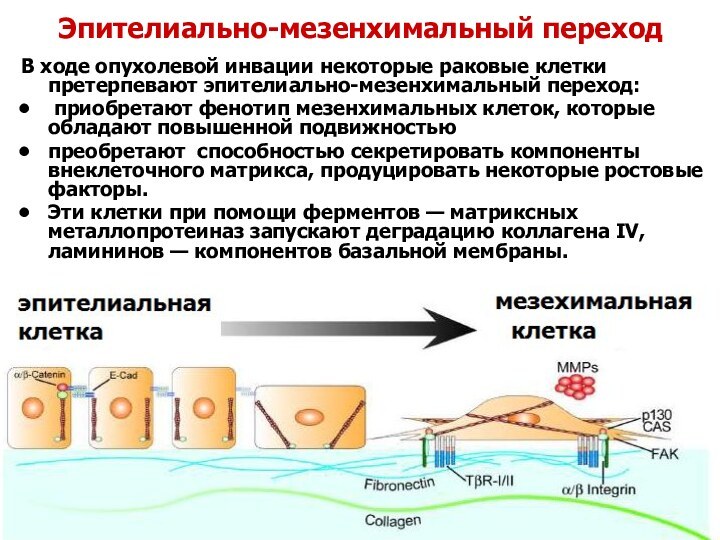
Эпителиально-мезенхимальный переход
В ходе опухолевой инвации некоторые раковые клетки
претерпевают эпителиально-мезенхимальный переход:
приобретают фенотип мезенхимальных клеток, которые обладают
повышенной подвижностью
преобретают способностью секретировать компоненты внеклеточного матрикса, продуцировать некоторые ростовые факторы.
Эти клетки при помощи ферментов — матриксных металлопротеиназ запускают деградацию коллагена IV, ламининов — компонентов базальной мембраны.
Слайд 36
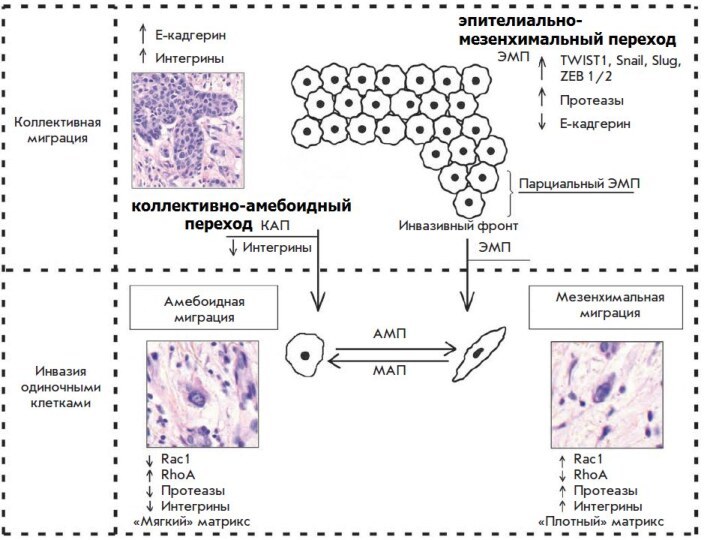
Процессы инвазивного роста обладают определенной пластичностью и возможностью
«переключения» в рамках индивидуальной клеточной инвазии с одного типа
миграции на другой (с мезенхимального на амебоидный и наоборот).
Это обусловлено возникновением изменений в активности определенных клеточных молекул и необходимостью адаптироваться к условиям тканевого микроокружения.
Слайд 37
Закономерности метастатического распространения
Процесс метастазирования не хаотичен, как представлялось
раньше, а подчиняется строго регулируемым биологическим и информационным механизмам;
Метастзирование
– волнообразный и дискретный процесс, имеет множество промежуточных стадий;
Ход метастазирования может как ускоряться, так и замедляться под воздействием определенных факторов;
Каждая ступень метастатического каскада может быть мишенью и объектом противоопухолевой терапии.
Слайд 40
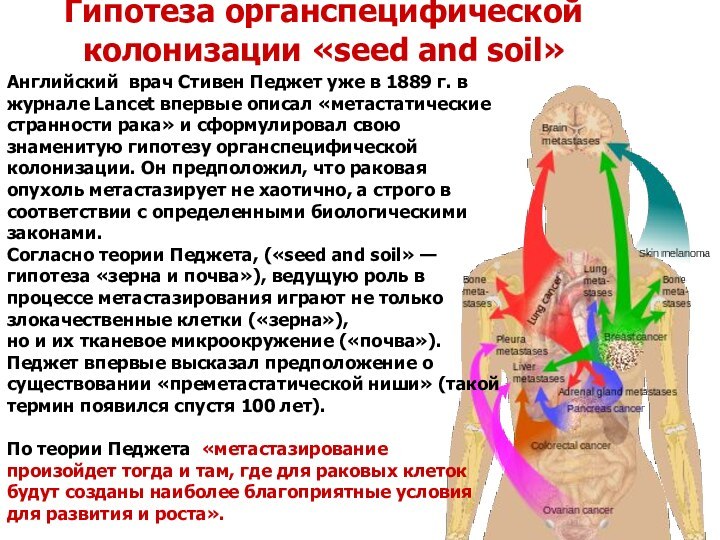
Гипотеза органспецифической колонизации «seed and soil»
Английский врач Стивен
Педжет уже в 1889 г. в журнале Lancet впервые
описал «метастатические странности рака» и сформулировал свою знаменитую гипотезу органспецифической колонизации. Он предположил, что раковая опухоль метастазирует не хаотично, а строго в соответствии с определенными биологическими законами.
Согласно теории Педжета, («seed and soil» — гипотеза «зерна и почва»), ведущую роль в процессе метастазирования играют не только злокачественные клетки («зерна»),
но и их тканевое микроокружение («почва»). Педжет впервые высказал предположение о существовании «преметастатической ниши» (такой термин появился спустя 100 лет).
По теории Педжета «метастазирование произойдет тогда и там, где для раковых клеток будут созданы наиболее благоприятные условия для развития и роста».
Слайд 41
Теории метастазирования
Гуморальные теории
Рудольф Вирхов, находясь под

влиянием гуморальной теории Галена, считал, что опухоли метастазируют «клеточными
ядами».
Циркулирующие клетки
Первым обнаружил инвазию раковыми клетками вен и лимфатических сосудов Карл Тирш (1865 г.). Впоследствии циркулирующие в крови опухолевые клетки (ЦОК) «метастазы в кровь» стали объектом пристального изучения онкологов.
Механическая сосудистая теория Юинга
В 1920-х гг. Джеймс Юинг, «шеф американских патоморфологов», оспаривая теорию Педжета, считал, что развитие метастазов в отдаленных органах обусловлено, в основном, анатомическими и механическими факторами. Юинг предполагал, что опухолевые клетки попадают в ловушку капиллярной сети, где и происходит их экстравазация с последующим формированием метастатических очагов. Согласно «механической» сосудистой теории метастазирования Юинга вероятность развития метастазов в отдаленном органе зависит от плотности сосудов и интенсивности кровообращения в нем. Такая точка зрения существовала в практической онкологии вплоть до 1980-х гг., так считает большинство практикующих онкологов в возрасте.
Слайд 42
Теория линейной прогрессии принадлежит Уильяму Холстеду. До 1960-х
гг. считалось, что раковые клетки из первичной опухоли вначале
обязательно должны попасть в регионарные лимфатические узлы, а затем гематогенным путем — в отдаленные висцеральные органы.
Из гипотезы линейной прогрессии следует, что формируют метастазы только раковые клетки, которые обладают высоким злокачественным потенциалом. Метастазирование начинается на поздних стадиях рака и также возможно развитие метастаза из метастаза.
Альтернативная теория метастазирования Бернарда Фишера – теория ранней диссеминации
он рассмативал канцерогенез как системное явление, канцерогенез в солидных опухолях он приравнивал к канцерогенезу при гемобластозах.
Концепция Фишера объясняла появление метахронных метастазов после, казалось бы, «радикального» лечения первичной опухоли и привела к возникновению теории адъювантной терапии.
Слайд 43
Гипотеза параллельной прогрессии
Продолжением теории ранней диссеминации опухолевых

клеток стала гипотеза параллельной прогрессии, предложенная Кристофером Кляйном (Nature
Reviews Cancer, April 2009).
Согласно этой гипотезе процесс метастазирования начинается на самых ранних стадиях канцерогенеза, сразу после активации в клетке протоонкогенов, а не в результате длительного накопления онкогенных мутаций отдельными клеточными клонами в первичной опухоли. Эпителиальная клетка уже после фазы инициации способна активировать скрытые эмбриональные программы эпителиально-мезенхимального перехода, приобретать нехарактерную для нее патологическую подвижность, разрушать базальную мембрану, проникать в системный кровоток, достигать преметастатической ниши в тканях отдаленного органа и формировать метастаз.
Исходя из теории ранней диссеминации, сформулированой К. Кляйном in silico, формирование метастаза происходит независимо и параллельно с ростом первичной опухоли, что было доказано в эксперименте.
Эта концепция позволяет объяснить наличие метастазов опухоли без выявленной первичной локализации и отдаленных метастазов при ранних клинических стадиях рака (T1-2N0M1), а также частые различия в рецепторных и генетических характеристиках первичной опухоли и ее метастазов.
Слайд 46
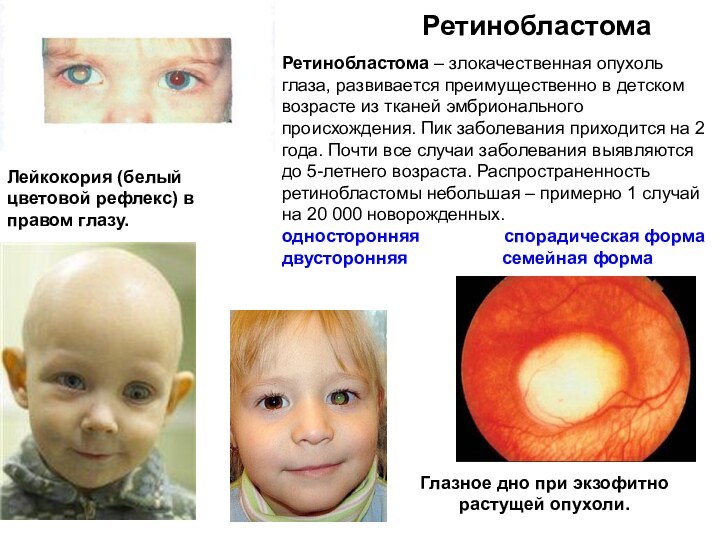
Ретинобластома
Глазное дно при экзофитно растущей опухоли.
Лейкокория
(белый цветовой рефлекс) в правом глазу.
Ретинобластома – злокачественная
опухоль глаза, развивается преимущественно в детском возрасте из тканей эмбрионального происхождения. Пик заболевания приходится на 2 года. Почти все случаи заболевания выявляются до 5-летнего возраста. Распространенность ретинобластомы небольшая – примерно 1 случай на 20 000 новорожденных.
односторонняя спорадическая форма
двусторонняя семейная форма
Слайд 47
Регуляция экспрессии гена белком RB1
Слайд 48
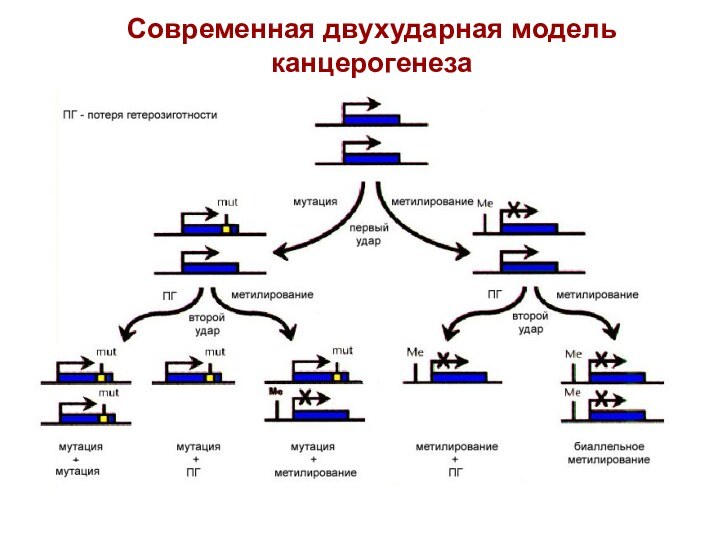
Современная двухударная модель канцерогенеза
Слайд 50
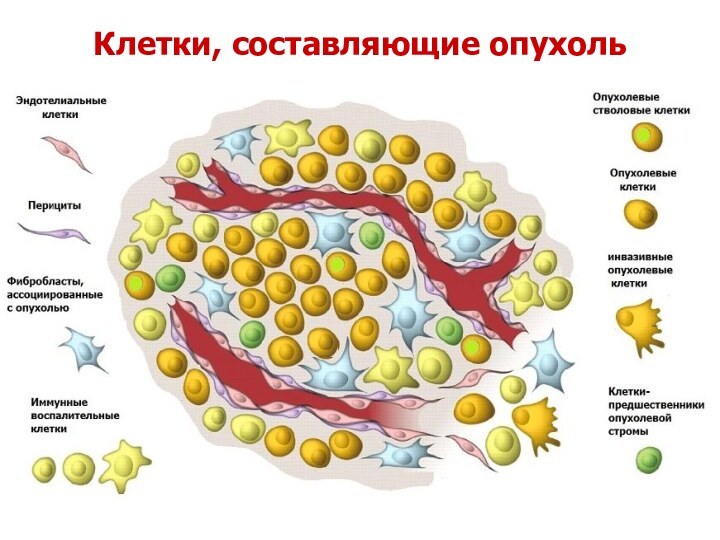
Строма опухоли
Второй важный структурный компонент опухоли — ее строма.
Строма в опухоли, так же как и строма в
нормальной ткани, в основном выполняет трофическую, модулирующую и опорную функции.
Стромальные элементы опухоли представлены клетками и экстрацеллюлярным матриксом соединительной ткани, сосудами и нервными окончаниями.
Экстрацеллюлярный матрикс опухолей представлен двумя структурными компонентами: базальными мембранами и интерстициальной соединительной тканью. В состав базальных мембран входят коллагены IV, VI и VII типов, гликопротеиды (ламинин, фибронектин, витронектин), протеогликаны (гепаран-сульфат и др.). Интерстициальная соединительная ткань опухоли содержит коллагены I и III типов, фибронектин, протеогликаны и гликозаминогликаны.
Слайд 51
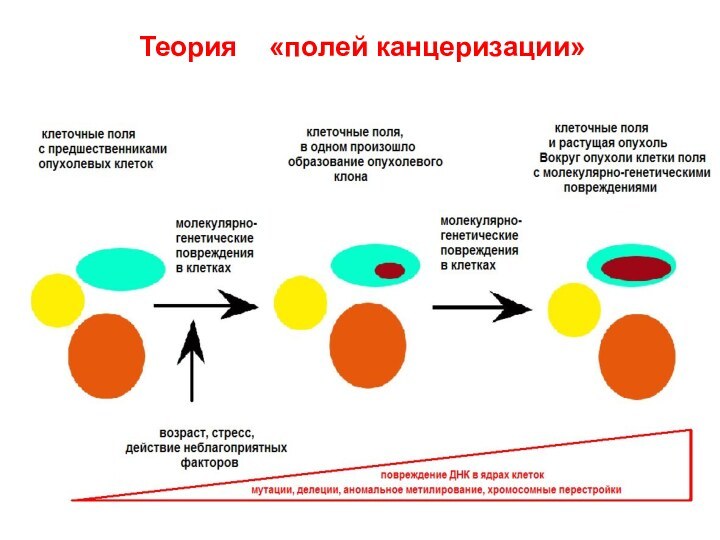
В 2000-х годах было показано, что связанное с
опухолью воспаление усиливает опухолеобразование
и прогрессию.
При воспалении в
опухолевом микроокружении происходит выработка биологически активных молекул, включая факторы роста, которые поддерживают пролиферацию.
Воспаление активирует факторы выживания, проангиогенные факторы, ферменты, модифицирующие клеточный матрикс и способствующие ангиогенезу, инвазии и метастазированию, а также индуктивные сигналы, которые активируют ЭМП.
Воспалительные клетки выделяют активные формы кислорода, которые являются сильными мутагенами для близлежащих клеток, что ускоряет их генетическую трансформацию в состояние повышенной злокачественности.