- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему к уроку Периодическая система химических элементов
Содержание
- 2. «ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ»Тема урока:
- 3. Цели урока: Сформировать представления о строении периодической системы2. Освоить на практике закономерности изменения свойств элементов.
- 4. Историческая справка Открыта 1 марта 1969 Д.
- 5. Периодическая система химических элементов Д.И.Менделеева (длиннопериодный вариант)
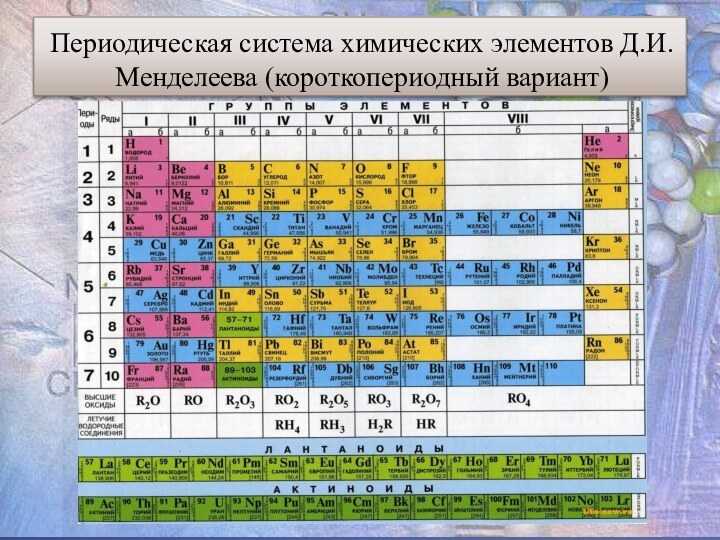
- 6. Периодическая система химических элементов Д.И.Менделеева (короткопериодный вариант)
- 8. Горизонтальные ряды , сходные по
- 9. Изменение свойств элементов в периодахR атома уменьшается;Заряд
- 10. Вертикальные ряды , сходные по
- 11. Изменение свойств элементов в группахR атома увеличивается;Заряд
- 12. Сравнить:Радиус атома:
- 13. Сравнить:Радиус атома:
- 14. Скачать презентацию
- 15. Похожие презентации
«ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ»Тема урока:










Слайд 3
Цели урока:
Сформировать представления о строении периодической системы
2.
Освоить на практике закономерности изменения свойств элементов.
Слайд 4
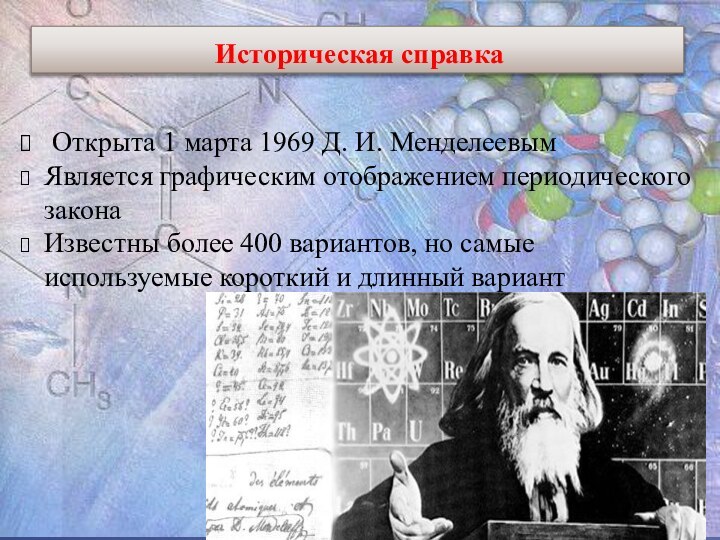
Историческая справка
Открыта 1 марта 1969 Д. И.
Менделеевым
Является графическим отображением периодического закона
Известны более 400 вариантов, но
самые используемые короткий и длинный вариантСлайд 8 Горизонтальные ряды , сходные по свойству
химических элементов, начинающиеся щелочным металлом и заканчивающиеся инертным газом
Подразделяются на малые (1,2,3,7) и большие (4,5,6)Номер периода равен числу энергетических уровней
Периоды
Слайд 9
Изменение свойств элементов в периодах
R атома уменьшается;
Заряд ядра
увеличивается;
Число энергетических уровней не изменяется;
Число электронов на внешнем уровне
увеличивается;Металлические свойства ослабевают;
Неметаллические свойства усиливаются.
Слайд 10 Вертикальные ряды , сходные по свойству
химических элементов
Подразделяются на главные и побочные
Номер
группы равен числу электронов на внешнем энергетическом уровнеГруппы
Слайд 11
Изменение свойств элементов в группах
R атома увеличивается;
Заряд ядра
увеличивается;
Число энергетических уровней увеличивается;
Число электронов на внешнем уровне не
изменяется;Металлические свойства усиливаются;
Неметаллические свойства уменьшаются.
Слайд 12
Сравнить:
Радиус атома:
Na * Mg S * O
Заряд ядра: Ca* Mg N * P
Число энергетических уровней: Na * Mg S * O
Число электронов на внешнем уровне: Ca* Mg N * P
Металлические свойства: Na * Mg S * O
Неметаллические свойства: Ca* Mg N * P
Самостоятельная работа
Слайд 13
Сравнить:
Радиус атома:
Na < Mg S < O
Заряд ядра: Ca < Mg С < F
Число энергетических уровней: Na = Mg S > O
Число электронов на внешнем уровне: Ca = Mg С < F
Металлические свойства: Na > Mg S > O
Неметаллические свойства: Ca < Mg С < F
Проверь себя:





























