- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Урок химии в 8 классе Типы химических реакций
Содержание
- 2. Цель урокаобеспечение усвоения учащимися понятия классификации химических реакций, деления их на типы.
- 3. Задачи урокаОбразовательные - развить навыки самостоятельной работы,
- 4. Химическая реакцияпревращение одного или нескольких исходных
- 6. Реакция разложенияхимические реакции, в которых из одного,
- 7. Реакции соединенияРеакции, в ходе которых из двух
- 8. Реакции замещенияхимические реакции, в которых одни функциональные
- 9. Условия протекания реакции замещенияМеталлы, стоящие левее (в
- 10. Реакции обменаЭто реакция между двумя сложными веществами,
- 11. Условия протекания реакции обмена1. Выпадение осадка2. Выделение газа
- 12. Условия протекания реакции обмена3. Образование малодиссоциирующего вещества Например, образование воды:NaOH + HCl → NaCl + H2O
- 13. РефлексияПроверь себя:
- 14. Задание 1.«Запиши уравнение»Железо + сера → _Кислород + кальций→ _Магний + хлор → _
- 15. Задание 2Реакции ______________________ - это____________________________________________________________________________________________________________2H2 + O2 →2H2O;
- 16. Задание 3Реакции _________________________- это_____________________________________________________________________________________________________________________Cu(OH)2 → CuO
- 17. Задание 4Реакции ________________ - это_______________________________________________________________________________________________________________CuCl2 +
- 18. Задание 5Реакции ________________ - это
- 19. Задание 6 Согласны ли вы что:При реакции
- 20. Скачать презентацию
- 21. Похожие презентации
Цель урокаобеспечение усвоения учащимися понятия классификации химических реакций, деления их на типы.




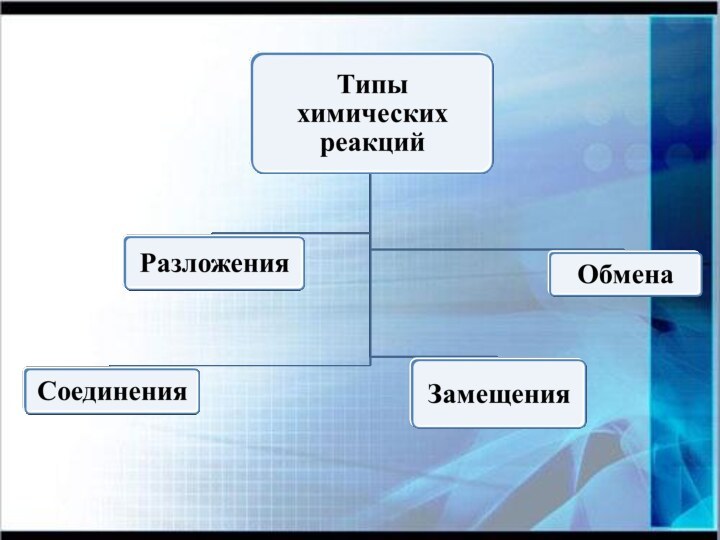















Слайд 2
Цель урока
обеспечение усвоения учащимися понятия классификации химических реакций,
деления их на типы.
Слайд 3
Задачи урока
Образовательные - развить навыки самостоятельной работы, умения
записывать уравнения реакций и расставлять коэффициенты, указывать типы реакций,
делать выводы и обобщения.Развивающие - развить речевые навыки, способности к анализу; развитие познавательных способностей, мышления, внимания, умения использовать изученный материал для познания нового.
Воспитательные - воспитание самостоятельности, сотрудничества, нравственных качеств - коллективизма, способности к взаимовыручке, адекватной самооценке.
Слайд 4
Химическая реакция
превращение одного или нескольких исходных веществ
(реагентов) в отличающиеся от них по химическому составу или
строению вещества (продукты реакции) –химические соединения
(демонстрация опыта
«Вулкан».
Слайд 6
Реакция разложения
химические реакции, в которых из одного, более
сложного вещества образуются два или более других, более простых
веществАВ→ А+В Н2О→ Н2 + О2
АВС→ АС + ВС СаСО3→ СаО + СО2
Слайд 7
Реакции соединения
Реакции, в ходе которых из двух или
нескольких веществ образуется одно вещество более сложного состава. (обратная
реакция разложения)2Са + О2→ 2СаО А+ В→ АВ
SO3 + H2O→ H2SO4 ВС + АС→ АВС
Слайд 8
Реакции замещения
химические реакции, в которых одни функциональные группы,
входящие в состав химического соединения, меняются на другие группы.
А
+ ВС→ АС + ВZn + 2HCl → ZnCl2 + H2
Слайд 9
Условия протекания реакции замещения
Металлы, стоящие левее (в ряде
напряженности металлов), являются более
сильными восстановителями, чем металлы, расположенные правее:
они вытесняют последние из растворов солей
Слайд 10
Реакции обмена
Это реакция между двумя сложными веществами, которые
обмениваются своими составными частями
АВ + СД →АД + ВС
2
NaOH + CuCl2→ 2NaCl + Cu(OH)2
Слайд 12
Условия протекания реакции обмена
3. Образование малодиссоциирующего вещества
Например,
образование воды:
NaOH + HCl → NaCl + H2O
Слайд 15
Задание 2
Реакции ______________________ - это____________________________________________________________________________________________________________
2H2 + O2 →2H2O;
4P + 5O2 →2P2O5;
Na2O + SO3 → Na2SO4;
Слайд 16
Задание 3
Реакции _________________________- это_____________________________________________________________________________________________________________________
Cu(OH)2 → CuO +H2 O
2HgO → 2Hg + O2
CaCO3 → CaO + CO2
Слайд 17
Задание 4
Реакции ________________ - это_______________________________________________________________________________________________________________
CuCl2 + Fe
→ Cu + FeCl2
Cr2 O3 + 2Al → 2Cr + Al2 O3
Zn
+ 2HCl → ZnCl2 + H2
Слайд 18
Задание 5
Реакции ________________ - это _________________________________________________________________________________________________________________
CuO
+ 2HCl → CuCl2 + H2 О
BaCl2 + K2 SO4 → BaSO4 ↓+ 2KCl
FeCl3
+ 3 NaOH → 3NaCl + Fe(OH)3↓Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O
Слайд 19
Задание 6
Согласны ли вы что:
При реакции обмена
участвуют два сложных вещества…
При реакции соединения образуется два вещества…
При
реакции замещения образуется одно вещество…При реакции обмена образуются два сложных вещества…





























