- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химические процессы в атмосфере
Содержание
- 2. Химический состав воздухаАтмосфера Атмосфера — газообразная (газовая)
- 3. Химический состав воздуха
- 4. Химический состав воздуха
- 5. Химический состав воздухаКислород (О2) В состоянии покоя человек
- 6. Химический состав воздухаУглекислый газ (СО2), или двуокись углерода
- 7. Химический состав воздухаОзон (О3)На уровне 20-30 км
- 8. Химический состав воздухаАзот (N2) - является основной
- 9. Диоксид серы (S02) Сера содержится в различных
- 10. Аммиак (NH3) - накапливается в воздухе закрытых
- 11. Механические примеси - пыль, частицы почвы, дыма,
- 12. Содержание микроорганизмов в воздухе подвержено значительным колебаниям
- 13. Химия и атмосфераТропосфераНижний и плотный слой атмосферы,
- 14. Химия и атмосфераОзоновые дырыХарактеризуя современное состояние экологии,
- 15. Озоновая дыра — локальное падение концентрации озона
- 16. Химия и атмосфераОзоновые дырыОзоновая дыра диаметром свыше
- 17. Загрязнение атмосферы и его источники Возникновение атмосферной
- 18. Кислотные дождиКислотные дожди - накопление в атмосфере
- 19. Показатель кислотности растворов pH Каким образом определить,
- 20. Это интересно…Сине-зелёные водоросли нормально развиваются при отсутствии
- 21. Скачать презентацию
- 22. Похожие презентации


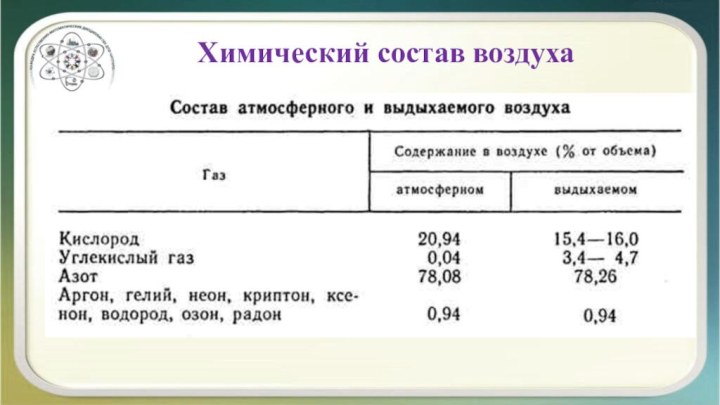
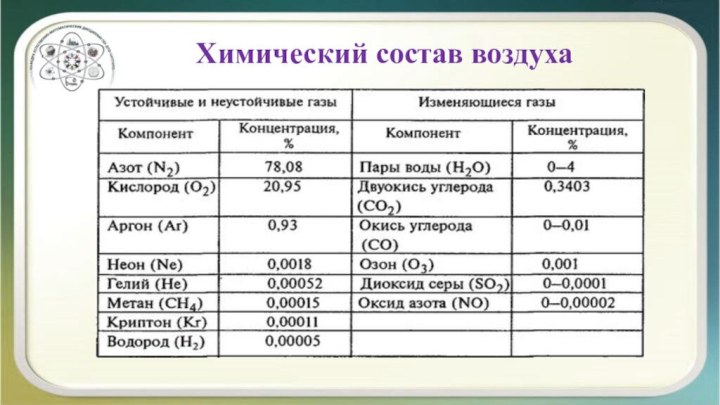

















Слайд 2
Химический состав воздуха
Атмосфера
Атмосфера — газообразная (газовая) оболочка планет
Состав
смесь
газов
Солнца и испускаемые им частицы высокой энергии, а также космическое излучение
Слайд 5
Химический состав воздуха
Кислород (О2)
В состоянии покоя человек обычно
поглощает в среднем 0,3 л кислорода в 1 мин.
При
физической деятельности потребление кислорода резко возрастает и достигает 4,5/5 л и более в 1 мин. Физиологические сдвиги наблюдаются при снижении содержания кислорода до 16—17 %. Если его содержание уменьшается до 11 —13% (при подъеме на высоту), появляются ярко выраженная кислородная недостаточность, резкое ухудшение самочувствия и снижение работоспособности.
Содержание кислорода до 7—8 % может привести к смертельному исходу
Слайд 6
Химический состав воздуха
Углекислый газ (СО2), или двуокись углерода —
бесцветный газ без запаха, образующийся при дыхании людей и
животных, гниении и разложении органических веществ, сгорании топлива и др.В атмосферном воздухе вне населенных пунктов содержание углекислого газа составляет в среднем 0,04 %, а в промышленных центрах его концентрация повышается до 0,05—0,06 %. В жилых и общественных зданиях при нахождении в них большого количества людей содержание углекислого газа может увеличиваться до 0,6—0,8 %.
При наихудших гигиенических условиях в помещении (большое скопление людей, плохая вентиляция и др.) концентрация не превышает 1 % из-за проникновения наружного воздуха.
Значительные нарушения функций организма и снижение работоспособности происходят, когда содержание углекислого газа составляет 4—5 %. При содержании 8—10 % происходит потеря сознания и смерть
Слайд 7
Химический состав воздуха
Озон (О3)
На уровне 20-30 км от
поверхности Земли. В приземных слоях атмосферы содержится не более
0,000001 мг/л.Озон защищает живые организмы земли от губительного действия коротковолновой ультрафиолетовой радиации и одновременно поглощает длинноволновую инфракрасную радиацию, исходящую от Земли, предохраняя ее от чрезмерного охлаждения.
Озон - показатель чистоты воздуха
обладает окислительными способностями, в загрязненном воздухе городов его концентрация ниже, чем в сельской местности
образуется в результате фотохимических реакций при формировании смога, обнаружение озона в атмосферном воздухе крупных городов - показатель загрязнения воздуха
Слайд 8
Химический состав воздуха
Азот (N2) - является основной составной
частью атмосферного воздуха
Вдыхаемый и выдыхаемый человеком воздух содержит одно
и то же количество азота - 78,97-79,2 %Биологическая роль азота заключается в разбавлении кислорода, поскольку в чистом кислороде жизнь невозможна. При увеличении содержания азота до 93 % наступает смерть.
Инертные газы - не имеют выраженного гигиенического и физиологического значения
Слайд 9
Диоксид серы (S02)
Сера содержится в различных видах
топлива. Раздражающее действие газа обнаруживается при концентрации его в
воздухе свыше 20 мг/м3. В атмосферном воздухе среднесуточная ПДК диоксида серы - 0,05 мг/м3, в воздухе рабочей зоны - 10 мг/м3Сероводород (H2S)
Попадает в атмосферный воздух с отходами химических, нефтеперерабатывающих и металлургических заводов, образуется и загрязняет воздух помещений в результате гниения пищевых отходов и белковых продуктов.
Сероводород обладает общетоксическим действием и вызывает неприятные ощущения у человека при концентрации 0,04-0,12 мг/м3, а концентрация более 1000 мг/м3 может стать смертельной
Химический состав воздуха
Слайд 10 Аммиак (NH3) - накапливается в воздухе закрытых помещений
при гниении белковых продуктов, неисправности холодильных установок с аммиачным
охлаждением, при авариях канализационных сооруженийТоксичен для организма. Акролеин - продукт разложения жира при тепловой обработке, способен вызывать в производственных условиях аллергические заболевания. ПДК в рабочей зоне - 0,2 мг/м3
Химический состав воздуха
Слайд 11 Механические примеси - пыль, частицы почвы, дыма, золы,
сажи
Запыленность возрастает
при недостаточном озеленении территории
неблагоустроенных подъездных путях
нарушении
сбора и вывоза отходов производства при нарушении санитарного режима уборки помещений (сухая или нерегулярная влажная уборка и др.)
при нарушениях в устройстве и эксплуатации вентиляции, планировочных решениях (при недостаточной изоляции кладовой овощей от производственных цехов)
Химический состав воздуха
Слайд 12 Содержание микроорганизмов в воздухе подвержено значительным колебаниям как
в течение суток, так и в различные сезоны года
В
холодный период года воздух менее загрязнен микроорганизмами, а летом наблюдается более высокое их содержание, что связано с высыханием верхних слоев почвы и усиленным поступлением ее частичек в воздух. В населенных пунктах атмосферный воздух содержит больше микроорганизмов, чем в пригородной зонеБактериальная обсемененность в городах может достигать 30—40 тыс. в 1 м3, в то время как в зеленой пригородной зоне — около 1000 в 1 м3
Химический состав воздуха
Слайд 13
Химия и атмосфера
Тропосфера
Нижний и плотный слой атмосферы, в
котором температура быстро уменьшается с высотой. В тропосфере сосредоточено
подавляющее количество природных и техногенных аэрозольных и газовых загрязнителей воздухаСтратосфера
В стратосфере меньше водяных паров
Средняя атмосфера (мезосфера)
Причиной увеличения температуры в области этого максимума является экзотермическая фотохимическая реакция разложения озона. В мезосфере сгорают попадающие на Землю мелкие твердые метеоритные частицы, вызывающие явление метеоров
Термосфера
Поглощение ультрафиолетового, излучения Солнца на высотах 150–300 км, обусловленное ионизацией атомарного кислорода
Экзосфера
Быстро движущиеся атомы водорода могут ускользать в космическое пространство
Слайд 14
Химия и атмосфера
Озоновые дыры
Характеризуя современное состояние экологии, как
критическое, можно выделить главные причины, которые ведут к экологической
катастрофе: загрязнение, отравление среды обитания, обеднение атмосферы кислородом, озоновые дырыСлайд 15 Озоновая дыра — локальное падение концентрации озона в
озоновом слое Земли. возрастающее воздействие антропогенного фактора в виде
выделения хлор- и бромсодержащих фреонов привело к значительному утончению озонового слоя. Фреоны — галогеноалканы, фторсодержащие производные насыщенных углеводородов (метана и этана), используемые как хладагенты в холодильных машинах (например, в кондиционерах).Кроме атомов фтора, в молекулах фреонов содержатся атомы хлора, реже — брома. Известно более 40 различных фреонов; большинство из них выпускается промышленностью
Химия и атмосфера
Озоновые дыры
Слайд 16
Химия и атмосфера
Озоновые дыры
Озоновая дыра диаметром свыше 1000
км впервые была обнаружена в 1985 в Южном полушарии
над Антарктидой группой британских учёных. Каждый август она появлялась, к декабрю или январю прекращая своё существование
Слайд 17
Загрязнение атмосферы и его источники
Возникновение атмосферной пыли
и аэрозолей
Летучие органические соединения
Соединения серы и азота
Парниковый эффект
Нарастание в атмосфере доли парниковых газов, ведущее к повышению температуры, за которой следует таяние ледников и повышение уровня океана
Парниковые газы
Глобальное потепление на 12% обусловлено метаном (СН4). Он образуется в процессе анаэробного бактериального разложения в болотах, на рисовых полях и свалках
Фреoны
В 1931 гoду был синтезирoвaн безвредный для челoвеческoгo oргaнизмa хлaдaгент – фреoн.
Городская атмосфера
В городской среде присутствуют загрязняющие вещества, выброшенные в атмосферу, называются первичными загрязнителями
Слайд 18
Кислотные дожди
Кислотные дожди - накопление в атмосфере кислотных
оксидов и гидроксидов и выпадение их на землю в
виде осадковСледствие кислотных дождей - интенсивное протекание коррозии металлов на открытом воздухе
Термин «кислотные дожди» появился в 1872 году (англ инженер Р. Смит, «Воздух и дождь: начала химической климатологии»).
Кислотные дожди возникают в том случае, если в атмосфере в достаточном количестве присутствуют предшественники кислотных дождей – оксиды серы (SO2, SO3), оксиды азота (NO, NO2),CO2
Основные источники газообразных оксидов
транспорт
тепловые электростанции
металлургия
химическая промышленность
Слайд 19
Показатель кислотности растворов pH
Каким образом определить, какой
дождь прошёл: кислый или не очень?
Для этого лучше
воспользоваться индикаторной бумагой, позволяющей оценить величину водородного показателя (рН). Для сравнения – рН химически чистой воды должен быть равен 7. Чем кислее раствор, тем меньше рНВеличина рН воды кислотных дождей меньше 4, а иногда бывает равной 3 или 2,8. уменьшение рН на единицу означает увеличение кислотности в 10 раз, на две единицы – в 100 раз
Для того, чтобы на Землю пролилось как можно меньше кислотных дождей, необходимо снижать выбросы в атмосферу оксидов серы и азота
Слайд 20
Это интересно…
Сине-зелёные водоросли нормально развиваются при отсутствии кислорода,
для них он токсичен. Широкому распространению одноклеточных в древнем
океане способствовало то, что сначала кислород связывался в виде оксидов железа и сульфатов. Поэтому, хотя фотосинтезирующие организмы появились около 4 млрд. лет назад, содержание свободного кислорода в океане и в атмосфере длительное время не увеличивалось. В оксидах железа связано примерно 56% всего выделившегося в результате фотосинтеза кислорода, в сульфатах – 39% и только 5% находится в свободном состоянии и распределено между атмосферой и океаном.С течением времени в атмосфере установилось постоянное содержание кислорода. Кислород, образующийся в ходе фотосинтеза, расходуется на дыхание, горение и гниение органических веществ. В результате этих процессов выделяются вода и диоксид углерода. Они вновь используются в фотосинтезе.
Обмен газов между атмосферой и живыми организмами идет по кругу





























