- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Газообразное состояние вещества
Содержание
- 2. Цели урока:Рассмотреть особенности газообразных веществ.Выделить важнейшие природные
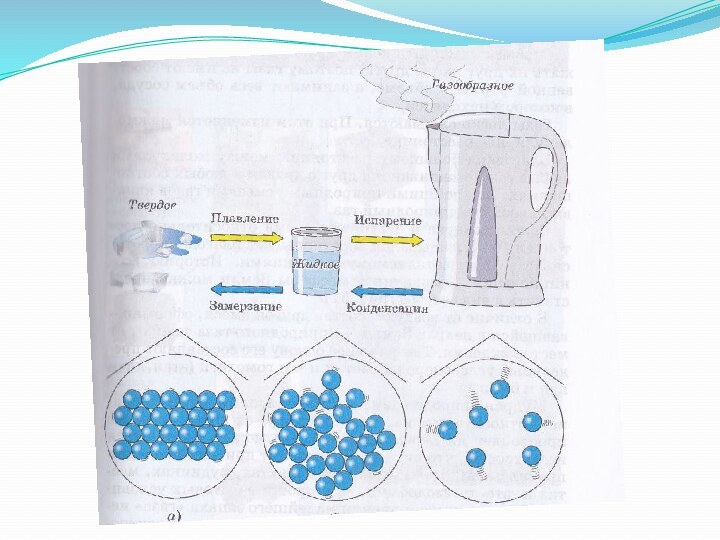
- 3. Агрегатные состояния веществаГазообразноеЖидкоеТвёрдое.
- 5. В газовой
- 6. Закон Авогадро В равных
- 7. Следствие При одинаковых условиях 1 моль любого
- 8. Задания Какой объём займут 2 моль углекислого
- 9. Для газов можно вычислять плотность:ρ = М
- 10. ЗаданияОпределите плотность при н.у. и относительную плотность по воздуху углекислого газа.Определите относительную плотность сероводорода по водороду.
- 11. Выберите один правильный ответ:0,5 моль кислорода займут
- 12. 4,48 л занимает водород количеством вещества1. 1моль
- 13. Относительная плотность оксида серы (IV) по водороду равна1. 32 2. 64 3. 28 4. 24
- 14. 18 * 1023 молекул оксида серы (IV)
- 15. 136 г сероводорода займут объём равный 1. 22,4 л2. 44,8 л3. 89,6 л 4. 44,8 м3
- 16. 34 г аммиака займут объём равный 1.
- 17. Относительная плотность углекислого газа по водороду равна1. 442. 223. 884. 66
- 18. Относительная плотность метана по кислороду равна1. 1 2. 0,53. 24. 4
- 19. 4,48 л занимает аммиак массой равной1. 34г 2. 3,4 г 3. 17 г4. 64г
- 20. Относительная плотность оксида серы (VI) по водороду
- 21. Особенности газовЛегко сжимаются.Не имеют собственной формы и объёма.Любые газы смешиваются друг с другом в любых соотношениях.
- 22. Важнейшие природные смеси газовВоздух (φ (N2) =78%,
- 23. Глобальные экологические проблемы атмосферыПарниковый эффект.Озоновые дыры.Кислотные дожди.
- 24. Задание: заполнить таблицу по
- 25. Скачать презентацию
- 26. Похожие презентации
Цели урока:Рассмотреть особенности газообразных веществ.Выделить важнейшие природные смеси газов.Обозначить основные экологические проблемы атмосферы.Систематизировать знания об изученных газах.























Слайд 2
Цели урока:
Рассмотреть особенности газообразных веществ.
Выделить важнейшие природные смеси
газов.
Слайд 5 В газовой фазе
расстояния между атомами или молекулами во много раз превышает
размеры самих молекул.
Слайд 6
Закон Авогадро
В равных объёмах
различных газов при одинаковых условиях содержится одинаковое число молекул.
Слайд 7
Следствие
При одинаковых условиях 1 моль любого газа
занимает одинаковый объём, который называется молярным
1 моль
любого газа при н.у. (760 мм рт. ст. и 00C) занимает объём 22,4 л.Vm = 22,4 л/моль – молярный объём газов
1 моль любого вещества занимает определённый объём, который вычисляется как частное при делении молярной массы на плотность вещества.
Молярный объём обозначается Vm =М / ρ
Слайд 8
Задания
Какой объём займут 2 моль углекислого газа
при н.у.?
Определите массу и объём 18 * 1023 молекул
сероводорода.№ 3, 4 стр. 79
Слайд 9
Для газов можно вычислять плотность:
ρ = М /
Vm (г/л);
относительная плотность показывает во сколько раз один
газ тяжелее другогоОтносительная плотность газа – это отношение молярной массы одного газа к молярной массе другого. DГ2(Г1) = М(Г1) / М(Г2) это безразмерная величина.
Отсюда М(Г1) = М(Г2) * DГ2(Г1)
Для определения относительной плотности газа по воздуху необходимо помнить, что М(возд) = 29 г/моль
Слайд 10
Задания
Определите плотность при н.у. и относительную плотность по
воздуху углекислого газа.
Определите относительную плотность сероводорода по водороду.
Слайд 11
Выберите один правильный ответ:
0,5 моль кислорода займут объём
равный?
1. 112 л
2. 22,4 л
3.11,2 л
4.
11,2 м3Слайд 14 18 * 1023 молекул оксида серы (IV) займут
объём равный
1. 67,2 л
2. 22,4 л
3. 672 л
4. 6,72 м3Слайд 20 Относительная плотность оксида серы (VI) по водороду 40,
его молярная масса равна
1. 64
2. 1203. 80
4. 40
Слайд 21
Особенности газов
Легко сжимаются.
Не имеют собственной формы и объёма.
Любые
газы смешиваются друг с другом в любых соотношениях.
Слайд 22
Важнейшие природные смеси газов
Воздух (φ (N2) =78%, φ
(O2) =21%, φ (CO2) =0,03%, ).
Природный газ (смесь углеводородов).
Слайд 23
Глобальные экологические проблемы атмосферы
Парниковый эффект.
Озоновые дыры.
Кислотные дожди.
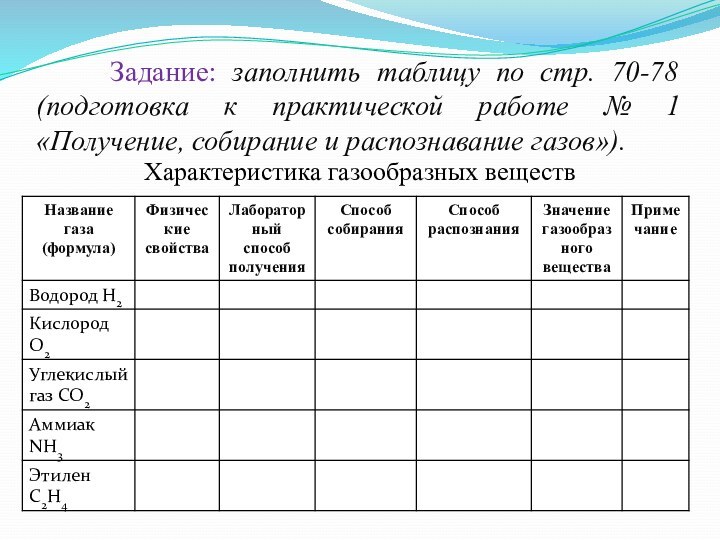
Слайд 24 Задание: заполнить таблицу по стр.
70-78 (подготовка к практической работе № 1 «Получение, собирание
и распознавание газов»).Характеристика газообразных веществ