- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Аминокислоты и белки
Содержание
- 2. БелкиБолее 4 млрд. лет назад на Земле
- 3. БелкиВпервые белок был выделен (в виде клейковины)
- 4. БелкиБелки, или протеины (от греч. “протос” —
- 5. БелкиС помощью белков мы перевариваем пищу и
- 6. БелкиБелковых молекул в живой клетке во много
- 7. Биологические «бусы»Молекула белка очень длинная. Химики называют
- 8. Биологические «бусы»Секрет белков спрятан в особенностях этих
- 9. Биологические «бусы»Нечто подобное происходит и в белках.
- 10. БелкиПри длительном кипячении белков в присутствии сильных
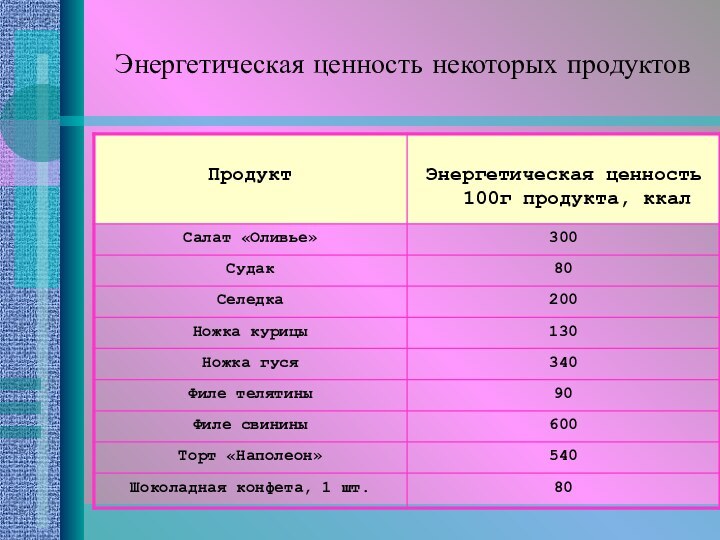
- 11. Энергетическая ценность некоторых продуктов
- 12. Устройство аминокислотыВ каждой молекуле аминокислоты есть атом
- 13. АминокислотыДля нормальной жизнедеятельности организм нуждается в полном
- 14. АминокислотыДля удобства 20 главных аминокислот обозначают символами,
- 15. Скачать презентацию
- 16. Похожие презентации
БелкиБолее 4 млрд. лет назад на Земле из маленьких неорганических молекул непостижимым образом возникли белки, ставшие строительными блоками живых организмов. Своим бесконечным разнообразием всё живое обязано именно уникальным молекулам белка, и иные формы жизни во Вселенной











Слайд 3
Белки
Впервые белок был выделен (в виде клейковины) в
1728 г. итальянцем Якопо
Бартоломео Беккари (1682— 1766) из пшеничной
муки. Это событие принято считать рождением химии белка. С тех пор почти за три столетия из природных источников получены тысячи различных белков и исследованы их свойства.
Слайд 4
Белки
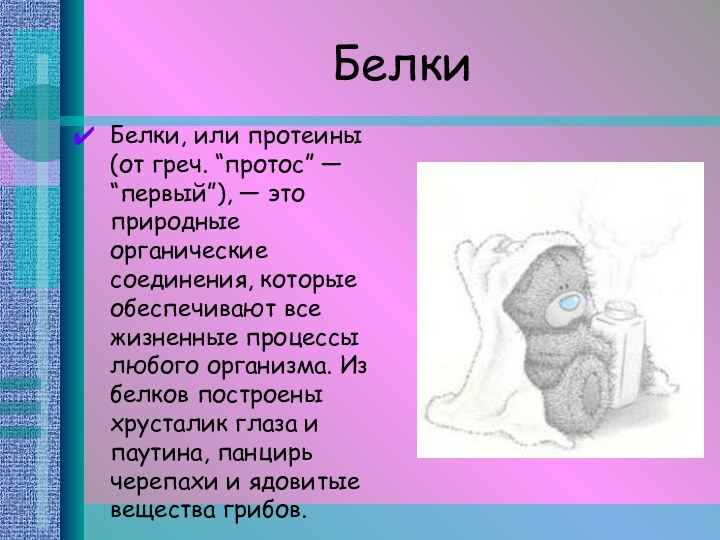
Белки, или протеины (от греч. “протос” — “первый”),
— это природные органические соединения, которые обеспечивают все жизненные
процессы любого организма. Из белков построены хрусталик глаза и паутина, панцирь черепахи и ядовитые вещества грибов.
Слайд 5
Белки
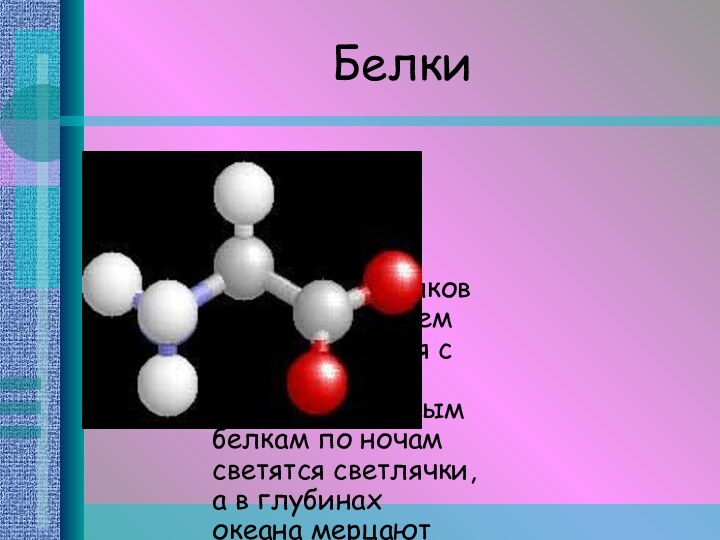
С помощью белков мы перевариваем пищу и боремся
с болезнями. Благодаря особым белкам по ночам светятся светлячки,
а в глубинах океана мерцают таинственным светом медузы.
Слайд 6
Белки
Белковых молекул в живой клетке во много раз
больше, чем всех других
(кроме воды, разумеется). Учёные выяснили, что
у большинства организмов белки составляют более половины их сухой массы. И разнообразие видов белков очень велико — в одной клетке такого маленького организма, как бактерияEscherichia сой', насчитывается около 3 тыс.. различных белков.
Слайд 7
Биологические «бусы»
Молекула белка очень длинная. Химики называют такие
молекулы полимерными
(от греч. “поли” — “много” и “мерос” —
“часть”, “доля”). Действительно, длинная молекула полимера состоит из множества маленьких молекул, связанных друг с другом. Так нанизываются на нить бусинки в ожерелье. В полимерах роль нити играют химические связи между бусинками-молекулами.
Слайд 8
Биологические «бусы»
Секрет белков спрятан в особенностях этих самых
бусинок. Большинство полимеров не принимает устойчивой формы в пространстве,
уподобляясь тем же бусам, у которых и не может быть пространственной структуры: повесишь их на шею — они примут форму кольца или овала, положишь в коробку — свернутся в клубок неопределённой формы. А теперь представим себе, что некоторые бусинки могут “слипаться” друг с другом. Например, красные притягиваются к жёлтым. Тогда вся цепочка примет определённую форму, обязанную своим существованием “слипанию” жёлтых и красных бусинок
Слайд 9
Биологические «бусы»
Нечто подобное происходит и в белках. Отдельные
маленькие молекулы, входящие в состав белка, обладают способностью “слипаться”,
так как между ними действуют силы притяжения. В результате у любой белковой цепи есть характерная только для неё пространственная структура. Именно она определяет чудесные свойства белков. Без такой структуры они не могли бы выполнять те функции, которые осуществляют в живой клетке.
Слайд 10
Белки
При длительном кипячении белков в присутствии сильных кислот
или щелочей белковые цепи распадаются на составляющие их молекулы,
называемые аминокислотами. Аминокислоты — это и есть те “бусинки”, из которых состоит белок, и устроены они сравнительно просто.
Слайд 12
Устройство аминокислоты
В каждой молекуле аминокислоты есть атом углерода,
связанный с четырьмя заместителями. Один из них — атом
водорода, второй — карбоксильная группа—СООН. Она легко “отпускает на волю” ион водорода Н+, благодаря чему в названии аминокислот и присутствует слово “кислота”. Третий заместитель — аминогруппа —NH2 и, наконец, четвёртый заместитель — группа атомов, которую в общем случае обозначают R. Свойства “бусинок”, отличающие одну аминокислоту от другой, скрыты в
R- группах (их ещё называют боковыми цепями). Что же касается группы —СООН, то всем другим атомам углерода в молекуле даются обозначения в зависимости от степени их удалённости от карбоксильной группы. Ближайший к ней атом именуют а-атомом, второй — в-атомом, следующий — у-атомом.
Слайд 13
Аминокислоты
Для нормальной жизнедеятельности организм нуждается в полном наборе
из 20 основных a-Z-аминокислот. Но одни из них могут
быть синтезированы в клетках самого организма, а другие — должны поступать в готовом виде из пищевых продуктов. В первом случае аминокислоты называют заменимыми, а во втором — незаменимыми. Набор последних для разных организмов различен. Например, для белой крысы незаменимыми являются 10 аминокислот, а для молочнокислых бактерий — 16. Растения могут самостоятельно синтезировать самые разнообразные аминокислоты, создавать такие, которые не встречаются в белках.
Слайд 14
Аминокислоты
Для удобства 20 главных аминокислот обозначают символами, используя
одну или первые три буквы русского или английского названия
аминокислоты, например аланин — Ала или А, глицин — Гли или G.Аланин