- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Белки, ферменты
Содержание
- 2. Структурные единицы белков – аминокислоты Классификация аминокислотНеполярные (гидрофобные)Полярные (гидрофильные)Ароматические(главным образом неполярные)Отрицательно заряженныеПоложительно заряженные
- 3. Первичная структура белка
- 4. Установление первичной структуры
- 5. Вторичная структура белкаα-спиральβ-складчатый слой
- 6. Третичная структура белка
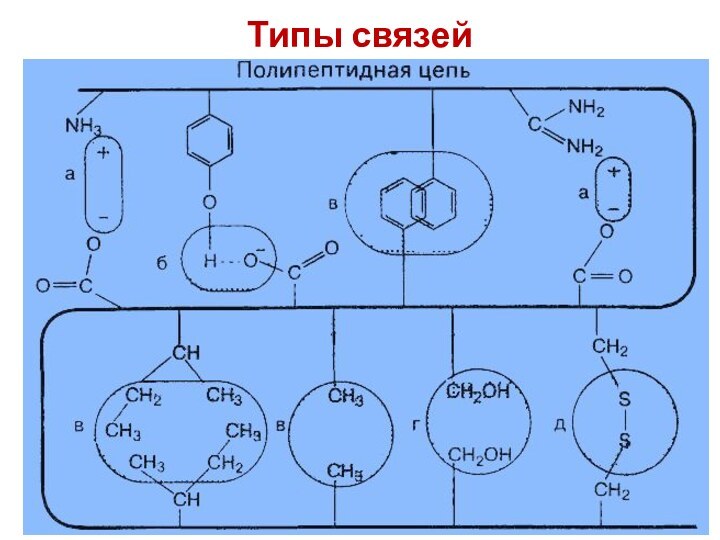
- 7. Типы связей
- 8. Участие шаперонов в фолдинге белков
- 9. Глобулярные домены в g-кристаллине (белке хрусталика глаза)
- 10. Четвертичная структура гемоглобина
- 11. I, II, III и IV – комплексыдыхательной цепи митохондрийПятый уровень структурной организации - метаболон
- 12. Классификация белков
- 13. Аномальные гемоглобины
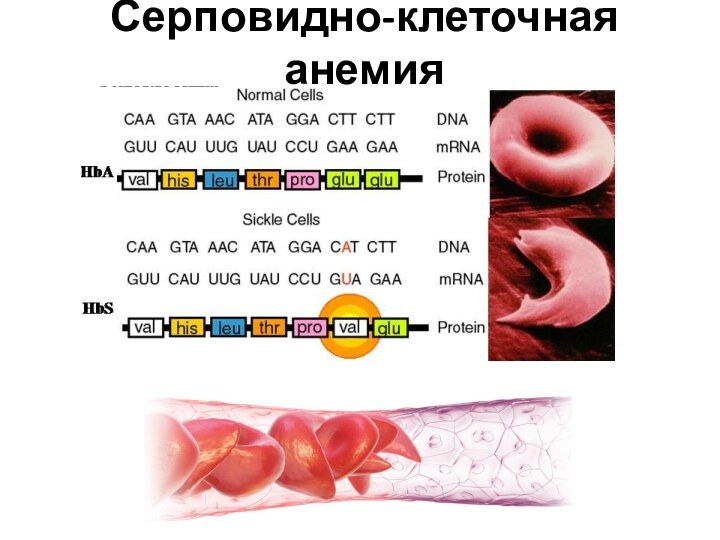
- 14. Серповидно-клеточная анемия
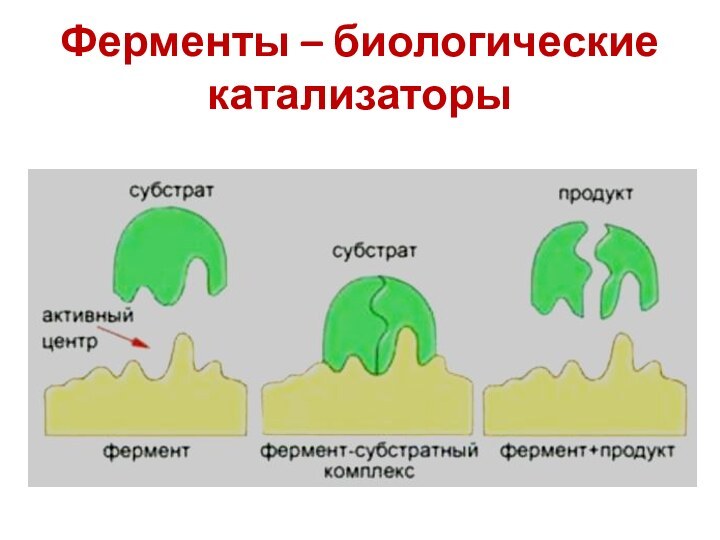
- 15. Ферменты – биологические катализаторы
- 16. Классификация ферментов1. Оксидоредуктазы2. Трансферазы3. Гидролазы4. Лиазы5. Изомеразы6. Лигазы
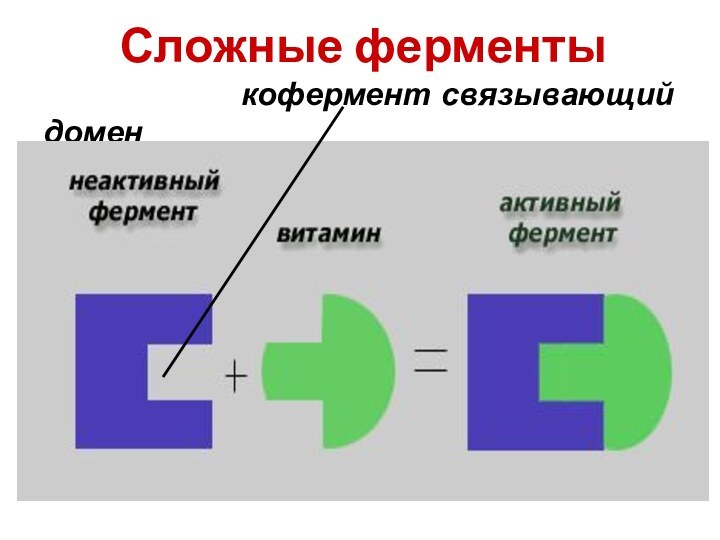
- 17. кофермент связывающий доменСложные ферменты
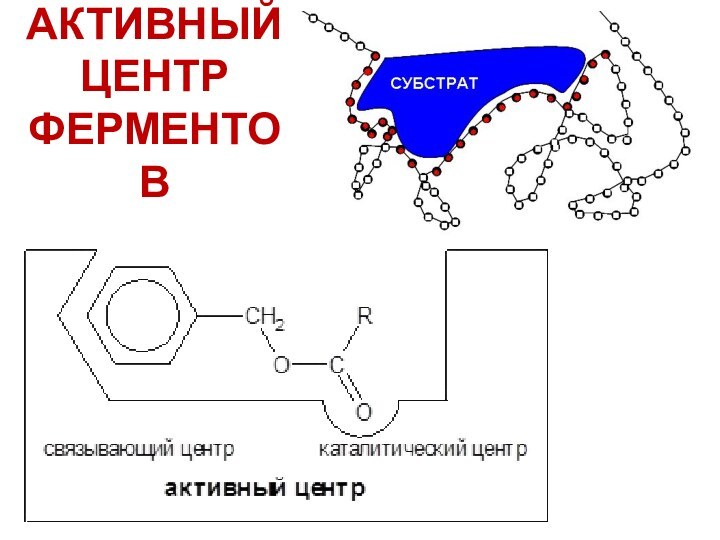
- 19. АКТИВНЫЙ ЦЕНТР ФЕРМЕНТОВ
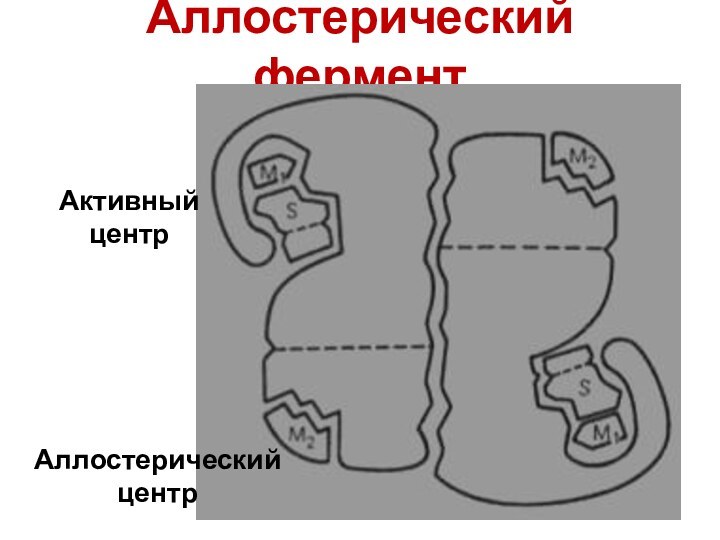
- 20. Аллостерический ферментАктивный центрАллостерический центр
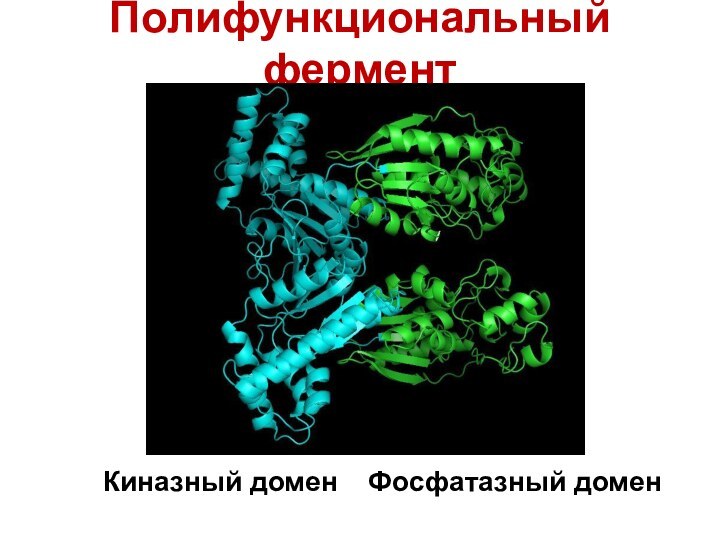
- 21. Полифункциональный ферментКиназный домен Фосфатазный домен
- 22. Дыхательная цепь митохондрийМУЛЬТИМОЛЕКУЛЯРНЫЕ ФЕРМЕНТНЫЕ СИСТЕМЫ
- 23. Изоферментылактатпируват
- 24. Теории ферментативного катализа Герман Эмиль Фишер (1852 – 1919)
- 25. Теория «ключ - замок» ФишераE + S → E-S → E + P
- 26. Дэниел Кошланд (1920 – 2007)
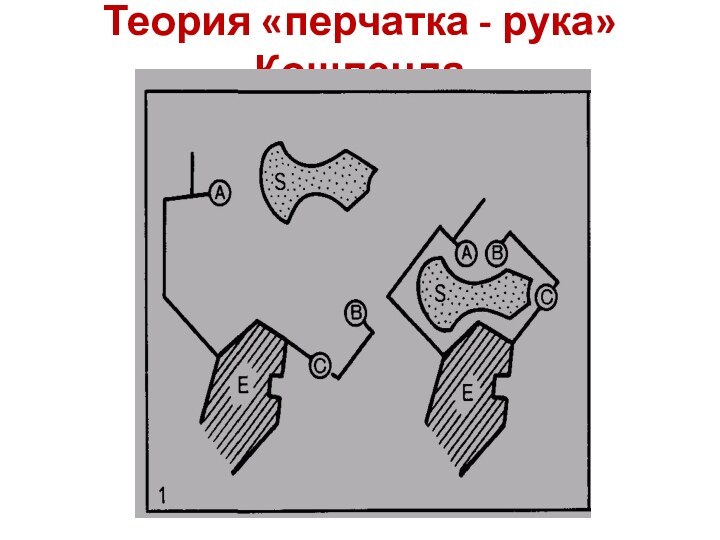
- 27. Теория «перчатка - рука» Кошленда
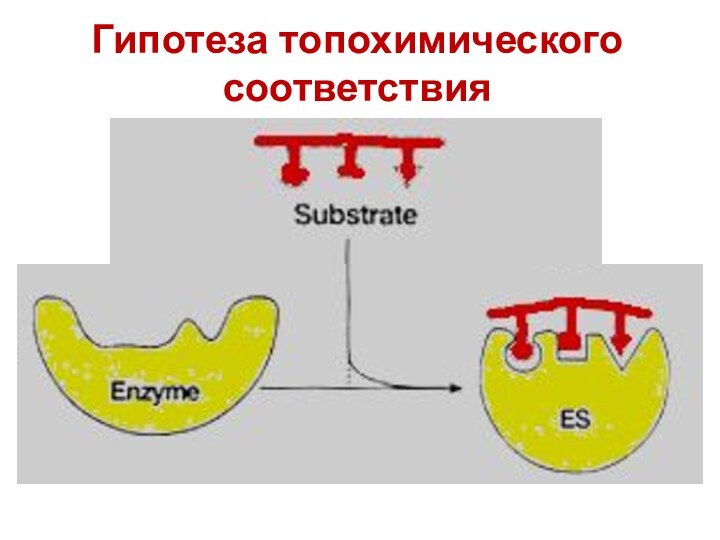
- 28. Гипотеза топохимического соответствия
- 29. Ферментативная кинетика
- 31. МИХАЭЛИС ЛеонорМЕНТЕН Мод Леонора
- 32. УравнениеМихаэлиса-МентенУравнениеБриггса-Холдейна
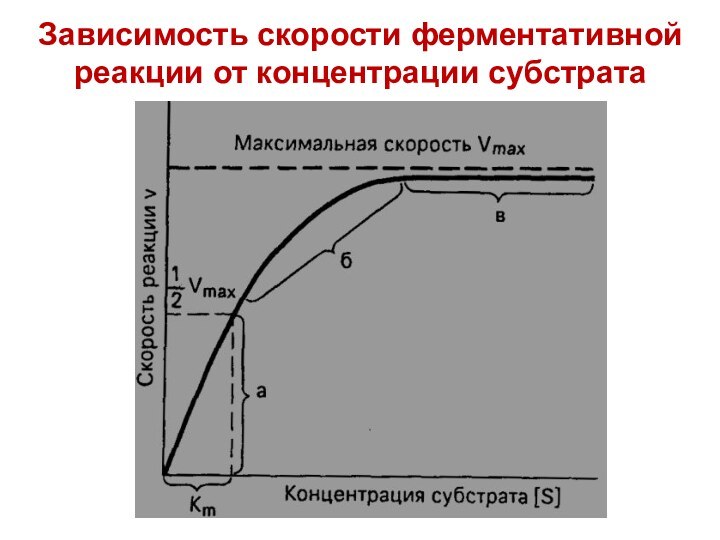
- 33. Зависимость скорости ферментативной реакции от концентрации субстрата
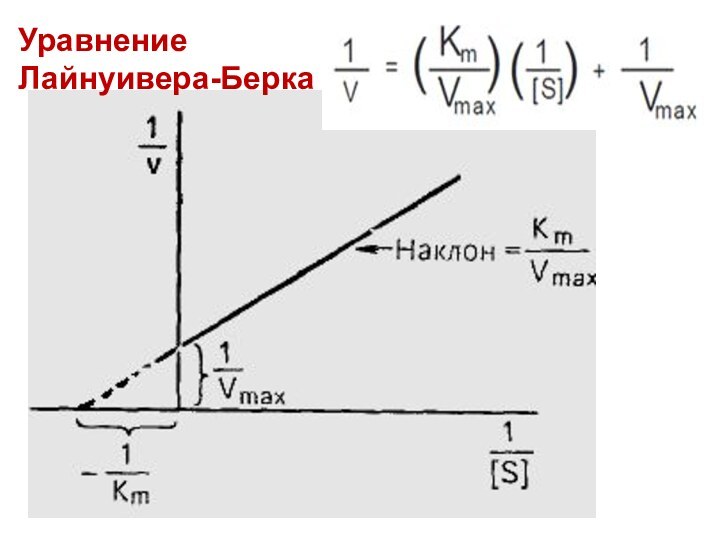
- 34. УравнениеЛайнуивера-Берка
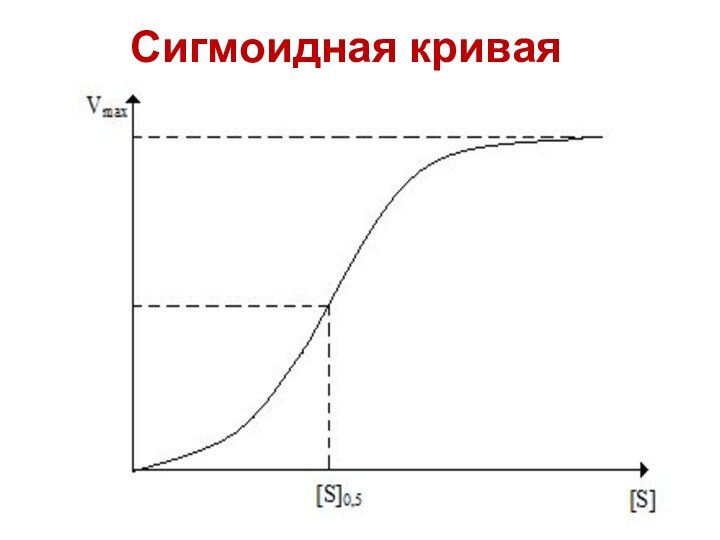
- 35. Сигмоидная кривая
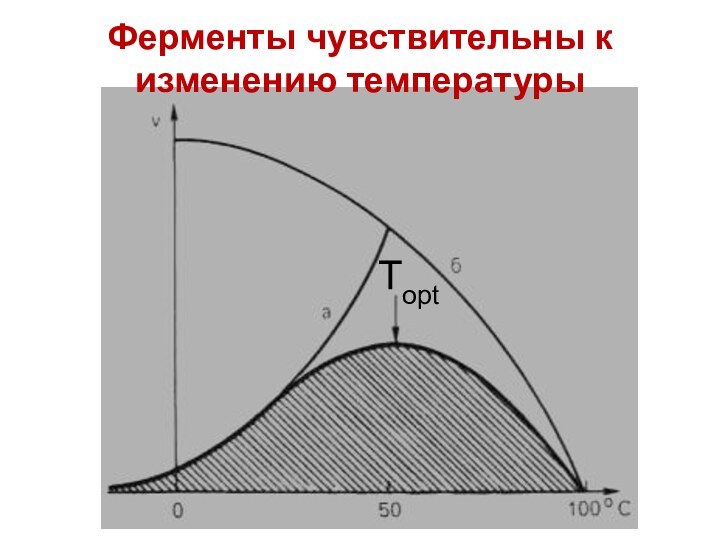
- 36. ТoptФерменты чувствительны к изменению температуры
- 37. pHoptФерменты чувствительны к изменению рН
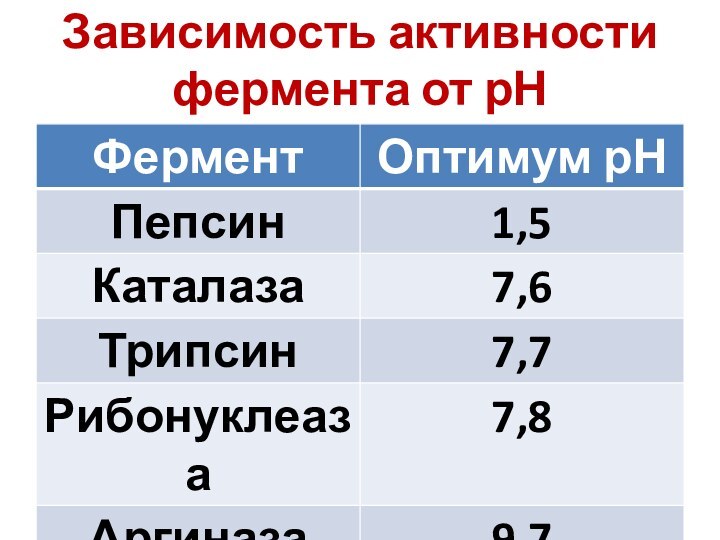
- 38. Зависимость активности фермента от рН
- 39. Ферменты специфичны (действуют только на определенный субстрат)
- 40. CO(NH2)2 + 2H2O = H2O + CO2 + 2NH3Абсолютная специфичностьУреаза
- 41. Панкреатическая липазаГрупповая (относительная) специфичность
- 42. Фумараза (малатдегидрогеназа)Стереоспецифичность
- 43. Регуляция метаболизмаСкорость химических реакцийКонцентрации метаболитовАктивность ЕКоличество ЕГомеостаз; функционирование организма
- 44. Регуляция синтеза ферментов
- 45. Регуляция активности ферментов
- 46. Единицы ферментативной активностиЕ (U) = 1мкмоль/мин1 кат = 1 моль/с1 Е = 16.67 нкат
- 47. Активаторы ферментов
- 48. Скачать презентацию
- 49. Похожие презентации
Структурные единицы белков – аминокислоты Классификация аминокислотНеполярные (гидрофобные)Полярные (гидрофильные)Ароматические(главным образом неполярные)Отрицательно заряженныеПоложительно заряженные