- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Биотехнология производства антибиотиков
Содержание
- 2. План лекции:1. Общая характеристика антибиотиков2. Микроорганизмы – продуценты антибиотиков.3. Особенности получения антибиотиков.4. Технологическая схема производства пенициллина
- 3. Общая характеристика антибиотиковТермин «антибиотик» был предложен в
- 4. Антибиотики являются вторичными метаболитами -средствами преодоления стрессовых
- 5. Антибиотики являются «средством преодоления стрессовых ситуаций» для
- 6. Классификация антибиотиковПо характеру воздействия на бактериальную клетку
- 7. Классификация антибиотиковПо механизму биологического действия антибиотики делятся:1.
- 8. В зависимости от химической природы антибиотики делят
- 9. Классификация антибиотиков по штаммам-продуцентам:В зависимости от продуцирующих
- 10. Продуценты антибиотиковВ качестве продуцентов антибиотиков используются микроорганизмы,
- 12. Мицелиальные грибы, продуцирующие беталактамные антибиотики. мицелиальные грибы
- 13. Антибиотики животного происхождения. Экмолин, выделенный из осетровых
- 14. Значение антибиотиков для сельского хозяйства: 1. Антибиотики
- 15. Из большого числа антибиотиков, испытанных с целью
- 16. Применение антибиотиков в пищевой промышленности хозяйстваПервые сведения
- 17. Методы получения антибиотиков:1. Химический синтез. С помощью
- 18. рДНК-биотехнологии в создании антибиотиков4. рДНК-биотехнологии - создание
- 19. Биосинтез вторичных метаболитов Процесс развития микроорганизмов продуцентов
- 20. 1- трофофаза,
- 21. Схема
- 22. 4. Ферментация: для получения антибиотиков используют методы
- 23. 6. Очистка антибиотиков. включает стадии: осаждение, сорбцию,
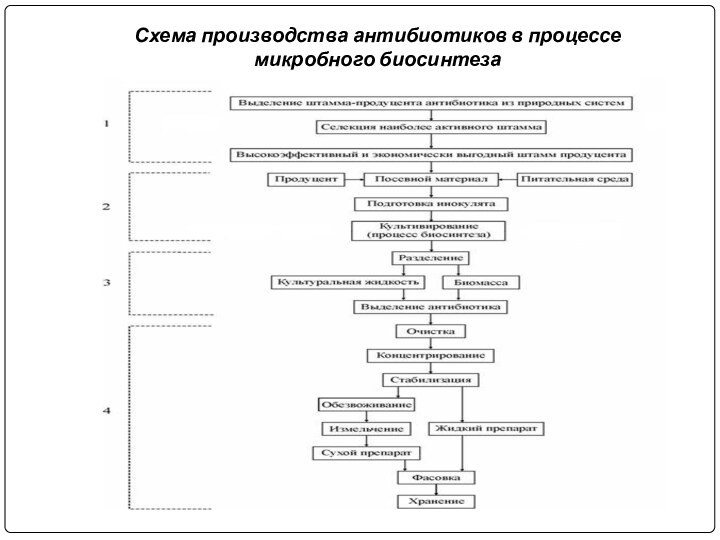
- 24. Схема производства антибиотиков в процессе микробного биосинтеза
- 25. Питательной среды Для каждого продуцента разрабатывается оптимальная
- 26. Большинство сапрофитных бактерий хорошо развивается на богатых
- 27. Источниками минерального питания служат фосфор, сера и
- 28. Влияние рН среды. Многие бактериальные организмы, синтезирующие
- 29. технологический процесс получения пенициллинаПодготовка инокулятаПодготовка посевного материала
- 30. Основные биотехнологические этапы получения антибиотика: 1
- 31. Состав одной из сред для выращивания посевного
- 32. Процесс ферментацииВ промышленности применяется метод глубинной ферментации,
- 33. Основными показателями, свидетельствующими об окончании ферментации, являются
- 34. Фильтрация Обычно для отделения мицелия от культуральной
- 35. Выделение и очисткаПроцессы экстракции и реэкстракции
- 36. Этапы технологии производства неочищенных антибиотиков: 1.
- 37. По окончании процесса ферментации антибиотиков культуральную жидкость
- 38. Аэрация посевного материала с использованием встряхивания на
- 39. Оценка антибиотиков на биологическую активность методами: перпендикулярных штрихов (А), по бумажных дисков (В), незапаянных цилиндриков (С)
- 40. Скачать презентацию
- 41. Похожие презентации
План лекции:1. Общая характеристика антибиотиков2. Микроорганизмы – продуценты антибиотиков.3. Особенности получения антибиотиков.4. Технологическая схема производства пенициллина






































Слайд 2
План лекции:
1. Общая характеристика антибиотиков
2. Микроорганизмы – продуценты
антибиотиков.
Слайд 3
Общая характеристика антибиотиков
Термин «антибиотик» был предложен в 1942
г. Зельман Абрахам Ваксман для обозначения веществ, образуемых микроорганизмами
и обладающих антимикробным действием. Разработка и производство антибиотиков активно началась в конце XIX века. Первым антибиотиком, выпущенным в промышленное производство, стал сальварсан (1910 год).Антибиотики – это группа высокоэффективных биологически активных веществ, которые синтезируются микроорганизмами и способны убивать или подавлять рост живых клеток.
В настоящее время под антибиотиками понимают химиотерапевтические вещества, полученные из микроорганизмов или иных природных источников, а также их полусинтетические аналоги и производные, обладающие способностью избирательно подавлять в организме больного возбудителей заболеваний и (или) задерживать развитие злокачественных новообразований.
Слайд 4
Антибиотики являются вторичными метаболитами -средствами преодоления стрессовых ситуаций
для продуцента
Предназначены для уничтожения микроорганизмов, конкурирующих с продуцентом за
питательные веществабиосинтез антибиотиков фазоспецифичен и происходит по завершении роста биомассы.
кривая накопления биомассы продуцента и кривая накопления антибиотика в культуральной жидкости не совпадают по времени,
кривая образования вторичного метаболита значительно запаздывает.
Слайд 5 Антибиотики являются «средством преодоления стрессовых ситуаций» для м/о.
Антибиотики для почвенных м/о являются не только средствами
борьбы, они
также являются низкомолекулярными «эффекторами» м/о; с их помощью м/о меняет свой метаболизм при неблагоприятных условиях (например, спорообразование). Каждый антибиотик - это конечный продукт длинной цепи специфических ферментативных реакций превращения первичных метаболитов в антибиотическую структуру.
Слайд 6
Классификация антибиотиков
По характеру воздействия на бактериальную клетку антибиотики
можно разделить на три группы:
- бактериостатические (бактерии живы,
но не в состоянии размножаться),- бактерициды (бактерии умертвляются, но физически продолжают присутствовать в среде),
- бактериолитические (бактерии умертвляются, и бактериальные клеточные стенки разрушаются).
Слайд 7
Классификация антибиотиков
По механизму биологического действия антибиотики делятся:
1. Антибиотики,
ингибирующие синтез бактериальной стенки (пенициллины, цефалоспорины, бацитрацин, ванкомицин).
2. Антибиотики,
нарушающие функционирование цитоплазматической мембраны (полипептиды, полиены, грамицидин).3. Антибиотики, разрушающие рибосомальные субчастицы и сдерживающие синтез белка (тетрациклины, хлормицетины, аминогликозиды, макролиды).
4. Антибиотики, избирательно подавляющие синтез нуклеиновых кислот:
- ингибиторы синтеза РНК (актиномицин, гризеофульвин, канамицин, неомицин, новобиоцин и др.);
- ингибиторы синтеза ДНК (брунеомицин, саркомицин).
Слайд 8 В зависимости от химической природы антибиотики делят на:
-лактамные (пенициллины, цефалоспорины);
-тетрациклины (тетрациклин, морфоциклин, метациклин);
-макролиды (эритромицин);
-аминогликозиды (гентамицин);
-гликопептиды (ванкомицин);
- амфениколы (левомицетин);
-линкосамиды (линкомицин);
-полиеновые (противогрибковые –нистатин);
-противоопухолевые (блеомицин) и др.
Слайд 9
Классификация антибиотиков по
штаммам-продуцентам:
В зависимости от продуцирующих организмов антибиотики
могут быть разделены на следующие группы:
1. Образуемые эубактериями: •
бактериями рода Bacillus: грамицидины, полимиксины и др.; • бактериями рода Pseudomonas: мупироцин, пиоцианин, антифунгин и др.; • бактериями других родов (Micrococcus, Streptococcus, Escherichia, Proteus): низин, колиформин и др.2. Образуемые бактериями рода Streptomyces: стрептомицин, тетрациклин, новобиоцин и др.
3. Образуемые несовершенными грибами: пенициллин, гризеофульвин и др.
4. Образуемые грибами классов базидио- и аскомицетов: термофиллин, лензитин, хетомин и др.
5. Образуемые лишайниками, водорослями, низшими растениями:
усниновая кислота и др.
6. Образуемые высшими растениями: аллицин, рафанин и др.
7. Образующиеся в организмах животных: лизоцим, интерферон, круцин и др.
Слайд 10
Продуценты антибиотиков
В качестве продуцентов антибиотиков используются микроорганизмы, плесневые
грибы, актиномицеты, высшие растения и ткани животных.
Микроорганизмы одного
вида могут синтезировать антибиотики различной природы и, наоборот, один и тот же антибиотик могут продуцировать микроорганизмы различных таксономических групп.Из эубактерий наиболее часто продуцентами являются представители родов Bacillus и Pseudomonas (около 400−600), причем большинство антибиотиков бактериального происхождения – полипептиды.
Слайд 11
Микроорганизмы – продуценты антибиотиков.
Актиномицеты – это многоклеточные
бактерии. Актиномицеты не имеют ядра (вместо ядра имеется одна
замкнутая нить ДНК), т.е. актиномицеты – прокариоты, не имеют митохондрий, имеют сложный цикл развития.Всего имеется 12 тысяч природных антибиотиков, из них 9 тысяч антибиотиков продуцируют актиномицеты.
Актиномицеты продуцируют следующие группы антибиотиков: (не менее 50 % из всех известных),
-канамицин - Actinomyces kanamycetus
-неомицин - Actinomyces iracie
-окситетрациклин – Аctinomyces ninesus
- линкомицин – Streptomyces linconiensis
Природный левомицетин (хлорамфеникол) продуцируется Streptomyces venezuelae.
Рифамицин – Streptomyces mediterranei, на основе рифамицина получен рифампицин.
Слайд 12
Мицелиальные грибы, продуцирующие беталактамные антибиотики.
мицелиальные грибы
продуцируют (около 10 %) антибиотиков:
Пенициллины – Penicillium
chrysogenum, P. notatum цефалоспорины Cephalosporium Acremonium chrysogenum являются известными представителями бета-лактамных антибиотиков, продуцирующимися мицелиальными грибами. В структуре антибиотика имеется бета-лактамное кольцо, обладающее способностью ингибирования синтеза пептидогликанов клеточной стенки. Антибиотики используются в лечении инфекций, вызванных грам(-) бактериями. Фторхинолоны – синтетические антибиотики. Обладают широким спектром антимикробного действия. Некоторые фторхинолоны обладают не только антибактериальной, и но и противоопухолевой , анти-ВИЧ-активностью.
Слайд 13
Антибиотики животного происхождения. Экмолин, выделенный из осетровых рыб,
эритрин – из эритроцитов, лизоцим и интерферон – обладающие
антимикробным и противовирусным действиями.Антибиотики, продуцируемые высшими растениями - фитонциды. Это аллицин из чеснока – Allium sativum, иманин из зверобоя, сальван из шалфея, рафанин из редиса - Raphanus sativum, фазеолин из фасоли - Phaseolus vulgaris и другие
Слайд 14
Значение антибиотиков для сельского хозяйства:
1. Антибиотики применяются для
лечения животных и птиц;
2. Кормовые антибиотики используются для
кормления животных и птиц. 3. Применяются антибиотики в растениеводстве для борьбы с болезнями растений, антибиотики используются в качестве гербицидов, инсектицидов и имеют 42 ряд преимуществ перед химическими препаратами.
4. Антибиотики применяются также в пищевой промышленности для консервирования продуктов питания, для сохранения свежего мяса, молока, рыбы и т.д.
Слайд 15 Из большого числа антибиотиков, испытанных с целью применения
для борьбы с различными заболеваниями растений, наибольший эффект наблюдается
при использовании стрептомицина, гризеофульфина, циклогексамида и некоторых других.Стрептомицин используется для борьбы с возбудителями, вызывающими бактериальное увядание фасоли и сои; болезнями косточковых (в США); хлопка, риса (в Индии). В некоторых странах выпускают препараты стрептомицина с окситетрациклином, известные как «агримицин», «фитомицин», «фитостреп».
Биалофос – гербицид, полученный в начале 1980-х годов из культуры S. hydroscopicus. По своей структуре представляет трипептид, со-
стоящий из двух остатков L-аланина и L-глутаминовой кислоты.
Антибиотики широко используются в животноводстве как лечебные средства против заболеваний сельскохозяйственных животных, птиц и пчел. Среди наиболее распространенных антибиотиков можно отметить авермектины, используемые для подавления развития паразитов, в том числе нематод; монензин для лечения кокцидоза домашней птицы; линкомицин для лечения дизентерии; новобиоцин для лечения холеры индеек.
Слайд 16
Применение антибиотиков в пищевой промышленности хозяйства
Первые сведения об
использовании антибиотиков в консервной промышленности относятся к 1943 году.
К таким антибиотикам относятся субтилин, низин и др.Так, для консервирования овощей предложено использовать субтилин, под действием которого наблюдается гибель клостридиальных и термофильных бактерий.
Низин – антибиотик, образуемый молочнокислыми бактериями, используется при консервировании не только овощей (томаты, зеленый горошек, цветная капуста), но и рыбы, молока, сыров и др. Антибиотик подавляет развитие ряда термофильных спорообразующих бактерий, не оказывая токсического действия на организм человека.
Слайд 17
Методы получения антибиотиков:
1. Химический синтез. С помощью этого
метода получают основные синтетические антибиотики.
2. Биосинтез (прямая ферментация микроорганизма
– продуцента). Для получения антибиотиков этим способом используют штаммы микроорганизмов, образующие наибольшее количество антибиотика. 3. Мутационный биосинтез (мутасинтез). Биосинтез антибиотиков с применением блокированных мутантов, у которых отсутствует или блокировано определенное звено в цепи реакций, ведущих к синтезу антибиотиков. Блокированные мутанты не способны образовывать нужный антибиотик. Используя низкую субстратную специфичность ферментов вторичного метаболизма и вводя аналоги предшественников антибиотиков, последние переводят в аналоги самого антибиотика в ходе процесса мутасинтеза.
Слайд 18
рДНК-биотехнологии в создании антибиотиков
4. рДНК-биотехнологии - создание высокоактивных
штаммов продуцентов антибиотиков.
С помощью рДНК можно создавать новые
антибиотики с уникальной структурой, оказывающие мощное воздействие на определенные микроорганизмы, обладающие минимальными побочными эффектами.
Слайд 19
Биосинтез вторичных метаболитов
Процесс развития микроорганизмов продуцентов вторичных
метаболитов носит двухфазный характер:
первая фаза развития (тропофаза или
фаза сбалансированного роста) характеризуется тем, что в культуре продуцента антибиотика происходит быстрое накопление биомассы. Биосинтез антибиотика в этот период не происходит или осуществляется в незначительном количестве. Эта фаза должна быть быстрой, а питательная среда – дешевой.вторая фаза (идиофаза или фаза несбалансированного роста) - во время идиофазы рост биомассы замедляется и происходит быстрое накопление антибиотика в культуральной жидкости.
Слайд 21
Схема промышленного биотехнологического производства антибиотиков
1. получение соответствующего штамма
— продуцента антибиотика, пригодного для промышленного производства;
2. подготовка
питательной среды: в технологии получения антибиотиков применяют твердые питательные среды – агаризованные или сыпучие субстраты (пшено, ячмень, пшеничные отруби и т.п.) и жидкие питательные среды.3. Подготовка посевного материала (продуценты-мутанты→ колба на качалке→ первый инокулятор (10 л)→ второй инокулятор (100–500 л)→ ферментер).
Слайд 22 4. Ферментация: для получения антибиотиков используют методы поверхностного
и глубинного культивирования.
В ходе ферментации культура непрерывно аэрируется
стерильным подогретым воздухом. Процесс ферментации осуществляется в строго стерильной глубинной аэробной периодической культуре, носит выраженный двухфазный характер. Температура среды, рН и ряд др. параметров автоматически регулируются в соответствии с регламентом производства антибиотика. Антибиотики получают при глубинной аэробной ферментации периодического действия в асептических условиях. Период ферментации длится 7-10 суток. 5.Выделение антибиотиков. Если антибиотик находится в клетках, на первом этапе обработки биомассу выделяют из культуральной жидкости (фильтрацией или центрифугированием); после разрушения клеток антибиотик экстрагируют и переводят в растворимую фазу. Затем данный раствор и культуральные среды (если антибиотик выделяется из клеток в среду) подвергают разным методам экстракции, разделения, очистки и концентрирования для получения готового продукта. Слайд 23 6. Очистка антибиотиков. включает стадии: осаждение, сорбцию, сушку.
Затем препарат фасуют в стерильные флаконы с соблюдением условий,
гарантирующих стерильность.7. Получение готового продукта: Готовый продукт подвергается биологическому и фармакологическому контролю. Биологический контроль определяет степень стерильности препарата. При фармакологическом контроле проводят всесторонние испытания препарата на токсичность, пирогенность, токсикогенность и др., оценивают антимикробный спектр препарата, действие на лейкоциты крови, устанавливают максимально переносимую дозу антибиотика, дозы, вызывающие полную и 50 % гибель экспериментальных животных.
Готовая форма лекарственного препарата антибиотического вещества поступает к потребителю с указанием биологической активности и даты выпуска.
Слайд 25
Питательной среды
Для каждого продуцента разрабатывается оптимальная среда, которая
должна соответствовать определенным требованиям:
а) обеспечивать максимальный выход антибиотика;
б) состоять
из относительно дешевых компонентов;в) иметь хорошую фильтрующую способность;
г) обеспечивать применение наиболее экономичных приемов для выделения и очистки антибиотиков.
Используются следующие среды:
мясопептонная среда, в состав которой одновременно с мясным экстрактом и пептоном входят хлорид натрия, фосфат калия, иногда глюкоза или сахароза; используется обычно в лабораторной практике;
картофельные среды с глюкозой и пептоном, часто используемые в лаборатории для культивирования многих видов актиномицетов и бактерий;
среды с кукурузным экстрактом, соевой мукой, бардой и другими веществами, в состав которых входят сульфат аммония, карбонат кальция, фосфаты, глюкоза, сахароза, лактоза или иные углеводы и ряд других соединений; среды успешно применяются в промышленности, т. к. являются дешевыми и обеспечивают хорошее развитие микроорганизмов с высоким выходом антибиотиков.
Слайд 26 Большинство сапрофитных бактерий хорошо развивается на богатых по
составу натуральных средах (мясопептонный агар, картофельный агар, сусло-агар и
др.) при рН около 7,0 и температуре 30–37 °С. В этих же условиях развиваются актиномицеты и некоторые грибы, но для них они менее благоприятны, чем для бактерий.Значение рН среды после стерилизации устанавливается в пределах 6,8–7,1.
Мицелиальные грибы предпочтительнее развиваются на средах с несколько пониженным значением рН (4,5–5,0), на которых плохо растут многие бактерии и актиномицеты.
Стерилизация питательных сред в промышленных условиях достигается в результате:
• периодического метода для небольших объемов среды, при котором среда нагревается до 120–130 оС непосредственно в ферментере и выдерживается в течение определенного времени;
• непрерывного метода для значительных объемов, при котором приготовленная среда подается в стерилизационную колонку, через которую пропускают острый пар. Нагретая до необходимой температуры среда поступает в специальный аппарат, где выдерживается определенное время.
Слайд 27 Источниками минерального питания служат фосфор, сера и другие
макро- и микроэлементы.
Продуценты антибиотиков по отношению к концентрации фосфора
в среде можно разделить на три группы:- высокочувствительные продуценты, для которых оптимальная концентрация фосфора в среде составляет менее 0,01 % (продуценты нистатина, тетрациклинов, флоримицина, ванкомицина);
- продуценты средней чувствительности, для которых оптимальная концентрация фосфора составляет 0,010–0,015 % (продуценты стрептомицина, эритромицина, циклосерина, неомицина);
- малочувствительные продуценты, для которых оптимальная концентрация фосфора составляет 0,018–0,020 % (продуценты новобиоцина, грамицидина, олеандомицина).
Слайд 28 Влияние рН среды. Многие бактериальные организмы, синтезирующие антибиотики,
лучше развиваются при рН около 7,0, хотя некоторые, например
молочнокислые стрептококки, продуцирующие низин, лучше развиваются в среде при рН = 5,5÷6,0. Большинство актиномицетов хорошо развиваются при начальных значениях рН среды в пределах от 6,7 до 7,8; в большинстве случаев жизнеспособность актиномицетов при рН ниже 4,0–4,5 подавлена.Температура. Для большинства бактериальных организмов температурный оптимум развития лежит в диапазоне 30–37 °С. Для продуцента грамицидина С оптимальная температура для развития и биосинтеза равна 40 °С.
Актиномицеты, как правило, культивируются при температуре 26–30°С, хотя некоторые виды стрептомицетов могут развиваться как при пониженных (от 0 до 18 °С), так и при повышенных (55–60 °С) температурах.
Для большинства мицелиальных грибов оптимальная температура составляет 25–28 °С.
Аэрация. Большинство изученных продуцентов антибиотиков являются аэробами. Для биосинтеза многих антибиотиков (пенициллин, стрептомицин и др.) максимальное их накопление происходит при степени аэрации, равной единице, при которой через определенный объем среды за 1 мин продувается такой же объем воздуха.
В процессе развития продуцента антибиотика в промышленных условиях потребность организма в кислороде меняется в зависимости от стадии развития, вязкости культуральной жидкости и других факторов. На определенных стадиях могут возникнуть ситуации, связанные с кислородным голоданием продуцента. В этих условиях следует принимать дополнительные меры, например, повышение концентрации окислителя добавлением пероксида водорода.
Слайд 29
технологический процесс получения пенициллина
Подготовка инокулята
Подготовка посевного материала включает
следующие стадии:
1) выращивание посевного мицелия 1-й генерации в аппаратах
малой емкости (инокуляторах);2) выращивание посевного мицелия 2-й генерации в аппаратах большой емкости.
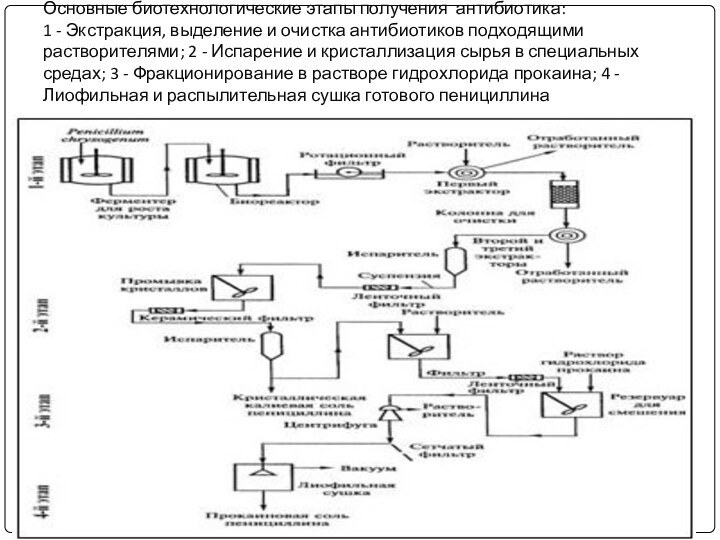
Слайд 30 Основные биотехнологические этапы получения антибиотика: 1 - Экстракция, выделение
и очистка антибиотиков подходящими растворителями; 2 - Испарение и
кристаллизация сырья в специальных средах; 3 - Фракционирование в растворе гидрохлорида прокаина; 4 - Лиофильная и распылительная сушка готового пенициллина
Слайд 31
Состав одной из сред для выращивания посевного материала.
Вещество
%
Кукурузный экстракт 2 (на сухой вес)
Глюкоза 2
Лактоза 0,5
Азотнокислый аммоний 0,125
Однозамещенный фосфорнокислый калий 0,2
Сернокислый магний 0,025
Сернокислый натрий 0,05
Мел 0,5
Слайд 32
Процесс ферментации
В промышленности применяется метод глубинной ферментации, при
котором культура микроорганизма выращивается в питательной среде, заполняя весь
ее объем.Предшественниками называются вещества, непосредственно включающиеся в молекулу получаемого продукта. Предшественником бензилпенициллина является фенилуксусная кислота (ФУК) или ее производные - фенилацетамид (ФАА), фенилэтиламин, фенилацетилглицин и другие вещества. Предшественником феноксиметилпенициллина является феноксиуксусная кислота (ФОУК)
Слайд 33 Основными показателями, свидетельствующими об окончании ферментации, являются полное
исчезновение углеводов в культуральной жидкости и прекращение биосинтеза антибиотика.
Процесс ферментации в производственных условиях осуществляется при температуре 26±10С и продолжается обычно 120-125 часов.
Слайд 34
Фильтрация
Обычно для отделения мицелия от культуральной жидкости применяют
вакуум-барабанные фильтры непрерывного действия. Фильтрацию начинают до начала автолиза
мицелия, поскольку при фильтрации автолизированной культуры мицелий не образует плотной пленки на фильтрующей поверхности барабана, а налипает в виде отдельных тонких комков, которые сами не отходят в зоне «отдувки» фильтра, и их приходится удалять вручную. При этом продолжительность фильтрации увеличивается в 2 - 3 раза, выход фильтрата резко падает, а сам фильтрат получается очень мутным.Необходимо тщательно соблюдать условия, препятствующие разрушению пенициллина во время фильтрации, - охлаждение нативного раствора до 4-6°С и систематическая (после каждой загрузки) обработка фильтра, коммуникаций и сборников антисептиками, например хлорамином. Фильтр также должен систематически стерилизоваться острым паром.
Слайд 35
Выделение и очистка
Процессы экстракции и реэкстракции для
пенициллинов и эритромицина
Ионообменная и адсорбционная хроматографии - для
аминогликозидовтетрациклины - осаждение, экстракция органическими растворителями и методы ионообменной хроматографии.
сублимационная или распылительная сушка
Слайд 36
Этапы технологии производства неочищенных антибиотиков:
1. Посуду, инструменты,
материалы стерилизуют, используя для этой цели автоклаве водяным паром
в течение 30-45 минут. Наиболее эффективным способом стерилизации рабочего бокса является ультрафиолетовое облучение его бактерицидной лампой в течение 60 минут.2. Для размножения гриба используют его исходную культуру, расфасованную в стеклянные флаконы. Для расплодки посевного материала производят посев грибка в колбу над пламенем спиртовой горелки. Колбы с посевным материалом ставят на специальную качалку для лучшей аэрации с целью более интенсивного роста грибка при температуре от 26 до 28° С на 18-24 ч.
3. Переносят посевной материал в большие бутыли и вновь помещают на качалку и подвергают встряхиванию при температуре 26-28° С в течение 18-24 ч.
4. Производят загрузку расплодки гриба и необходимых компонентов питательной среды в специальные реакторы для ферментации.
При изготовлении кормового нативного антибиотика ферментация протекает 24—36 ч. Через каждые 6-12 ч из ферментатора отбирают пробу для проверки антибиотика на активность. В процессе развития грибка в ферментаторе скапливаются газообразные продукты его жизнедеятельности, которые удаляются через шланг.
Слайд 37 По окончании процесса ферментации антибиотиков культуральную жидкость проверяют
на активность преимущественно следующими микробиологическими методами:
методом перпендикулярных штрихов на
агаре. Для этого вырезанную в питательной среде канавку заполняют средой с антибиотиком. Перпендикулярно канавке засевают различные виды микроорганизмов. Длина белых полосок указывает на неодинаковую чувствительность микробов к антибиотику. методом бумажных дисков. Для этого на питательную среду, засеянную микробами, накладывают диски из фильтровальной бумаги, пропитанные антибиотиком. В центре наложен диск без антибиотиков (контрольный). Вокруг диска с антибиотиками роста микроорганизмов не наблюдается (зона угнетения);
методом цилиндриков. Для этого в питательную среду, засеянную бактериями, погружают стеклянные или металлические незапаянные цилиндрики, которые заполняют антибиотиками. Ширина зоны угнетения вокруг цилиндриков указывает на антимикробные свойства антибиотиков.