- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Чистота и здоровье человека
Содержание
- 2. Цели:Изучить состав и свойства как современных, так
- 3. Задачи:Провести опрос среди одноклассников, что они знают
- 4. Гипотеза:Средства гигиены позволяют сохранить здоровье человека
- 5. Проблема:Средства гигиены- польза или вред?
- 6. План исследовательской работы:Актуальность исследовательской работыЧто представляют собой
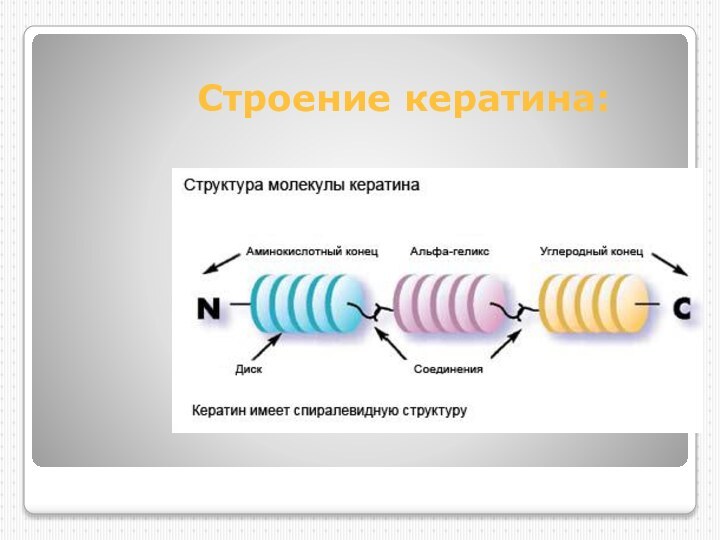
- 7. Строение кератина:
- 8. Ph- показатель содержания в растворе ионов водорода Ph чистой воды - 7
- 9. Строение и состав волоса
- 10. Нити фибрилл:
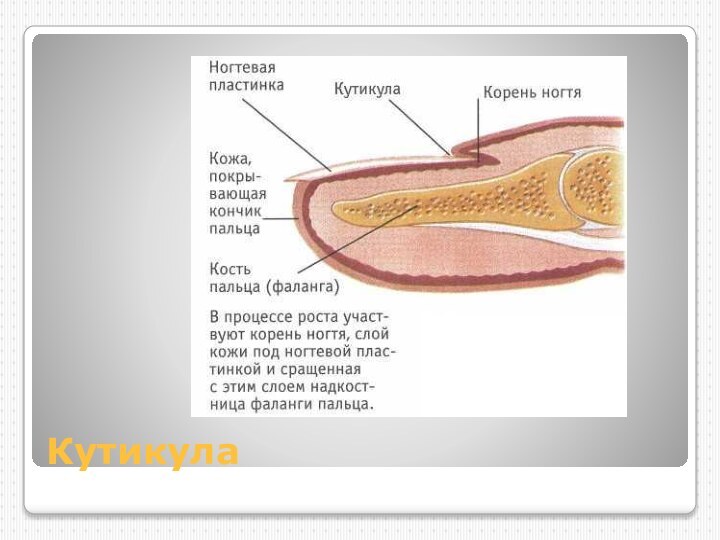
- 11. Кутикула
- 12. Окрашивание волос
- 13. Типы красителей:ОтбеливающиеХимическиеФизическиеЕстественного происхожденияМеталлосодержащие
- 15. Пероксид водорода (пергидроль)Н2О2 = Н2О + О
- 16. Задание №1 Все твердые туалетные
- 17. Ответ: Калиевые соли высших карбоновых кислот –
- 18. Задание №2Дезодоранты по принципу действия делятся на
- 19. Ответ: Оба способа следует отнести к химико
- 20. Задание №3 Во время
- 21. Ответ: Зола содержит большое количество карбоната калия:
- 22. Скачать презентацию
- 23. Похожие презентации
Цели:Изучить состав и свойства как современных, так и старинных средств гигиеныПоказать, как знание химии позволяет более грамотно выбирать средства гигиены


















Слайд 2
Цели:
Изучить состав и свойства как современных, так и
старинных средств гигиены
выбирать средства гигиены
Слайд 3
Задачи:
Провести опрос среди одноклассников, что они знают о
средствах гигиены
Провести исследование состава и свойств различных видов гигиены
Слайд 6
План исследовательской работы:
Актуальность исследовательской работы
Что представляют собой загрязнения
кожи и волос
Способы очистки кожи и волос. Характеристика моющего
средстваСредства гигиены во время ВОВ
Слайд 13
Типы красителей:
Отбеливающие
Химические
Физические
Естественного происхождения
Металлосодержащие
Слайд 16
Задание №1
Все твердые туалетные мыла
изготовлены на основе нитриевых солей высших жирных кислот. Но
людям с повышенной жирностью кожи лица и головы врачи – дерматологи рекомендуют умываться и мыть голову жидким мылом, которое изготавливают из калиевых солей жирных кислот или препаратом, которое продается в аптеках под названием «зеленое мыло» и представляет собой чистое калийное мыло без ароматизаторов. Как это можно объяснить?
Слайд 17
Ответ:
Калиевые соли высших карбоновых кислот – стеариновой
и пальмитиновой – по сравнению с натриевыми лучше растворимы
в воде и поэтому обладают более сильным моющим действием.
Формула твердого мыла
Слайд 18
Задание №2
Дезодоранты по принципу действия делятся на два
типа. Одни содержат бактерицидные вещества, уничтожающие микроорганизмы и таким
образом тормозящие бактериальное разложение пота. Препараты второго типа содержат вещества, взаимодействующие с компонентами пота с образованием нерастворимых соединений, которые закрывают каналы потовых желез и таким образом уменьшают потовыделение (например, алюмокалиевые квасцы КАI(SO4) * 12 Н2О, формальдегид СН2 = О).Определите, какому способу можно отнести описанные приемы борьбы с запахом пота – к биологическому, химическому или химико – биологическому?. И какой из описанных способов можно считать более физиологичным?
Слайд 19
Ответ:
Оба способа следует отнести к химико –
биологическим, так как в том и другом случае имеют
место и химические, и биологические процессы. Более физиологичным является первый способ, так как потоотделение – естественный процесс, способствующий терморегуляции организма и выведению продуктов обмена, и лучше ему не препятствовать.
Слайд 20
Задание №3
Во время Великой
Отечественной войны и в первые послевоенные годы, когда был
дефицит мыла, многие женщины мыли волосы процеженным настоем древесной золы. И сейчас иногда в деревнях принято мыться в бане и мыть голову хотя и с мылом, но не чистой водой, а настоем золы. Особенно это распространено там, где пользуются не речной, а колодезной водой. Как можно объяснить применение золы для этих целей?
Слайд 21
Ответ:
Зола содержит большое количество карбоната калия:
К2СО3
+ Н2О = КОН + КНСО3
В растворе
накапливаются ионы ОН-, поэтому среда становится щелочной. Под действием щелочи происходит омыление жиров.Кроме того, зола хорошо смягчает воду, так как карбонат калия осаждает растворимые соли кальция и магния.