Слайд 2
Органические вещества клетки:
Белки
Жиры
Углеводы
Нуклеиновые кислоты
БЕЛКИ, высокомолекулярные
органические соединения, биополимеры, построенные из 20 видов L-a-аминокислотных остатков, соединенных в определенной последовательности в длинные цепи.
Название «белки» впервые было дано веществу птичьих яиц, свертывающемуся при нагревании в белую нерастворимую массу. Позднее этот термин был распространен на другие вещества с подобными свойствами, выделенные из животных и растений.
Слайд 4
Многие белки построены из 20 a-аминокислот, принадлежащих к
L-ряду, и одинаковых практически у всех организмов. Аминокислоты в
белках соединены между собой пептидной связью—СО—NH—, которая образуется карбоксильной и a-аминогруппой соседних аминокислотных остатков (см. рис.): две аминокислоты образуют дипептид, в котором остаются свободными концевые карбоксильная (—СООН) и аминогруппа (H2N—), к которым могут присоединяться новые аминокислоты, образуя полипептидную цепь.
Участок цепи, на котором находится концевая Н2N-группа, называют N-концевым, а противоположный ему — С-концевым. Огромное разнообразие белков определяется последовательностью расположения и количеством входящих в них аминокислотных остатков. Хотя четкого разграничения не существует, короткие цепи принято называть пептидами или олигопептидами, а под полипептидами (белками) понимают обычно цепи, состоящие из 50 и более аминокислот.
Слайд 5
Функции белков
Катализаторы (белки – ферменты)
Регуляторы биологических процессов (ферменты)
Транспортная
(гемоглобин)
Двигательная (актин, миозин)
Строительная (кератин, коллаген)
Энергетическая – 1 г белка
– 17кДж (казеин, яичный альбумин)
Защитная (иммуноглобулины, интерферон)
Антибиотики (неокарциностатин)
Токсины (дифтерийный)
Рецепторные белки (родопсин, холинорецепторы)
Слайд 6
Структура белка
Первичная(линейная):состоит из пептидной связи (инсулин)
Вторичная (спиральная):имеются пептидная
и водородная связи (волосы, когти и ногти)
Третичная : трехмерное
расположение вторичной структуры молекулы белка. Связи : пептидная, ионная, водородная, дисульфидная, гидрофобная (клеточная мембрана)
Четвертичная : образуется из 2-3-х глобул (третичных структур) (гемоглобин)
Слайд 7
Денатурация белков
Сравнительно слабые связи, ответственные за стабилизацию вторичной,
третичной и четвертичной структур белка, легко разрушаются, что сопровождается
потерей его биологической активности. Разрушение исходной (нативной) структуры белка, называемое денатурацией, происходит в присутствии кислот и оснований, при нагревании, изменении ионной силы и других воздействиях. Как правило, денатурированные белки плохо или совсем не растворяются в воде. При непродолжительном действии и быстром устранении денатурирующих факторов возможна ренатурация белка с полным или частичным восстановлением исходной структуры и биологических свойств.
Слайд 8
Значение белков в питании
Белки - важнейшие компоненты пищи
животных и человека. Пищевая ценность белков определяется содержанием в
них незаменимых аминокислот, которые в самом организме не образуются. В этом отношении растительные белки менее ценны, чем животные: они беднее лизином, метионином и триптофаном, труднее перевариваются в желудочно-кишечном тракте. Отсутствие незаменимых аминокислот в пище приводит к тяжелым нарушениям азотистого обмена. В процессе пищеварения белки расщепляются до свободных аминокислот, которые после всасывания в кишечнике поступают в кровь и разносятся ко всем клеткам. Часть из них распадается до простых соединений с выделением энергии, используемой на разные нужды клеткой, а часть идет на синтез новых белков, свойственных данному организму.
Слайд 10
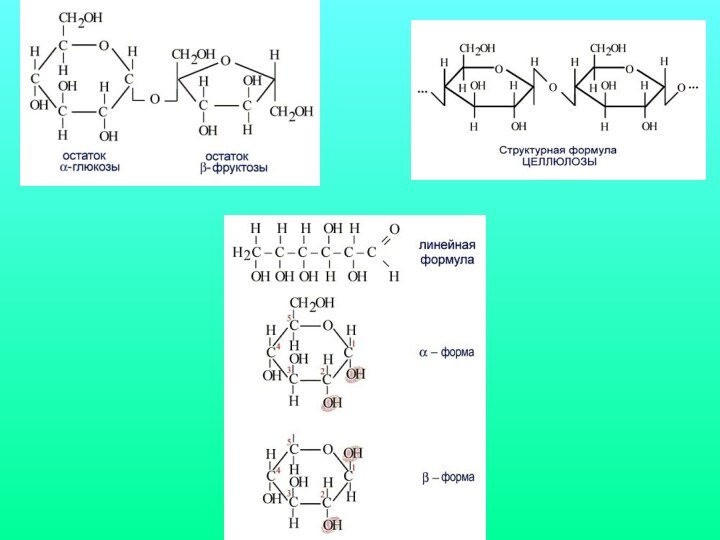
УГЛЕВОДЫ – органические соединения, химическая структура которых часто
отвечает общей формуле Cn(H2O)n(т. е. углерод и вода, отсюда
название). Углеводы — первичные продукты фотосинтеза и основные исходные продукты биосинтеза других веществ в растениях. Составляют существенную часть пищевого рациона человека и многих животных. Подвергаясь окислительным превращениям, обеспечивают все живые клетки энергией (глюкоза и ее запасные формы — крахмал, гликоген). Различают моно-, олиго- и полисахариды, а также сложные углеводы — гликопротеиды, гликолипиды, гликозиды и др.
Слайд 11
МОНОСАХАРИДЫ, простые углеводы, содержащие гидроксильные и альдегидную (альдозы)
или кетонную (кетозы) группы. По числу атомов углерода различают
триозы, тетрозы, пентозы и т. д. В живых организмах в свободном виде (кроме глюкозы и фруктозы) встречаются редко. В составе сложных углеводов (гликозидов, олиго- и полисахаридов и др.) присутствуют во всех живых клетках.
ДИСАХАРИДЫ, углеводы, образованные остатками двух моносахаридов. В животных и растительных организмах распространены дисахариды: сахароза, лактоза, мальтоза, трегалоза.
ПОЛИСАХАРИДЫ, высокомолекулярные углеводы, образованные остатками моносахаридов (глюкозы, фруктозы и др.) или их производных (напр., аминосахаров). Присутствуют во всех организмах, выполняя функции запасных (крахмал, гликоген), опорных (целлюлоза, хитин), защитных (камеди, слизи) веществ. Участвуют в иммунных реакциях, обеспечивают сцепление клеток в тканях растений и животных.
Слайд 13
Функции углеводов
Структурная (входят в состав оболочек клеток и
субклеточных образований)
Опорная (у растений)
Резервная (запас гликогена и крахмала)
Энергетическая
Сигнальная (нервные
импульсы)
участвуют в защитных реакциях организма (иммунитет).
Применяются в пищевой (глюкоза, крахмал, пектиновые вещества), текстильной и бумажной (целлюлоза), микробиологической (получение спиртов, кислот и других веществ сбраживанием углеводов) и других отраслях промышленности.
Используются в медицине (гепарин, сердечные гликозиды, некоторые антибиотики).
Слайд 14
Жиры
ЖИРЫ, органические соединения, в основном сложные эфиры глицерина
и одноосновных жирных кислот (триглицериды); относятся к липидам. Один
из основных компонентов клеток и тканей живых организмов. Источник энергии в организме; калорийность чистого жира 3770 кДж/100 г. Природные жиры подразделяются на жиры животные и масла растительные.
Слайд 15
Функции жиров:
Структурная (входят в состав клеточных мембран)
Энергетическая (1г
- 38.9 кДж энергии)
Запасающая
Терморегуляторная
Источник метаболической (эндогенной) воды
Защитно-механическая (защита от
повреждений)
Каталитическая (входят в состав ферментов)
Слайд 16
Нуклеиновые кислоты
НУКЛЕИНОВЫЕ КИСЛОТЫ (полинуклеотиды), высокомолекулярные органические соединения, обеспечивающие
хранение и передачу наследственной (генетической) информации в живых организмах
из поколения в поколение. В зависимости от того, какой углевод входит в состав нуклеиновой кислоты — дезоксирибоза или рибоза, различают дезоксирибонуклеиновую (ДНК) и рибонуклеиновую (РНК) кислоты. Последовательность нуклеотидов в нуклеиновых кислотах определяет их первичную структуру.
Слайд 17
Химическая структура.
В зависимости от химической структуры углеводного
компонента нуклеиновые кислоты делят на два типа: дезоксирибонуклеиновые и
рибонуклеиновые; первые содержат дезоксирибозу, а вторые — рибозу. Азотистые основания являются производными двух типов соединений — пуринов и пиримидинов. Основаниями они называются потому, что обладают основными (щелочными) свойствами, хотя и слабыми. В составе ДНК встречаются два пуриновых— аденин (А) и гуанин (G) и два пиримидиновых — цитозин (С) и тимин (Т) основания. В составе РНК вместо тимина обычно встречается урацил (U). Согласно правилам международной номенклатуры эти основания записываются начальными буквами их названий на английском языке, хотя в русскоязычной литературе часто используются начальные буквы русских названий; соответственно А, Г, Ц, Т и У.
Слайд 18
В молекулах нуклеиновых кислот нуклеотиды связаны между собой
фосфодиэфирными связями (фосфатными «мостиками»), образующимися между остатками сахаров соседних
нуклеотидов. Таким образом, цепи нуклеиновых кислот выглядят как остов из монотонно чередующихся фосфатных и пептозных групп, а основания можно рассматривать как присоединенные к нему боковые группы. Фосфатные остатки остова при физиологических значениях рН заряжены отрицательно. Пуриновые и пиримидиновые основания плохо растворимы в воде, то есть гидрофобны. О свойствах отдельных типов нуклеиновых кислот и их роли в процессах жизнедеятельности смотри в статьях Дезоксирибонуклеиновые кислоты и Рибонуклеиновые кислоты.
Строение молекул ДНК и РНК
Слайд 19
ДЕЗОКСИРИБОНУКЛЕИНОВЫЕ КИСЛОТЫ (ДНК), нуклеиновые кислоты, содержащие в качестве
углеводного компонента дезоксирибозу. ДНК является основной составляющей хромосом всех
живых организмов; ею представлены гены всех про- и эукариот, а также геномы многих вирусов. В нуклеотидной последовательности ДНК записана (кодирована) генетическая информация о всех признаках вида и особенностях особи (индивидуума) — ее генотип. ДНК регулирует биосинтез компонентов клеток и тканей, определяет деятельность организма в течение всей его жизни.
Слайд 21
РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ (РНК), семейство нуклеиновых кислот, содержащих в
качестве углеводного компонента остаток рибозы. PНK присутствуют во всех
живых клетках, участвуя в процессах, связанных с передачей генетической информации от дезоксирибонуклеиновой кислоты(ДНК) к белку. Из РНК образованы геномы многих вирусов.
За редким исключением все PНK состоят из одиночных полинуклеотидных цепей. Их многомерные единицы — монорибонуклеотиды — содержат пуриновые— аденин и гуанин и пиримидиновые основания — цитозин и урацил.