Слайд 2
ЦЕЛИ УРОКА:
продолжить формирование понятий количества вещества;
показать взаимосвязь
физико-химических величин: массы, объема, количества вещества и числа частиц;
научить
производить расчеты с указанными величинами;
показать межпредметную связь предметов: математики и химии;
продолжить формирование умений решать расчетные задачи с помощью алгоритма слабоуспевающими учащимися;
Определить роль консультанта (учителя или учащегося) в работе слабоуспевающих учащихся.
Слайд 3
Эпиграф:
О, физика – наука из наук!
Все впереди!
Как мало
за плечами!
Пусть химия нам будет вместо рук.
Пусть станет математика
очами.
Не разлучайте этих трех сестер
Познания всего в подлунном мире,
Тогда лишь будет ум и глаз остер
И знанье человеческое шире.
(отрывок из поэмы М. Алигер
“Ленинские горы”)
Слайд 4
Выполните задания устно:
Вычислите:
7,2∙10, 7,2 :100;
0,072 :100;
0,072∙10000.
Представьте в виде степени с основанием 10:
0,01; 1/1000; 10; 1; 100; 1000; 10000000;0,0000000001.
Слайд 5
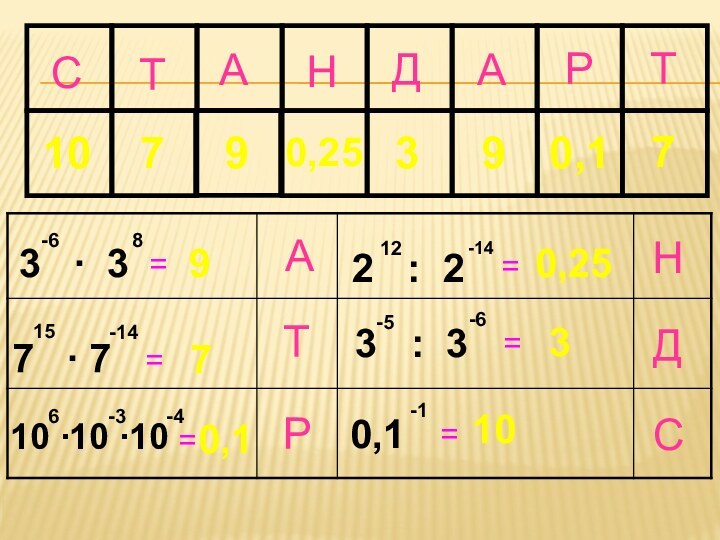
С
А
Р
Д
Н
А
Т
Р
Т
А
Д
Н
С
=
=
10
9
=
=
7
3 ∙ 3
=
0,1
-1
7 ∙ 7
10
∙10 ∙10
6
-3
0,1
0,1
2 : 2
=
12
-14
8
0,25
3 : 3
-5
-6
3
9
9
-14
15
7
0,25
3
10
-6
Т
7
-4
Слайд 6
Стандарт (от англ. – standard) (универсальный энциклопедический словарь)
образец,
эталон, модель,
с которым сопоставляются,
сравниваются подобные
объекты, процессы.
Слайд 7
Стандартный вид числа
Стандартным видом числа называется запись вида:
a ·10ⁿ , где 1 ≤ а< 10, n
Є Z
n- порядок числа
Слайд 8
Запишите в стандартном виде
1) 0,000 000 000
000 000 000 000 02662
2) 0,000
000 06
3) 0,000 000 1
4) 0,000 000 03
Слайд 9
ОТВЕТ
1) 2,662∙ 10⁻²³ г (Масса атома
кислорода)
2) 6 ∙ 10⁻⁸ см (Толщина
пленки мыльного
пузыря)
3) 1 · 10⁻⁷ см (Единица длины - ангстрем)
4) 3 ∙ 10⁻⁸ см (Диаметр молекулы воды)
Слайд 10
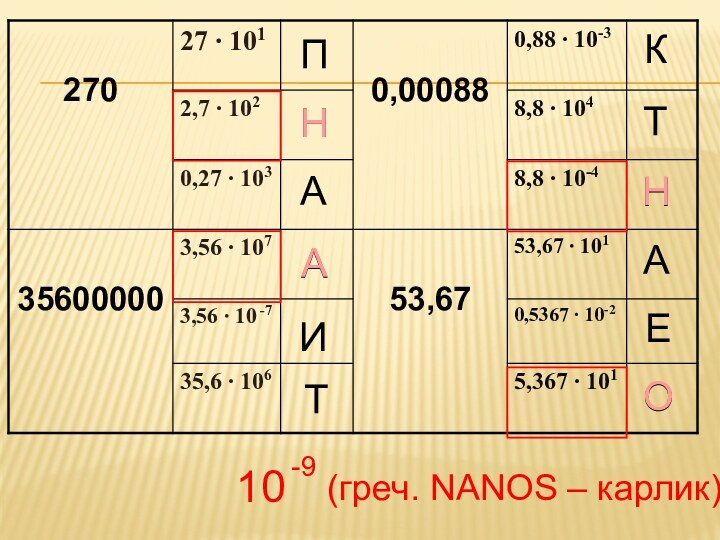
П
Н
А
А
И
Т
К
Т
Н
А
Е
О
Н
Н
А
О
10
-9
(греч. NANOS – карлик)
Слайд 11
Графический диктант
Ответьте на вопросы («да» – галочка, «нет»
– палочка)
Число 3 • 105 записано в стандартном
виде
Число 0,81 • 106 записано в стандартном виде
7,45 • 10–5 записано в стандартном виде
Число 50 записано в стандартном виде
Верно ли высказывание: «Чем больше порядок числа, тем больше само число?»
Если порядок числа отрицательный, то и само число отрицательно?
Если перемножить два числа в стандартном виде, то ответ будет числом в стандартном виде?
В стандартном виде можно записать любое число.
ЭКСПРЕСС- ОПРОС
(шуточное стихотворение)
1)Расскажу сегодня,
что ли,
О зловредной роли моли.
Моль съедает шерсть и мех –
Просто паника у всех….
Ну а в химии – изволь!
Есть другое слово “моль”
Прост, как небо и трава,
Моль любого вещества.
Но трудна его дорога:
В моле так молекул много!
Задача:
Сколько ж молекул в моле?
Слайд 14
2) Маша маме говорит
Что из шкафа
моль летит
« Как спасти нам вещи наши?»
Отвечает мама Маше:
Есть такой аэрозоль,
Убивает моли моль!
Маша химию учила,
Так что маме возразила:
«Что-то это многовато-
Целый моль врагов крылатых!
ЗАДАЧА. Рассчитайте массу 1моль моли, если масса 1 бабочки 0,01г.
(2мин)
Слайд 15
1. Что такое количество вещества?
2. Что
такое моль?
4. Сколько структурных единиц содержится в 1
моле?
5. Через какие величины можно определить количество вещества?
6. Что такое Молярная масса, с чем численно совпадает?
Масса 3 моль H2O составляет ______________
Масса 20 моль СО2 составляет ____________
7. Что такое молярный объем?
Экспресс-опрос:
Слайд 16
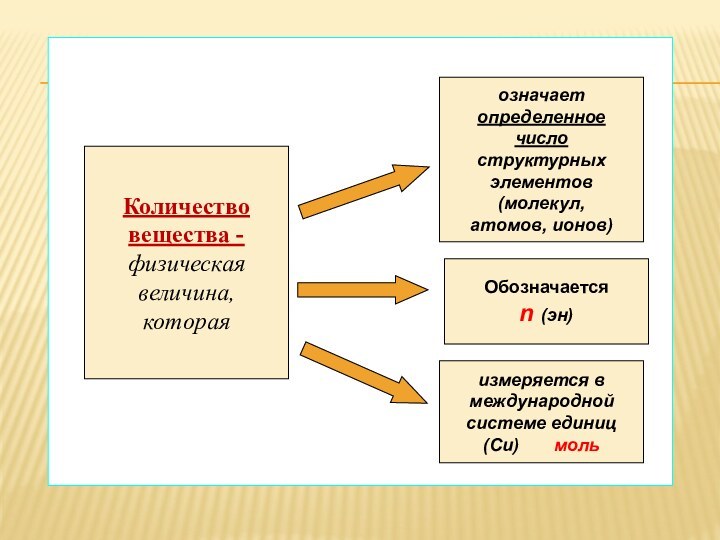
Количество
вещества -
физическая
величина,
которая
означает
определенное
число
структурных
элементов
(молекул,
атомов, ионов)
Обозначается
n
(эн)
измеряется в
международной
системе единиц
(Си) моль
Слайд 17
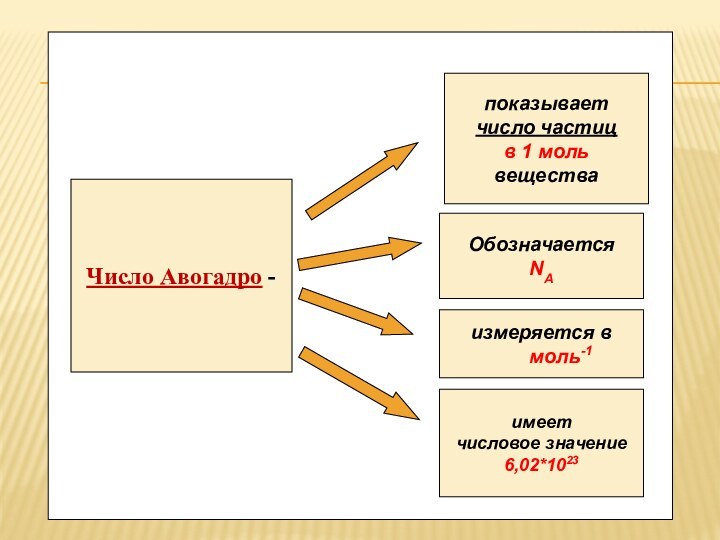
Число Авогадро -
показывает
число частиц
в 1
моль
вещества
Обозначается
NA
измеряется в
моль-1
имеет
числовое
значение
6,02*1023
Слайд 18
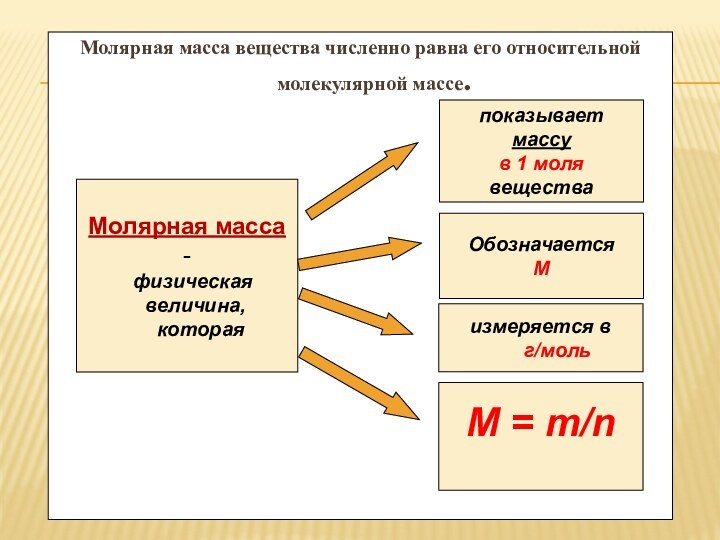
Молярная масса вещества численно равна его
относительной молекулярной массе.
Молярная масса -
физическая
величина,
которая
показывает
массу
в 1 моля
вещества
Обозначается
М
измеряется в
г/моль
М = т/n
Слайд 19
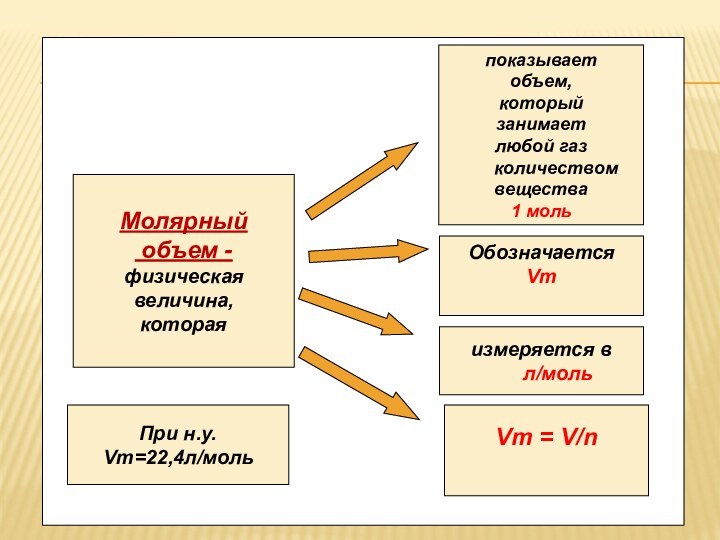
Молярный
объем -
физическая
величина,
которая
показывает
объем,
который
занимает
любой газ
количеством
вещества
1 моль
Обозначается
Vm
измеряется в
л/моль
Vm =
V/n
При н.у. Vm=22,4л/моль
Слайд 20
Теоретическое исследование
Задача 1.
В стратосфере
на высоте 20-30 км находится слой озона О3, защищающий
Землю от мощного ультрафиолетового излучения Солнца. Если бы не «озоновый экран» в атмосфере, то фотоны достигали бы поверхности Земли и уничтожали на ней все живое. Подсчитано, что в среднем на каждого жителя Санкт-Петербурга в воздушном пространстве над городом (вплоть до верхней границы стратосферы) приходится по 10 моль озона. Сколько молекул 03 и какая масса озона приходится в среднем на одного жителя Санкт-Петербурга?
Слайд 21
Теоретическое исследование
Задача 2.
Рассчитайте объем, который
занимает (при н. у.) порция газа, необходимого для дыхания,
если в этой порции содержится 2,69 • 1022 молекул этого газа. Какой это газ?
Слайд 22
Практическое исследование
Задание №3
Каждый день мы употребляем сахар,
например,
когда пьем чай.
Но вы когда-нибудь задумывались:
1. сколько
моль сахара содержится в кусочке рафинада?
2. Какое число молекул сахарозы вы выпиваете с чаем?
Слайд 23
Практическое исследование
Задание №4
Вам нужно приготовить сахарный сироп,
например, для десерта (он готовится в отношении сахара к
воде 2:1). Но с сахаром уже работает группа№3,а вы теперь работаете с водой. В каком она состоянии? (жидком, твёрдом или газообразном). И поэтому будем определять её объём. Для этого воспользуемся мерным цилиндром.
В мерный цилиндр отмерьте 12 столовых ложек воды. Определите объём и ответьте на вопрос:Какое количество моль и молекул воды содержится в этом объёме?
Слайд 24
ТЕОРЕтическое исследование
Задание №5 (для консультантов)
Массовая доля костей человека составляет 20% от общей массы
организма. На долю фосфата кальция, входящего в состав костей, приходится также 20% от массы костей, а кальция в фосфате - 40%. Зная массу своего тела, рассчитайте сколько кг фосфата кальция содержится в организме (каждый ведет расчет индивидуально для своего организма). Сколько молекул фосфата кальция содержится в организме?
Слайд 25
Ловушка для доверчивых
Пока вы проводили расчёты,
я налила в стаканчики минеральную воду, разложила конфеты. Кто
хочет выпить воды (плотность воды 1,2 г/мл, объем 150 мл)? А кто хочет съесть конфету( масса конфеты 15г, а сахара в ней 90%)?