тока.
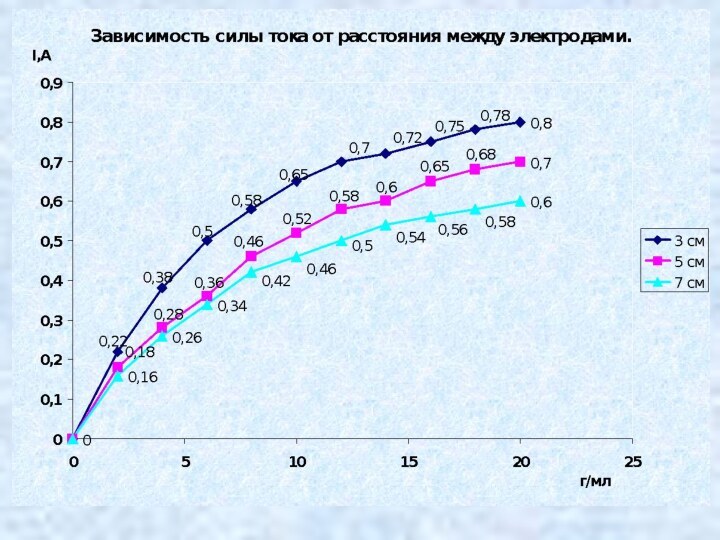
Установить, как влияет расстояния между электродами на силу
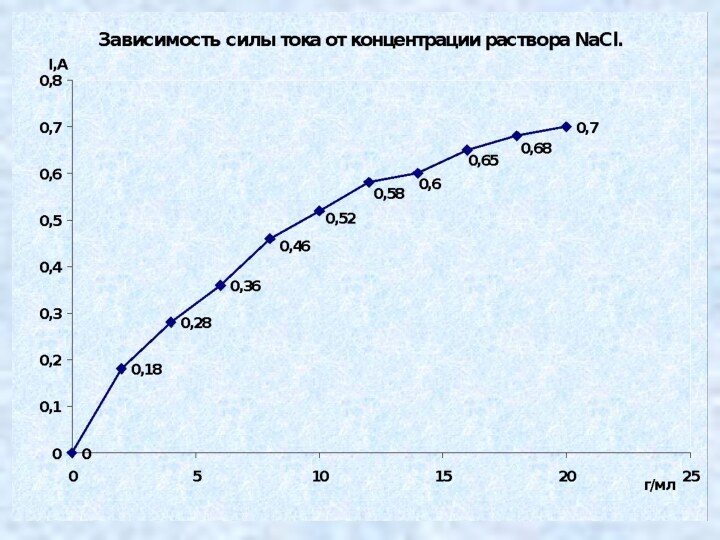
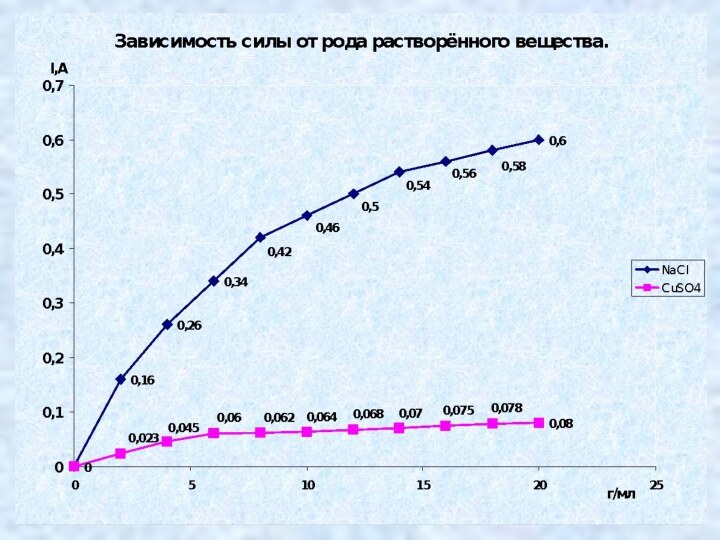
тока. Выяснить, как влияет природа электролита на силу тока в нём.
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть