- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Гибридизация Атома Углерода
Содержание
- 2. Строение электронной оболочки атома углерода12С*huВалентные электроны1s22s22p22s12p3Сафарова М.А., Саратов, 2013 г.
- 3. Гибридизация атома углеродаВ зависимости от количества орбиталей,
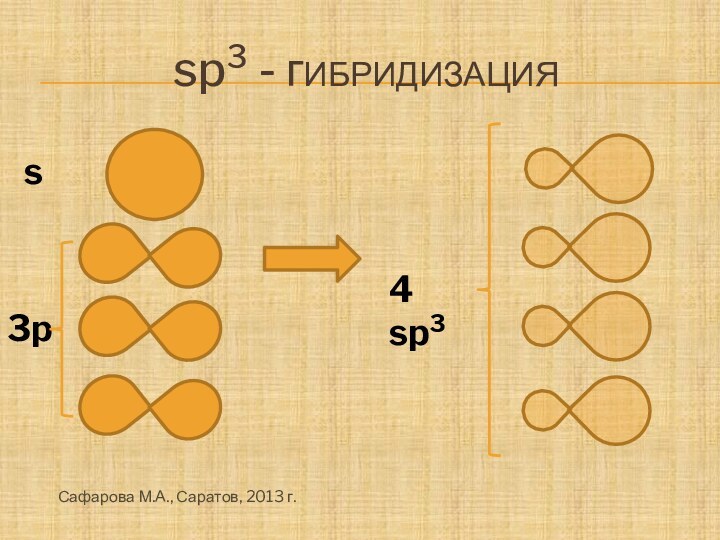
- 4. sp3 - гибридизация3ps4 sp3Сафарова М.А., Саратов, 2013 г.
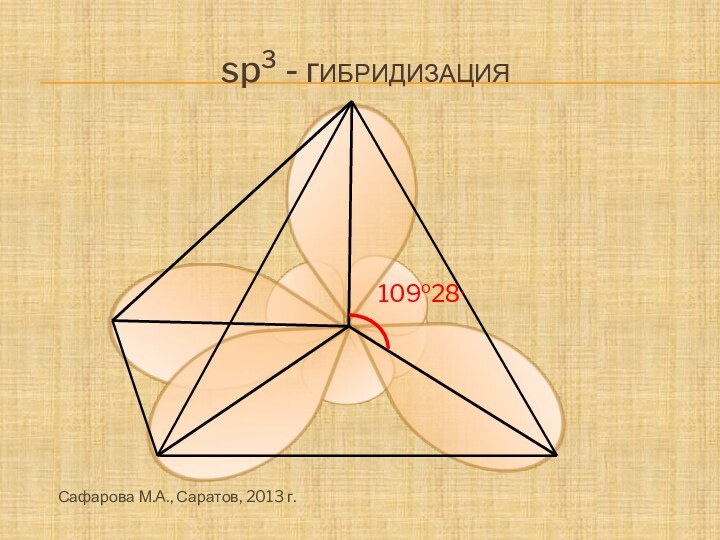
- 5. 109o28,sp3 - гибридизацияСафарова М.А., Саратов, 2013 г.
- 6. Строение углеродной цепи алкановМолекула метанаМолекула этана- Атомы
- 7. В алмазе атомы углерода находятся в sp3 – гибридизации. Сафарова М.А., Саратов, 2013 г.
- 8. Sp2 – гибридизация s3 sp22pСафарова М.А., Саратов, 2013 г.
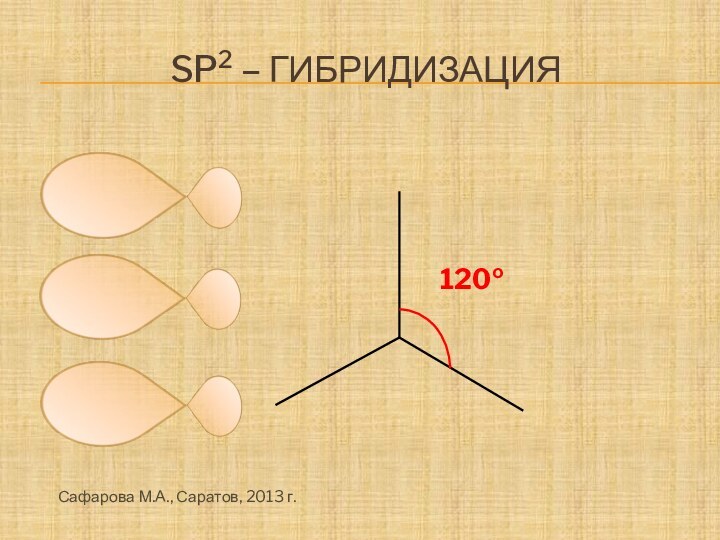
- 9. Sp2 – гибридизация 120оСафарова М.А., Саратов, 2013 г.
- 10. В соединениях с двойной C-C- связью гибридизованные
- 11. Строение молекулы бензолаВ молекуле бензола атомы углерода
- 12. В молекуле графита атомы углерода находятся в
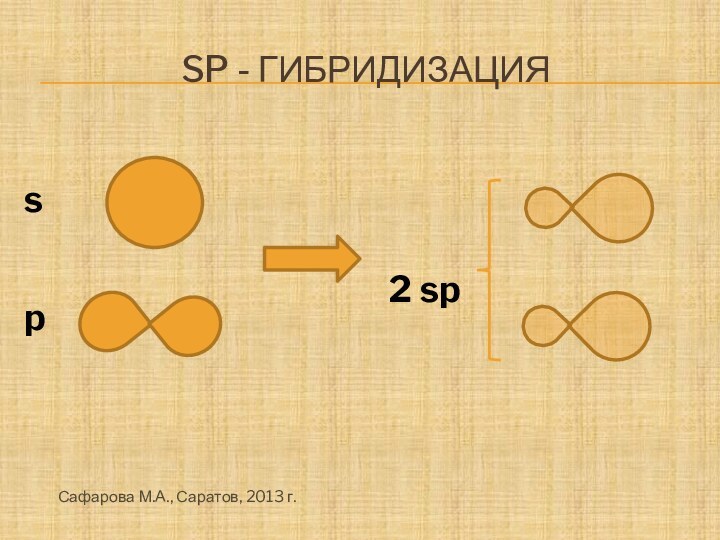
- 13. Sp - гибридизацияs2 sppСафарова М.А., Саратов, 2013 г.
- 14. Sp - гибридизация180оСафарова М.А., Саратов, 2013 г.
- 15. образование связей Sp- гибридизованные
- 16. Sp-гибритизация атомов углерода в молекулах карбинаИзотоп углерода
- 17. Скачать презентацию
- 18. Похожие презентации
Строение электронной оболочки атома углерода12С*huВалентные электроны1s22s22p22s12p3Сафарова М.А., Саратов, 2013 г.





Слайд 2
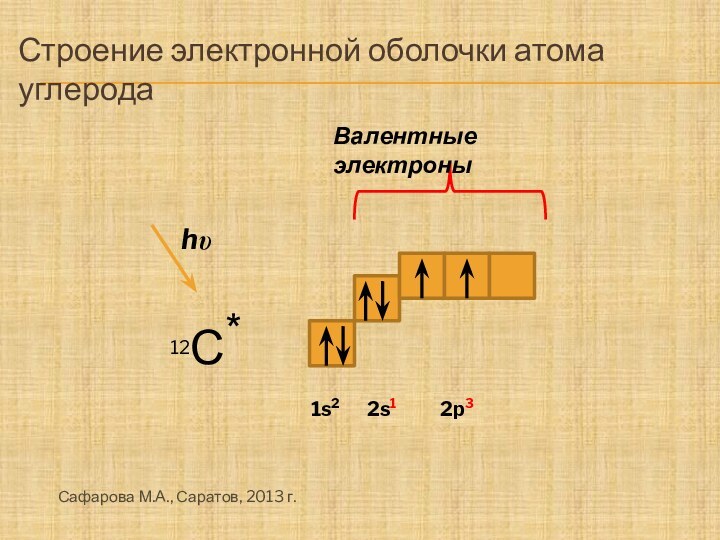
Строение электронной оболочки атома углерода
12С
*
hu
Валентные электроны
1s2
2s2
2p2
2s1
2p3
Сафарова М.А., Саратов,
2013 г.
Слайд 3
Гибридизация атома углерода
В зависимости от количества орбиталей, принимающих
участие в гибридизации, различают sp3-, sp2- и sp- гибридизацию.
Существуют
три типа гибридизации атомных орбиталей. Сафарова М.А., Саратов, 2013 г.
Слайд 6
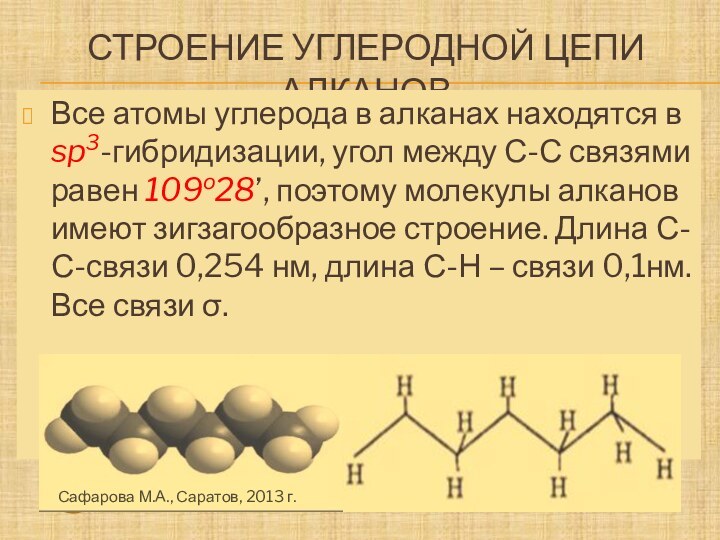
Строение углеродной цепи алканов
Молекула метана
Молекула этана
- Атомы водорода
Все
атомы углерода в алканах находятся в sp3-гибридизации, угол между
С-С связями равен 109о28’, поэтому молекулы алканов имеют зигзагообразное строение. Длина С-С-связи 0,254 нм, длина С-Н – связи 0,1нм.Все связи σ.Сафарова М.А., Саратов, 2013 г.
Слайд 10 В соединениях с двойной C-C- связью гибридизованные sp2-
орбитали расположены в одной плоскости, образуя σ-связи. Негибридизованные р-орбитали
перекрываются в перпендикулярной плоскости, образуя π-связь. Длина двойной С-С-связи составляет 0,134 нм.Сафарова М.А., Саратов, 2013 г.
Слайд 11
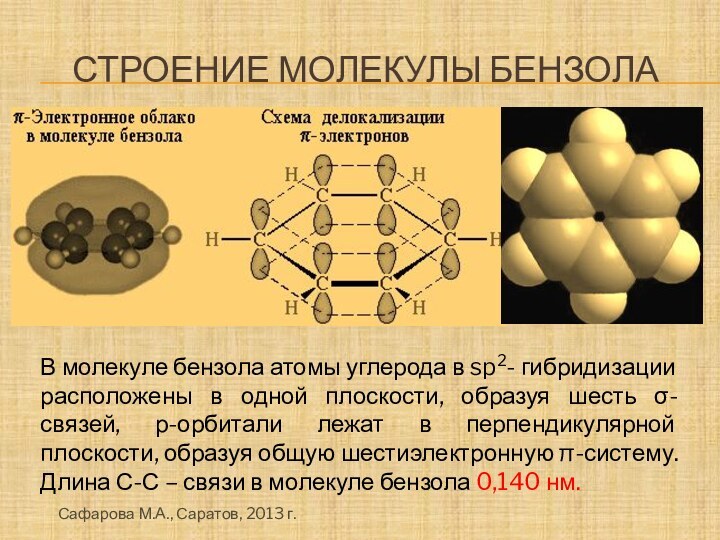
Строение молекулы бензола
В молекуле бензола атомы углерода в
sp2- гибридизации расположены в одной плоскости, образуя шесть σ-связей,
р-орбитали лежат в перпендикулярной плоскости, образуя общую шестиэлектронную π-систему. Длина С-С – связи в молекуле бензола 0,140 нм.Сафарова М.А., Саратов, 2013 г.
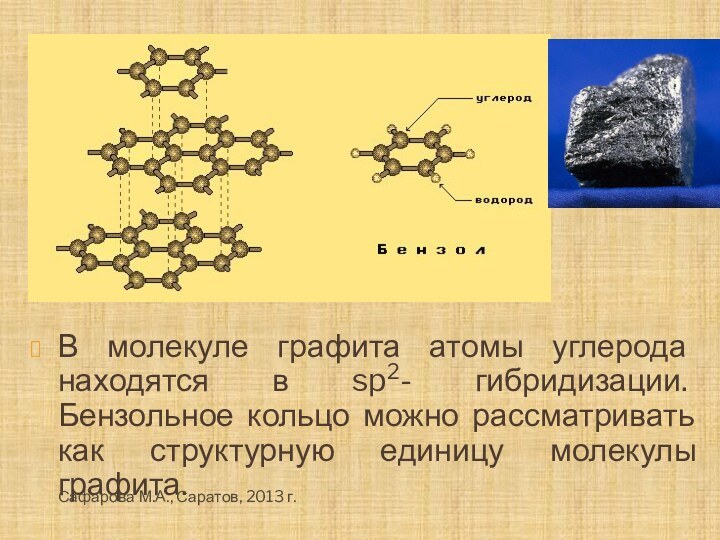
Слайд 12 В молекуле графита атомы углерода находятся в sp2-
гибридизации. Бензольное кольцо можно рассматривать как структурную единицу молекулы
графита.Сафарова М.А., Саратов, 2013 г.
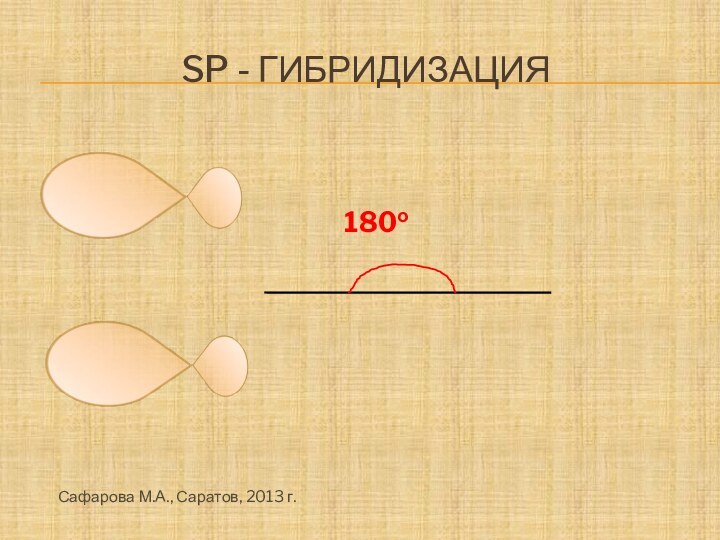
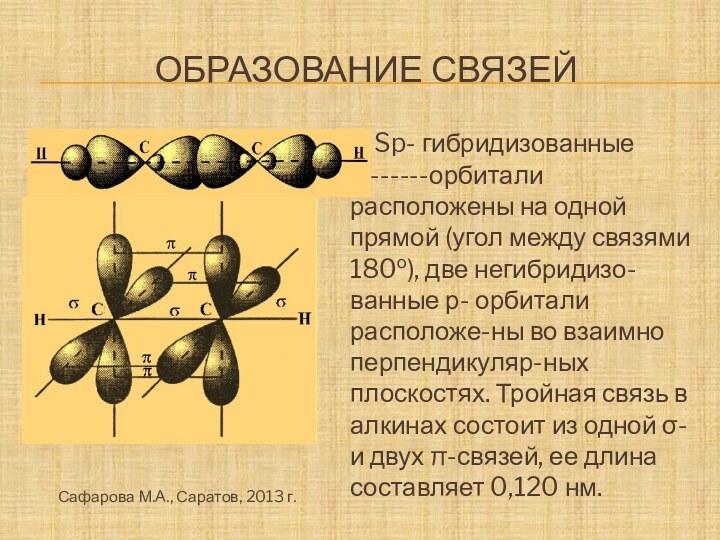
Слайд 15
образование связей
Sp- гибридизованные
--------орбитали расположены на одной прямой (угол
между связями 180о), две негибридизо-ванные р- орбитали расположе-ны во взаимно перпендикуляр-ных плоскостях. Тройная связь в алкинах состоит из одной σ- и двух π-связей, ее длина составляет 0,120 нм.Сафарова М.А., Саратов, 2013 г.
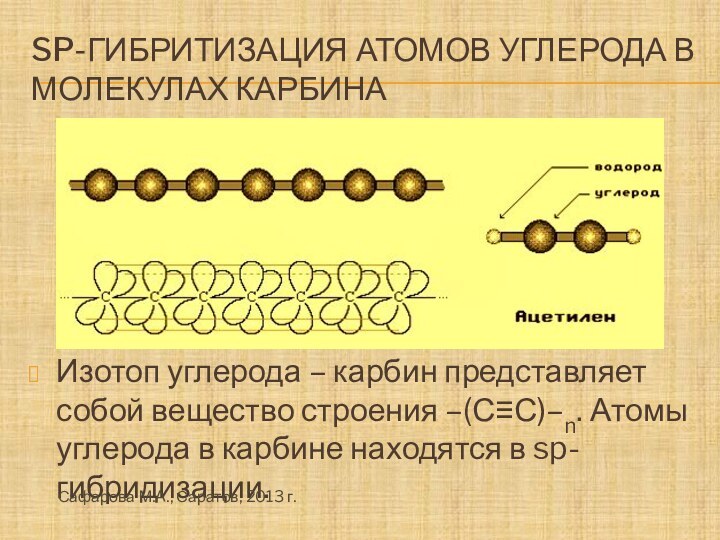
Слайд 16
Sp-гибритизация атомов углерода в молекулах карбина
Изотоп углерода –
карбин представляет собой вещество строения –(С≡С)–n. Атомы углерода в
карбине находятся в sp-гибридизации.Сафарова М.А., Саратов, 2013 г.