- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему атомная физика 11 класс
Содержание
- 2. План урока 1.
- 3. Конец XIX века. Из истории физики…1869г.
- 4. Модель атома Томсона-е+е-е
- 5. Эрнест Резерфорд (1871-1937) – великий английский физик
- 6. 1909-1913 гг. Опыты РезерфордаЦель:1. Исследование распределения
- 7. 1909-1913 гг. Опыты Резерфорда
- 8. 1909-1913 гг. Опыты РезерфордаРезультаты:1. Большинство частиц
- 9. 1909-1913 гг. Опыты Резерфорда.Выводы:1. Положительный заряд
- 10. Планетарная модель атома
- 11. Противоречие между экспериментальными данными и теорией
- 12. Нильс Бор (1885-1962) великий датский физикЕсть
- 13. 1913 г. Нильс БорРазрешая противоречия, учёл:1. Линейчатый
- 14. Постулаты Бора1. Атомная система может находиться только
- 15. Постулаты Бора2. Излучение света происходит при переходе
- 16. Постулаты Бора 3. Возможен дискретный ряд орбит
- 17. Энергетические уровни атома водорода0 эВ10.2 эВ12.1 эВ12.8
- 18. Скачать презентацию
- 19. Похожие презентации
План урока 1. Из истории физики 2. Модель Томсона 3. Опыт Резерфорда 4. Противоречия 5.Постулаты Бора 6.Энергетическая диаграмма атома водорода 7. Сообщения о Э.Резерфорде и Н. Боре















Слайд 3
Конец XIX века.
Из истории физики…
1869г. Д.Менделеев открыл
1896 г. А.Беккерель открыл явление
радиоактивности
1897 г. Томсон открыл электрон
1903 г. Томсон предложил модель атома
Слайд 5
Эрнест Резерфорд (1871-1937) – великий английский физик
Науки
делятся на две группы - на физику и
собирание
марок
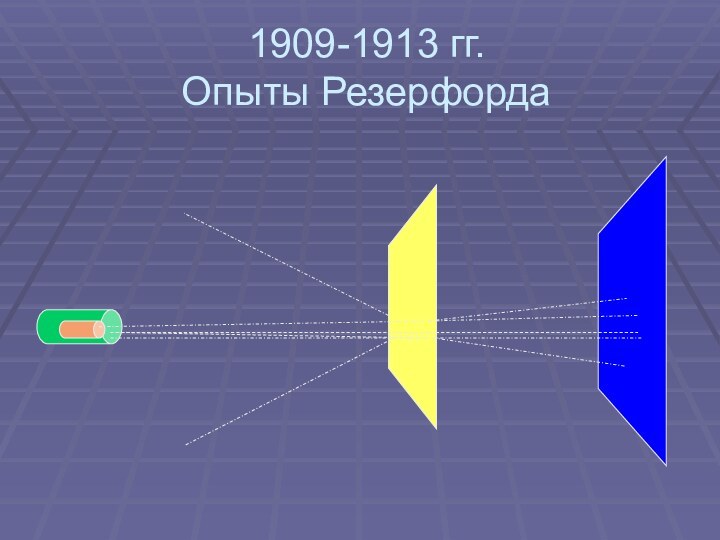
Слайд 6
1909-1913 гг.
Опыты Резерфорда
Цель:
1. Исследование распределения
положительного заряда
2. Исследование распределения
массы внутри
атома
Слайд 8
1909-1913 гг.
Опыты Резерфорда
Результаты:
1. Большинство частиц проходит
через фольгу не отклоняясь
2. Небольшое
число альфа частиц(примерно 1 из 2000)
отклонилось на углы, больше 90°
Слайд 9
1909-1913 гг.
Опыты Резерфорда.
Выводы:
1. Положительный заряд атома и
его масса сконцентрированы в очень малой области пространства –
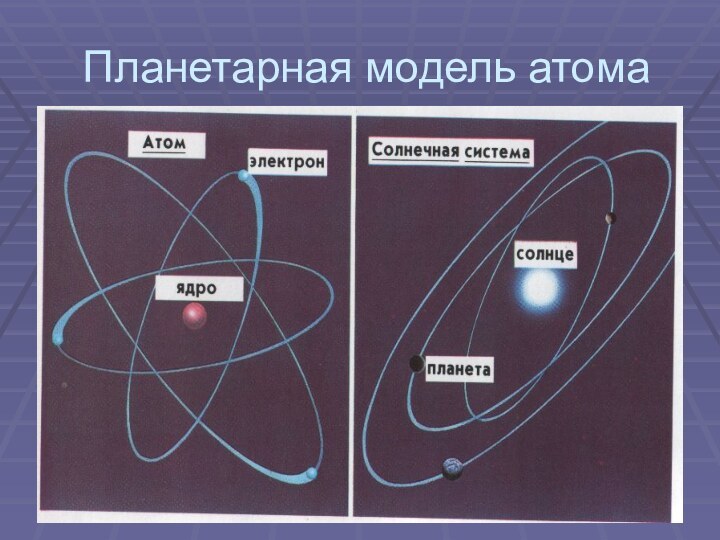
ядро2. Предложена новая модель атома – планетарная
3. Ядро имеет диаметр 10 -12 -10 -13 см
4. Размер атома 10 -8 см
5. Заряд ядра равен номеру химического элемента по таблице Д.И.Менделеева
Слайд 11
Противоречие
между экспериментальными данными и теорией
Ускоренное движение
электрона по орбите должно сопровождаться постоянным излучением
Излучение сопровождается излучением
энергии и электрон должен двигаться по спирали в итоге должен упасть на ядро
Слайд 12
Нильс Бор (1885-1962)
великий датский физик
Есть два вида
истины - тривиальная, которую отрицать нелепо, и глубокая, для
которой обратное утверждение - тоже глубокая истина
Слайд 13
1913 г. Нильс Бор
Разрешая противоречия, учёл:
1. Линейчатый спектр
атомов
2. Модель атома Резерфорда
3. Квантовый характер испускания и поглощения
энергии
Слайд 14
Постулаты Бора
1. Атомная система может находиться только в
особых стационарных, или квантовых состояниях, каждому из которых соответствует
определенная энергия Е n ; в стационарном состоянии атом не излучаетЕ1
Е2
+
+
Слайд 15
Постулаты Бора
2. Излучение света происходит при переходе атома
из стационарного состояния с большей энергией Еk в стационарное
состояние с меньшей энергией Еn Энергия излученного фотона равна разности энергий стационарных состояний: hv =E k– En hv
+
hv
hv
Слайд 16
Постулаты Бора
3. Возможен дискретный ряд орбит по
которым электрон может двигаться в стационарном состоянии:
m v
r = n h, m-масса электрона,
v -скорость электрона,
r-радиус данной орбиты,
n-номер орбиты,
h-постоянная (1,05•10-34 Дж•с)
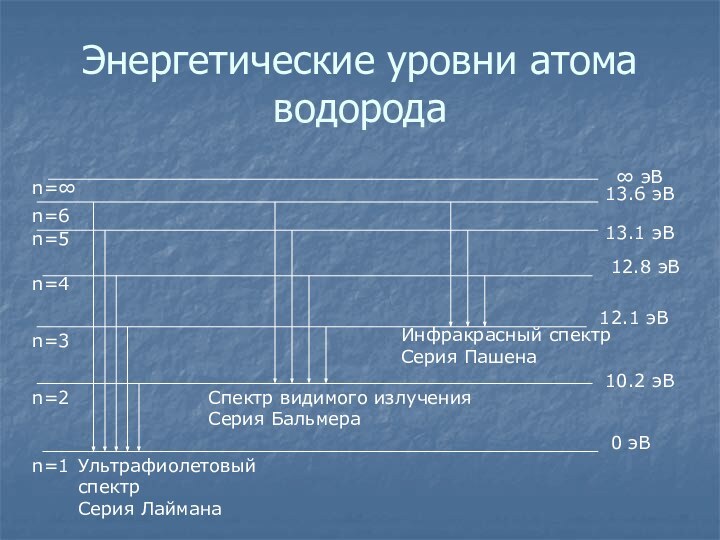
Слайд 17
Энергетические уровни атома водорода
0 эВ
10.2 эВ
12.1 эВ
12.8 эВ
13.1
эВ
13.6 эВ
∞ эВ
n=1
n=2
n=3
n=4
n=5
n=6
n=∞
Ультрафиолетовый спектр
Серия Лаймана
Спектр видимого излучения
Серия Бальмера
Инфракрасный
спектрСерия Пашена