- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Строение атома и атомного ядра
Содержание
- 2. Цели: Изучить строение атомаЗакрепить умение составлять электронно-графические, электронно-волновые модели атомаЗакрепить умение записывать электронные формулы атомов2
- 3. Атом и ядроАтом- наименьшая электронейтральная частица химического
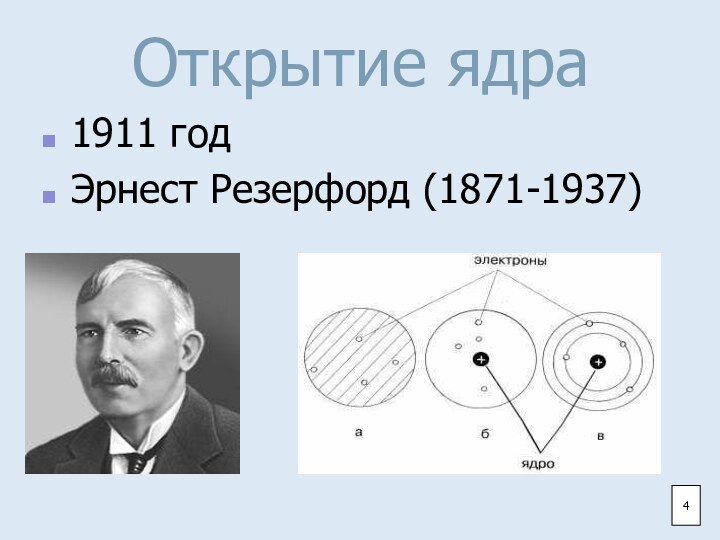
- 4. Открытие ядра1911 годЭрнест Резерфорд (1871-1937)4
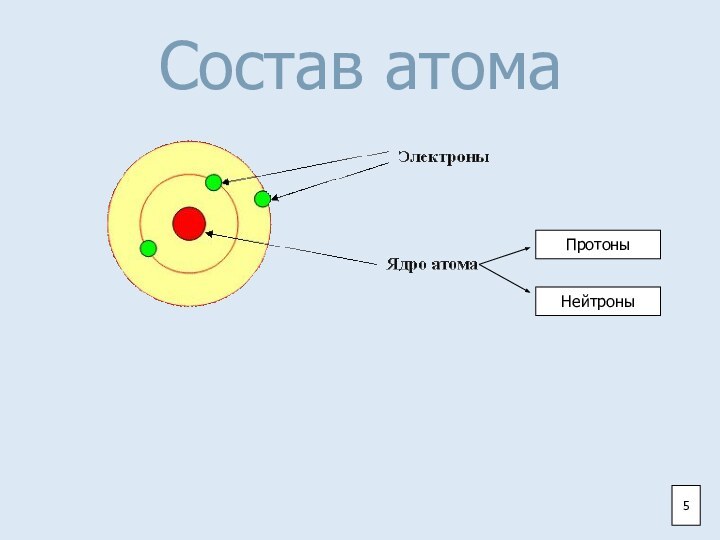
- 5. Состав атомаПротоныНейтроны5
- 6. Расчёт числа протонов, нейтронов и электроновma =m1p+m1n
- 7. Пример:Элемент калий (№ 19) ma = 39
- 8. Нахождение электрона в атомеОрбиталь - область пространства
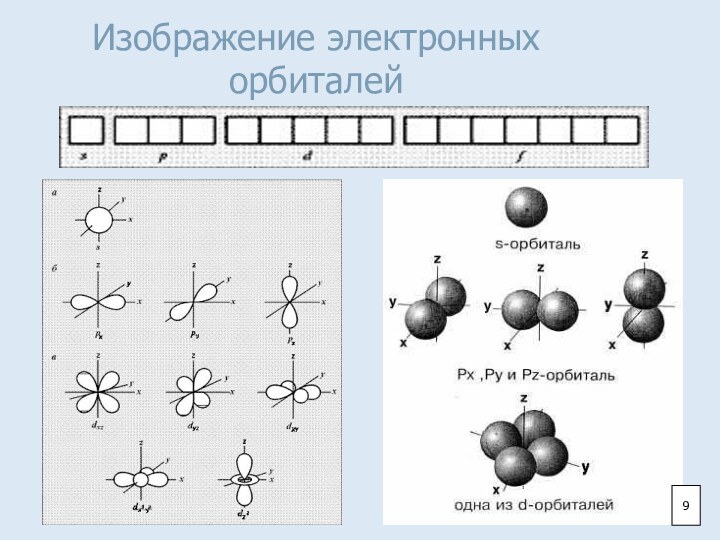
- 9. Изображение электронных орбиталей9
- 10. Энергетический уровень (электронный слой)Энергетический уровень (1,2,3…)-характеризует энергию
- 11. Уровни, подуровни и орбитали11
- 12. Правила распределения электронов на энергетическом уровнеМаксимальное число
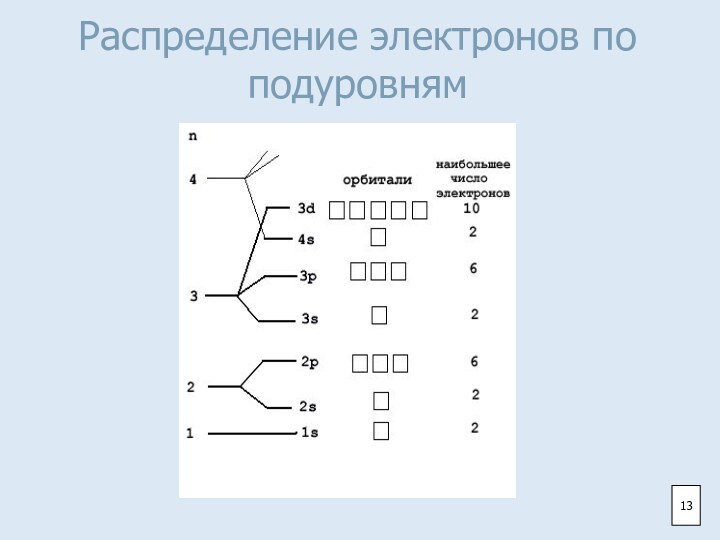
- 13. Распределение электронов по подуровням13
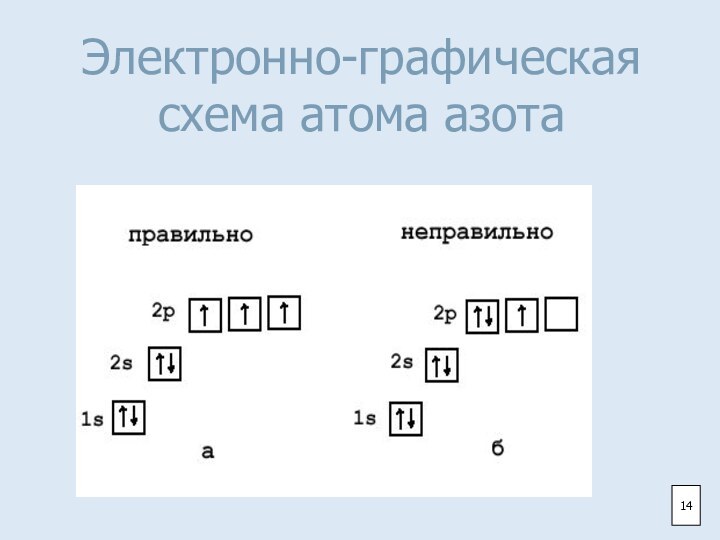
- 14. Электронно-графическая схема атома азота14
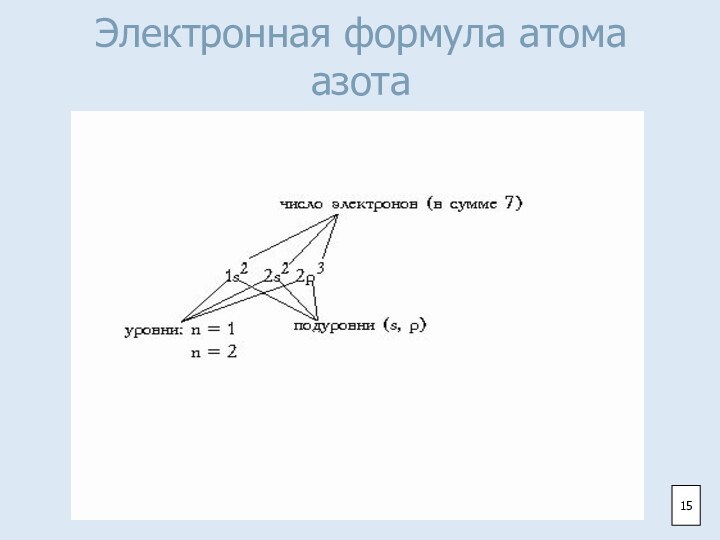
- 15. Электронная формула атома азота15
- 16. Примеры электронных формул атомов16
- 17. Контролирующие материалыВыполните задания из данного разделаПроверьте правильность выполнения заданийПоставьте себе оценку за работу17
- 18. Атом - это наименьшая … частица химического
- 19. Задание 2 Выберите правильный ответ: 1.
- 20. Задание 3 Назовите частицы, из которых состоит атом и покажите их обозначение20
- 21. Задание 4 Заполните электронно-графическую схему атома азота 2р 2s1sНапишите электронную формулу21
- 22. электронейтральная ядра, электронной ядро4. Э.Резерфорд,
- 23. Задание 21- А2- Б3- Г4- В5- А6- Б23
- 24. Задание 324
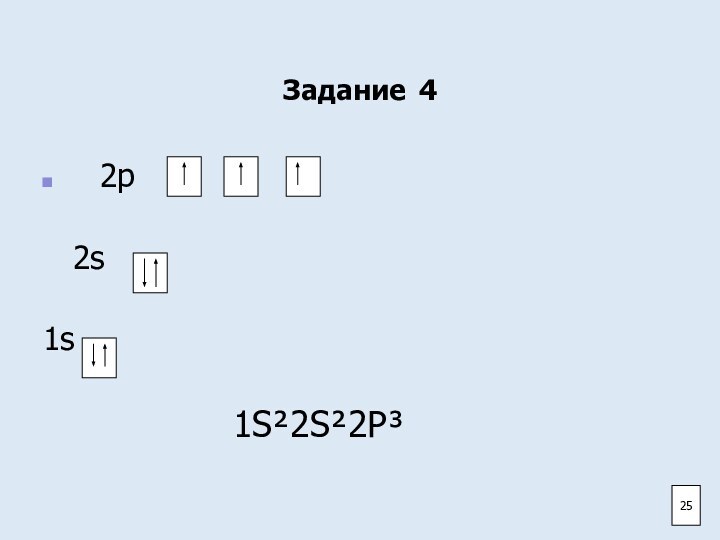
- 25. Задание 4 2р
- 26. Скачать презентацию
- 27. Похожие презентации
Цели: Изучить строение атомаЗакрепить умение составлять электронно-графические, электронно-волновые модели атомаЗакрепить умение записывать электронные формулы атомов2



















Слайд 2
Цели:
Изучить строение атома
Закрепить умение составлять электронно-графические, электронно-волновые
модели атома
Слайд 3
Атом и ядро
Атом- наименьшая электронейтральная частица химического элемента.
Атом
состоит из ядра и электронной оболочки.
Ядро состоит из
протонов и нейтронов.3
Слайд 6
Расчёт числа протонов, нейтронов и электронов
ma =m1p+m1n
1
01p=Zя=№элемента
1
e¯=1p=Zя=№элемента
1
1n =ma - m1p
0 1
6
Слайд 8
Нахождение электрона в атоме
Орбиталь - область пространства вокруг
ядра атома, где наиболее вероятно нахождение электрона.
На одной орбитали
может находиться не более двух электронов.8
Слайд 10
Энергетический уровень (электронный слой)
Энергетический уровень (1,2,3…)-характеризует энергию связи
электрона с ядром.
На одном уровне располагаются электроны, имеющие орбитали
разной формы, но с близким по величине запасом энергии.Внутри энергетического уровня в зависимости от формы орбиталей различают подуровни
(s, p, d, f).
10
Слайд 12
Правила распределения электронов на энергетическом уровне
Максимальное число электронов
на энергетическом уровне рассчитывается по формуле: N=2n² (n-порядковый номер
энергетического уровня).Например, 1-ый уровень (n=1) – 2 электрона, 2-ой уровень (n=2) – 8 электронов и т.д.
На внешнем энергетическом уровне может располагаться не более 8 электронов.
12
Слайд 17
Контролирующие материалы
Выполните задания из данного раздела
Проверьте правильность выполнения
заданий
Поставьте себе оценку за работу
17
Слайд 18
Атом - это наименьшая … частица химического элемента.
Атом
состоит из … и … оболочки.
3. … состоит
из протонов и нейтронов.4. В 1911 г. английский ученый … доказал, что в центре атома имеется … заряженное ядро.
5. В состав атомного ядра входят … и …
6. Число электронов, движущихся вокруг ядра атома, равно … … элемента.
7. Порядковый номер химического элемента совпадает с … … его атома.
8. Электроны, которые обладают наименьшим запасом энергии, находятся на первом … уровне.
9. Число энергетических уровней у элементов определяется по номеру …
10.На одной орбитали может располагаться только …электрона.
Задание 1
Вставьте пропущенные слова:
18
Слайд 19
Задание 2
Выберите правильный ответ:
1. Количество электронов у атома
углерода равно:
А) 6
Б) 12
В) 7
Г) 0
2. Количество нейтронов у
атома калия равно:А) 39
Б) 20
В) 19
Г) 59
3. Масса атома равна сумме масс:
А) нейтронов
Б) электронов
В) протонов
Г) протонов и нейтронов
4. Максимальное число электронов, которые могут находиться на одной орбитали:
А) 1
Б) 3
В) 2
Г) 0
5. Число электронов на внешнем энергетическом уровне у атома азота:
А) 5
Б) 2
В) 7
Г) 14
6. S-орбитали имеют форму:
А) правильной восьмерки
Б) шара
В) неправильной восьмерки
Г) квадрата
19
Слайд 21
Задание 4
Заполните электронно-графическую схему атома азота
2р
2s
1s
Напишите электронную формулу
21
Слайд 22
электронейтральная
ядра, электронной
ядро
4. Э.Резерфорд,
положительно
5. протоны и нейтроны
6. порядковому номеру
7.
зарядом ядра8. энергетическом
9. периода
10. два
Правильные ответы
Задание 1
22





























