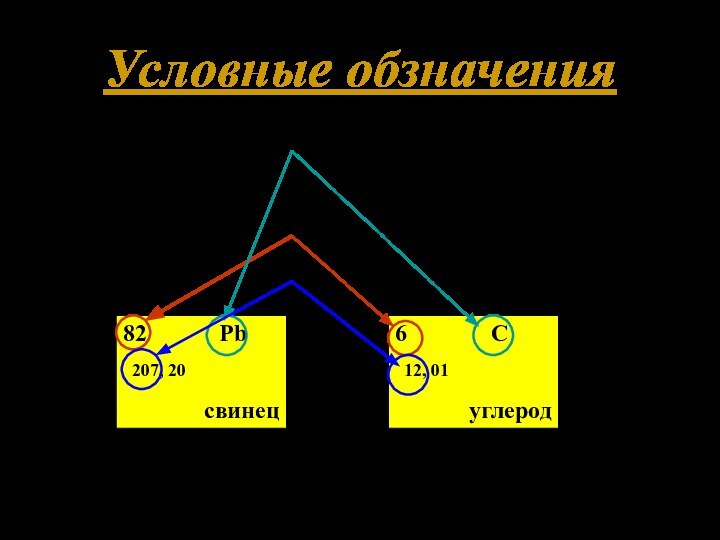
номер,
А – массовое число.
82 Pb
207, 20свинец
6 C
12, 01
углерод
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть















6 C
12, 01
углерод
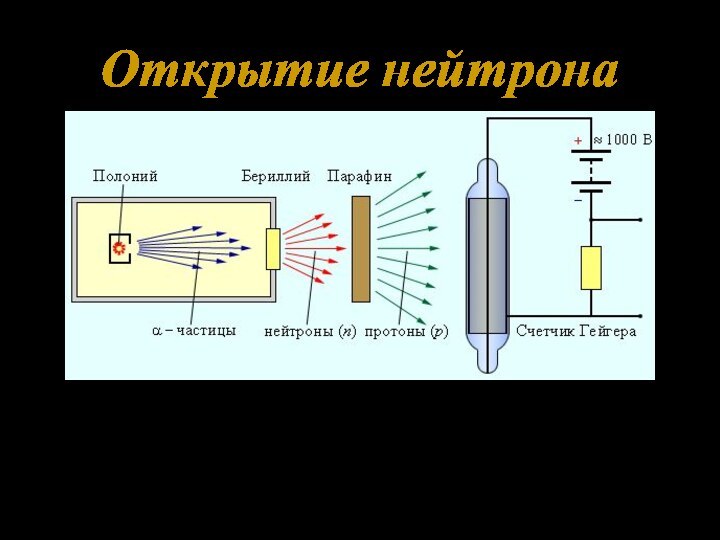
Протоны и нейтроны принято называть нуклонами.