- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Ток в растворах
Содержание
- 2. Цели урока.Исследование электропроводности твердых тел.Исследование электропроводности растворов веществ и формирование понятия об электролитах.Установление причин электропроводности.
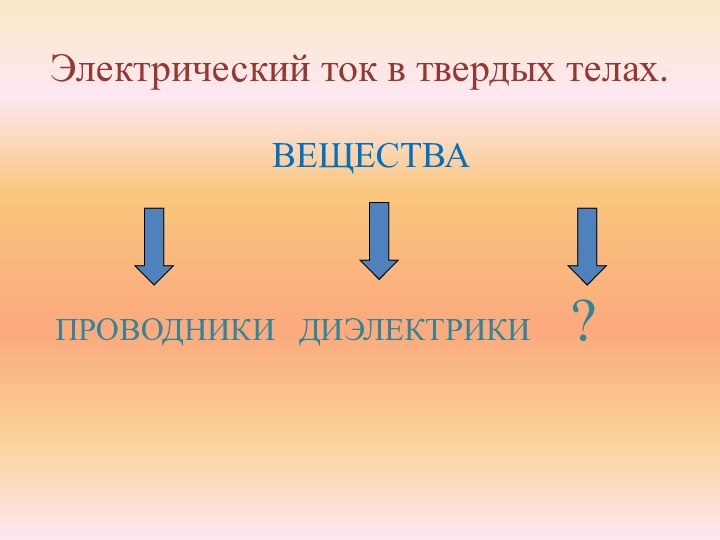
- 3. Электрический ток в твердых телах.
- 4. Опыт по исследованию проводимости различных тел. металл
- 5. Фильм о проводимости металлов.
- 6. Характеристики электронаm= 9,1 *10 -31 кгe = - 1,6 *10 -19 Кл
- 7. Причины электропроводимости металлов и неметаллов. 1) Наличие
- 8. Изучение электропроводимости различных веществ и их растворов. ?
- 9. Лабораторный опыт : Демонстрация электролитической проводимости растворов.Исследуем
- 10. Проводники NaCl растворNaOH раствор,HCl раствор CuSO4 растворЭлектролиты:кислоты, соли,основания в раствореДиэлектрикиNaCl кристаллическийСuSO4 кристаллическийСахар Чистая водаНеэлектролиты:оксиды
- 11. Механизм электролитической диссоциации.Схема электролитической диссоциации.
- 12. Степень диссоциации a = Nдисс./ N oбщее
- 13. Задание на выбор сильного электролита и составление
- 14. Выводы.1.На какие группы делятся вещества по электропроводности?
- 15. Скачать презентацию
- 16. Похожие презентации
Цели урока.Исследование электропроводности твердых тел.Исследование электропроводности растворов веществ и формирование понятия об электролитах.Установление причин электропроводности.














Слайд 2
Цели урока.
Исследование электропроводности твердых тел.
Исследование электропроводности растворов веществ
и формирование понятия об электролитах.
Слайд 4
Опыт по исследованию проводимости различных тел.
металл
дерево
резина
стекло
графит
На основе полученных наблюдений сделайте выводы.
Слайд 7
Причины электропроводимости
металлов и неметаллов.
1) Наличие свободных электронов в
кристаллической решетке металла.
2) Особенности строения кристаллической решетки графита.
Слайд 9
Лабораторный опыт : Демонстрация электролитической проводимости растворов.
Исследуем проводимость
веществ:
1) NaClр-р,
2)NaCl кр.,
3) сахар,
4)H2O дист.,
5) NaOHр-р,
6)HCl р-р
7)CuSO4
кр.8)CuSO4 р-р.
.
Слайд 10
Проводники
NaCl раствор
NaOH раствор,
HCl раствор
CuSO4 раствор
Электролиты:
кислоты, соли,
основания в
растворе
Диэлектрики
NaCl кристаллический
СuSO4 кристаллический
Сахар
Чистая вода
Неэлектролиты:
оксиды
Слайд 12 Степень диссоциации a = Nдисс./ N oбщее ;N- число
молекул
Сильные электролиты
1. Неорганические кислоты: HCl, H2SO4
2. Щелочи( растворимые основания):
КОН , NaOH3. Соли: NaCI (Р)
а = 1 (100%)
Слабые электролиты
1. Органические кислоты : СН3СООН
2. Неорганические кислоты: Н2S,H2SiO3 (Н)
H2CO3 = H2O + CO2
H2SO3 = H2O + SO2
3. Основания:
NH4OH = NH3 + H2O
4. Cоли, основания нерастворимые в воде.
Слайд 13 Задание на выбор сильного электролита и составление схемы
диссоциации на ионы:
Даны формулы веществ: Al(OH)3, НNO3,
ВaSO4, KOH,
AgCl, H2SiO3Пользуясь таблицей растворимости, выберите те, которые проводят электрический ток в растворе. Составьте схемы их диссоциации на ионы. Ответ поясните.
Слайд 14
Выводы.
1.На какие группы делятся вещества по электропроводности?
2.
Почему твердые вещества проводят электрический ток?
3. Почему растворы некоторых
веществ проводят электрический ток?4. Как называются такие вещества?