- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Сероводород. Сернистый водород, сульфид водорода, дигидросульфид
Содержание
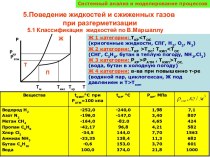
Сероводород (сернистый водород, сульфид водорода, дигидросульфи́д) — бесцветный газ со сладковатым вкусом, имеющий запах протухших куриных яиц. Бинарное химическое соединение водорода и серы. Химическая формула — H2S. Плохо растворим в воде, хорошо — в этаноле. В больших концентрациях ядовит, взаимодействует со многими металлами. Огнеопасен. Концентрационные пределы воспламенения в смеси




Слайд 2 Сероводород (сернистый водород, сульфид водорода, дигидросульфи́д) — бесцветный газ со сладковатым вкусом,
Слайд 3 Нахождение в природе В природе встречается редко в составе попутных
нефтяных газов, природного газа, вулканических газах, в растворённом виде в природных
водах (например, в Чёрном море слои воды, расположенные глубже 150—200 м, содержат растворённый сероводород). Образуется при гниении белков (только тех, которые содержат в составе серосодержащие аминокислоты метионин и/или цистеин). Небольшое количество сероводорода содержится в кишечных газах человека и животных.
Слайд 4
Физические свойства:
Термически устойчив (при температурах больше 400 °C разлагается
на простые вещества — S и H2). Молекула сероводорода имеет изогнутую форму, поэтому она полярна (μ
= 0,34·10−29 Кл·м). В отличие от молекул воды, в сероводороде атомы водорода не образуют прочных межмолекулярных водородных связей, поэтому сероводород является газом. Раствор сероводорода в воде — очень слабая сероводородная кислота. Является сверхпроводником при температуре 203 К (-70 °C) и давлении 150 ГПа.Получение сероводорода.
1. В лаборатории H2S получают в ходе реакции между сульфидами и разбавленными кислотами:
FeS + 2HCl = FeCl2 + H2S,
2. Взаимодействие Al2S3 с холодной водой (образующийся сероводород более чистый, чем при первом способе получения):
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S.