в природе.
Способы получения металлов.
4. Металлы в ПСХЭ Д.И.Менделеева.
5.
Особенности строения атомов. 6. Металлическая связь.
7. Физические свойства.
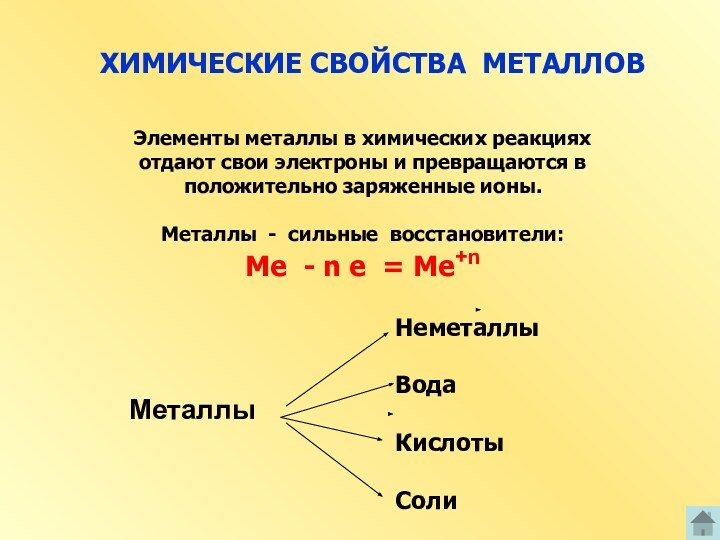
8. Химические свойства.
9. Применение.
10. Вопросы для закрепления материала.