- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Уравнение Менделеева - Клапейрона
Содержание
- 2. Уравнение Клапейрона p V=BT B-коэффициент пропорциональности зависит от природы и массы тела
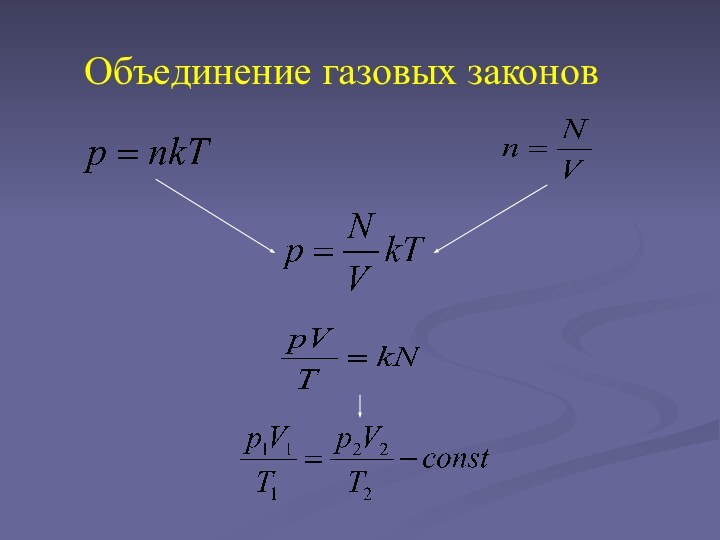
- 3. Объединение газовых законов
- 4. Уравнение Менделеева-Клапейрона. Уравнение состояния идеального газа.Д.И.Менделеев объединил
- 5. PV=n R T PV=n k T, где
- 6. Задание№1.Определите массу 5.6 аргона при давлении 202.6
- 7. Решение к заданию №1.Определяем объем аргона при
- 8. Решение к заданию №2.Для расчетов выбираем образец
- 9. Мосты Санкт-Петербурга
- 10. Первый инженерный мост
- 11. Второй инженерный мост
- 13. Список использованных источников:а) Список используемых печатных источниковД,
- 14. Скачать презентацию
- 15. Похожие презентации
Уравнение Клапейрона p V=BT B-коэффициент пропорциональности зависит от природы и массы тела













Слайд 2 Уравнение Клапейрона p V=BT B-коэффициент пропорциональности зависит от
природы и массы тела
Слайд 4
Уравнение Менделеева-Клапейрона.
Уравнение состояния идеального газа.
Д.И.Менделеев объединил уравнение Клапейрона
с законом Авогадро, отнеся уравнение к одному молю. От
него можно перейти к произвольной массе газа.PV=m\M*RT
М-масса одного моля вещества,R- универсальная газовая постоянная
Слайд 5
PV=n R T
PV=n k T,
где n
–концентрация молекул, число молекул в единице объёма ,
k- постоянная
БольцманаPV= N k T
Слайд 6
Задание№1.
Определите массу 5.6 аргона
при давлении 202.6 кПа
и температуре.
Задание№2.
Определите плотность воздуха при давлении 2 атм.
и температуре 300К.
Слайд 7
Решение к заданию №1.
Определяем объем аргона при н.у.,
используя для расчетов уравнения и учитывая, что Т =
273+27=300К :V0(Ar)=PVT0 / P0T
V(Ar)/22,4 л/моль;
v(Ar) = 10.2 / 22.4= 0.455 моль
Рассчитываем массу аргона :
m(Ar)= v(Ar)* M(Ar);
m(Ar)= 0.45V0(Ar)=(202.6 *5.6*273) / (300*101.3) = 10.2л
Количество аргона будет равно:
v(Ar)= 5 * 40 =18.2г
Слайд 8
Решение к заданию №2.
Для расчетов выбираем образец воздуха
количеством вещества 1 моль. Молярная масса воздуха равна 29г/моль.
Тогда масса образца будет равна :m(воздуха)=v(воздуха) * M(воздуха)
Объем воздуха при н.у. будет равен :
V0(воздуха)= v(воздуха)* 22.4 л/моль
V0(воздуха)= 1* 22.4=22.4 л.
Определяем объем воздуха при заданных условиях, используя уравнение
V(воздуха)=P0V0T / PT0
V(воздуха)=(1 * 22/4 * 300) / (2*273) = 12.3 л
Рассчитываем плотность воздуха при заданных условиях по уравнению
p( плотность воздуха)= m(воздуха) / V(воздуха)
p(плотность воздуха) = 29 / 12,3 = 2.36 г/л.





























